Clear Sky Science · it
Sintesi e valutazione biologica di complessi di Schiff a base di ibuprofene/o-vanillina con attività antinfiammatorie, antiproliferative e anti‑SARS‑COV‑19
Perché aggiornare un analgesico familiare è importante
L'ibuprofene è uno dei farmaci più usati al mondo per il dolore e la febbre, ma l'uso prolungato può irritare lo stomaco e non è mai stato progettato per combattere infezioni, cancro o nuovi virus. In questo studio i chimici reingegnerizzano l'ibuprofene fissandolo a una molecola naturale simile alla vaniglia e quindi legando diversi metalli. Il risultato è una famiglia di nuovi composti che agiscono non solo come analgesici, ma come potenziali antibiotici, agenti anticancro, farmaci antinfiammatori e persino inibitori di un enzima chiave del SARS‑CoV‑2, offrendo al contempo indicazioni su come progettare farmaci più intelligenti partendo da medicinali di uso comune.
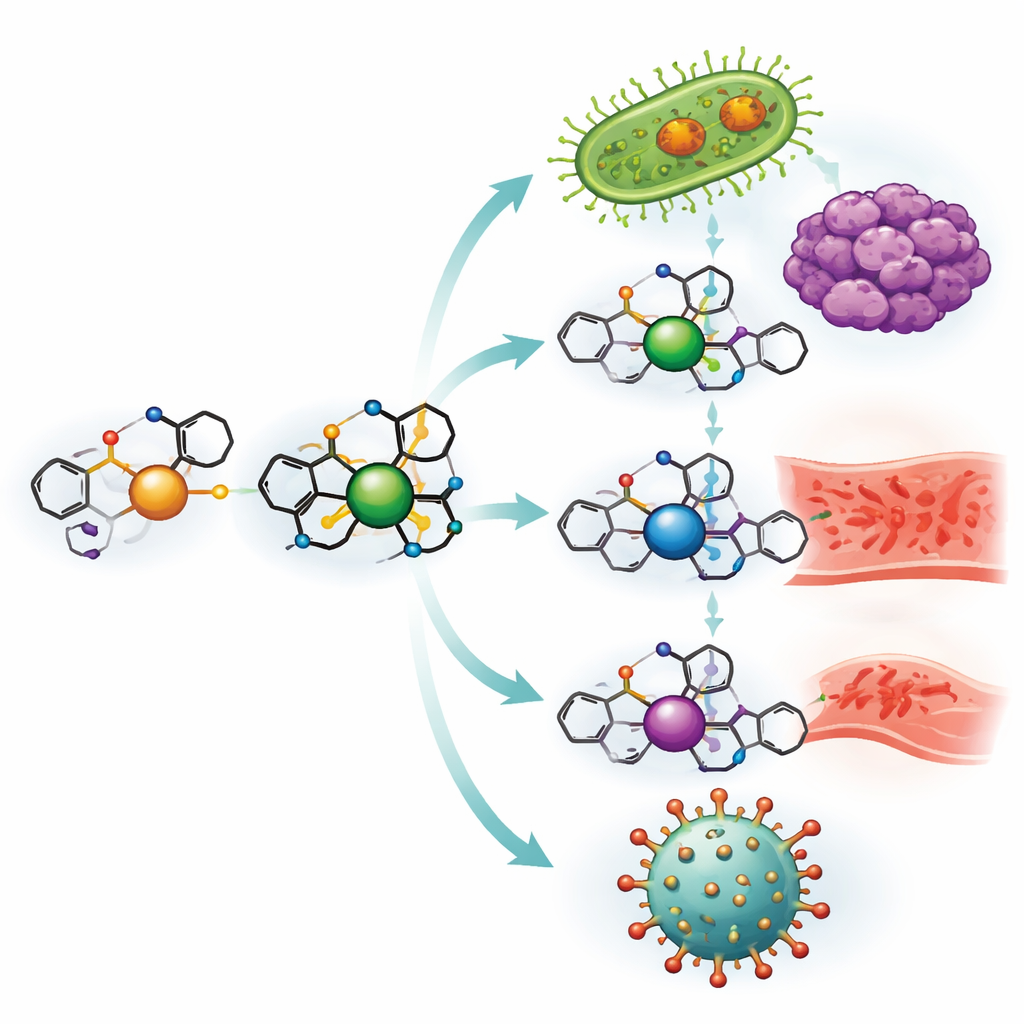
Costruire nuove molecole dal profilo farmacologico a partire dall'ibuprofene
Il gruppo ha iniziato trasformando l'ibuprofene in un blocco più versatile e poi collegandolo all'o‑vanillina, una stretta parente chimica del composto aromatico della vaniglia. Insieme formano un ligando di tipo “Schiff base”—essenzialmente una pinza su misura in grado di trattenere ioni metallici. Questo ligando è stato quindi combinato separatamente con sali di rame, nichel, zinco e vanadio per ottenere quattro distinti complessi metallici. Test di laboratorio accurati, incluse misure di comportamento al calore di fusione, assorbimento di luce, proprietà magnetiche e struttura cristallina, hanno confermato come il ligando avvolge ciascun metallo e quanto siano stabili i complessi risultanti, anche a elevate temperature e su un ampio intervallo di acidità.
Come i complessi interagiscono con le cellule e il DNA
Poiché l'efficacia di un farmaco spesso dipende dal modo in cui incontra bersagli biologici, i ricercatori hanno esaminato come questi nuovi complessi interagiscono con il DNA e le cellule viventi. In esperimenti in provetta, in particolare il complesso di rame si è legato saldamente a filamenti di DNA ed è stato in grado di danneggiarli o “tagliarli”, un comportamento spesso osservato in potenti agenti anticancro e antibatterici. Testati contro linee cellulari tumorali umane di seno, colon e fegato, tutti e quattro i complessi si sono mostrati più tossici per le cellule tumorali rispetto al solo ligando a base di ibuprofene, con il complesso di rame che si è avvicinato alla potenza del farmaco chemioterapico vinblastina a dosi simili.
Contrasto a germi, funghi e infiammazione
Gli stessi composti sono stati sfidati contro microrganismi patogeni comuni, inclusi batteri Gram‑positivi e Gram‑negativi e due funghi problematici. Anche in questo caso i complessi metallici hanno superato il ligando libero, con il rame in testa, che ha fortemente inibito sia batteri sia funghi. Gli autori interpretano questo attraverso la teoria della “chelazione”: una volta che il metallo è trattenuto dal ligando, la sua carica è in parte schermata e l'intero complesso diventa più lipofilo, permettendogli di penetrare nelle membrane microbiche e disturbare enzimi vitali. In un semplice test di infiammazione basato sulla denaturazione di una proteina d'uovo danneggiata dal calore, i nuovi complessi hanno anche ridotto la denaturazione proteica più efficacemente dello stesso ibuprofene, suggerendo che potrebbero calmare processi infiammatori a dosi inferiori.
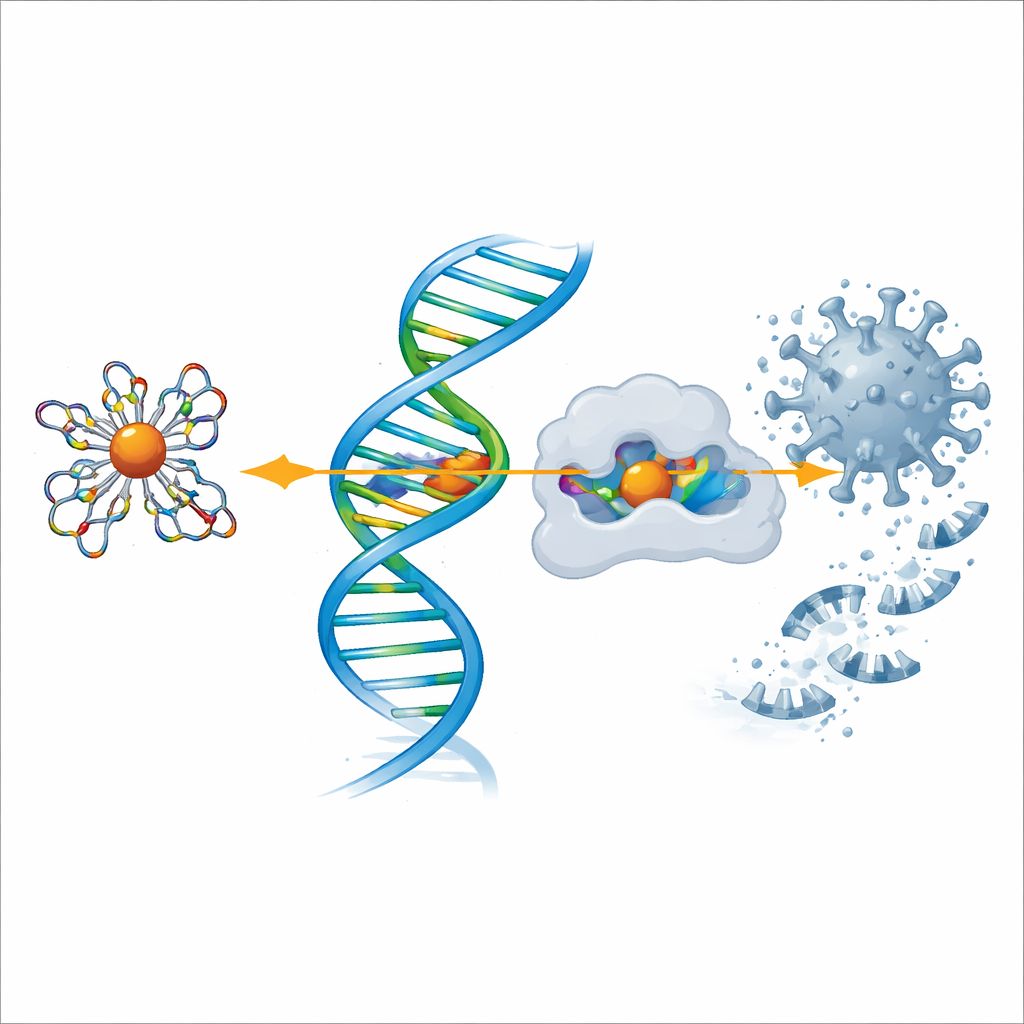
Esplorare l'azione contro le proteine del COVID‑19 e gli enzimi del dolore
Per valutare il potenziale antivirale, il team ha usato modellizzazione computerizzata per far “dockare” il ligando e ciascun complesso metallico nelle forme tridimensionali di due proteine chiave: la proteasi principale del SARS‑CoV‑2, che il virus usa per tagliare i suoi poliproteine, e la cicloossigenasi‑2 (COX‑2), un enzima coinvolto nel dolore e nell'infiammazione. Le simulazioni hanno mostrato che i complessi, in particolare quelli di rame e zinco, si inseriscono perfettamente nelle tasche attive di queste proteine e formano molteplici interazioni stabilizzanti. Più è negativo il valore calcolato dell'energia di legame, più forte è il legame previsto, e anche qui il complesso di rame si è distinto, seguito da vicino da zinco e nichel, supportando i risultati sperimentali sull'attività antinfiammatoria e antimicrobica.
Cosa potrebbe significare per i farmaci futuri
Nel complesso, il lavoro dimostra che un comune farmaco da banco può essere trasformato in uno strumento chimico multiuso fondendolo con un partner organico accuratamente scelto e con l'ione metallico giusto. Tra i quattro metalli testati, il rame ha prodotto il candidato più promettente, con forti attività antibatteriche, antifungine, anticancro, antinfiammatorie e un'azione anti‑SARS‑CoV‑2 prevista dalla modellizzazione computazionale, mentre nichel e zinco hanno mostrato effetti leggermente più miti ma comunque notevoli. Sebbene questi risultati siano ancora a livello di laboratorio e di modello computazionale, indicano una strategia in cui farmaci di uso comune vengono “aggiornati” in complessi metallici mirati che potrebbero agire a dosi inferiori e su una gamma più ampia di malattie rispetto ai farmaci originali.
Citazione: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Parole chiave: derivati dell'ibuprofene, complessi metal‑farmaco, agenti anticancro, terapia antimicrobica, proteasi del COVID‑19