Clear Sky Science · it
Funzionalizzazione asimmetrica catalitica di esteri boronici di bicyclo[1.1.0]butano abilitata da migrazione 1,2 dell’ossigeno
Perché i minuscoli anelli quadrati contano
I chimici amano costruire nuovi farmaci e materiali assemblando piccoli pezzi molecolari, un po’ come con i mattoncini Lego. Gli anelli carboniosi a quattro membri chiamati ciclobutani sono particolarmente apprezzati perché concentrano molta energia e forma in uno spazio ridotto, il che può modificare il comportamento di un farmaco nell’organismo. Questo articolo descrive un nuovo modo per ottenere questi anelli in forma molto controllata, “a mano sola” (chirale), usando una reazione intelligente che costringe un gruppo contenente ossigeno a spostarsi da un atomo al successivo. Il lavoro apre la strada alla progettazione di molecole più complesse e precise per applicazioni farmaceutiche e materiali avanzati.
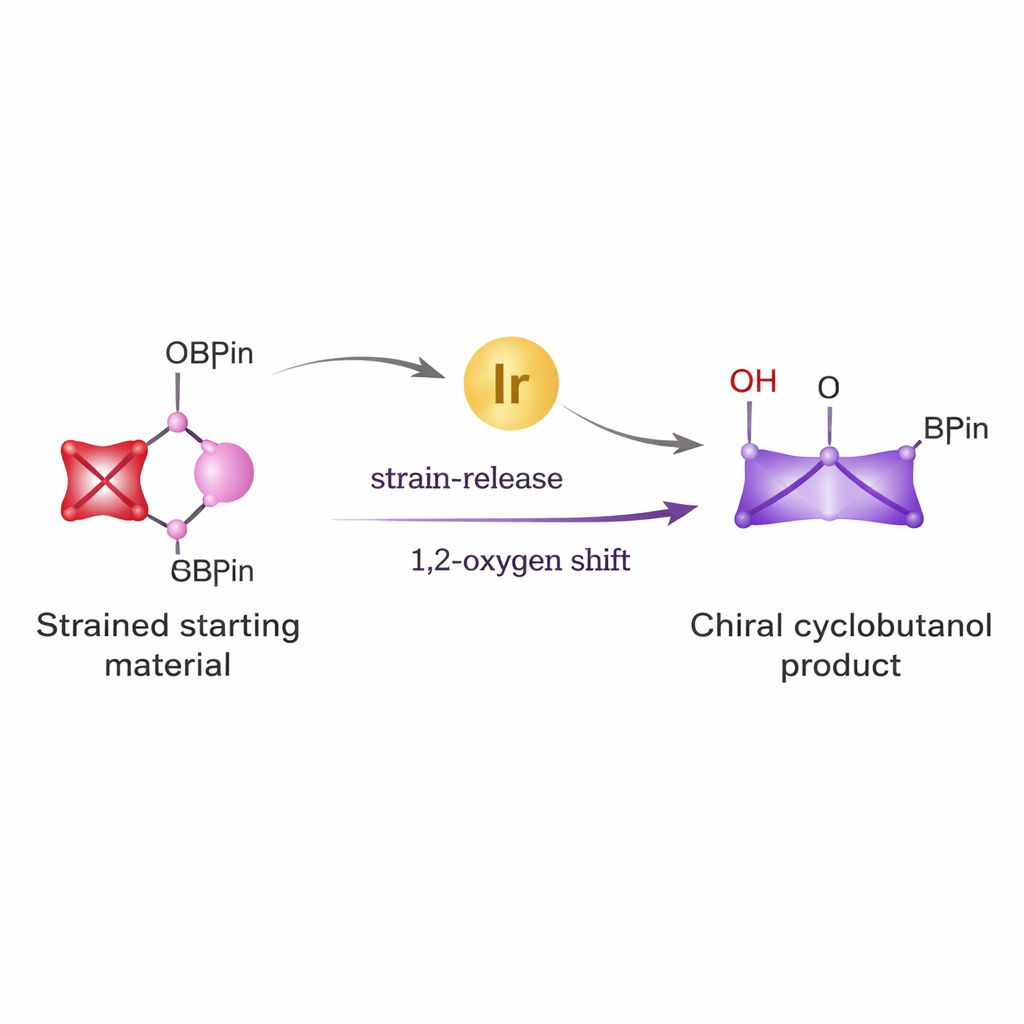
Dai blocchi di base a potenti anelli
I ciclobutani compaiono in vari agenti antivirali, candidati antitumorali e altre molecole bioattive. Tuttavia costruirli con l’esatta disposizione tridimensionale richiesta in campo medicinale è stato difficile. Le vie tradizionali spesso richiedono reagenti aggressivi e producono miscele di prodotti immagine speculare difficili da separare. Gli autori si sono posti l’obiettivo di risolvere questo problema combinando due idee potenti: la reattività insolita di un anello piccolissimo e altamente tensionato chiamato bicyclo[1.1.0]butano, e la versatilità degli esteri boronici, una famiglia ben nota di reagenti ampiamente usata nella chimica di cross‑coupling per formare legami carbonio–carbonio.
Trasformare un limite in una nuova via reattiva
Nelle reazioni di accoppiamento mediate da metalli, gli esteri boronici formano un complesso intermedio con un alchossido (una base a base di ossigeno). Questo complesso quasi sempre segue un percorso consolidato chiamato transmetallazione, che porta direttamente alla formazione di nuovi legami carbonio–carbonio o carbonio–alogeno. Quella via “di default” ha reso difficile esplorare altre possibilità, come lo spostamento dello stesso gruppo ossigeno. Il gruppo ha capito che partendo da un estere boronico di bicyclo[1.1.0]butano, la tensione intrinseca del piccolo anello poteva essere sfruttata per sovrascrivere il percorso usuale. Abbinando questo sistema teso a un catalizzatore a base di iridio e a un ligando chirale accuratamente scelto, hanno puntato a indurre la migrazione dell’ossigeno in modo controllato, mentre l’anello si apriva e si richiudeva in un ciclobutano.
Una danza graduale guidata dalla tensione
Gli esperimenti hanno confermato che la strategia funziona. Utilizzando alchossidi di litio preparati da una vasta gamma di alcoli — incluse zuccheri, terpeni, steroidi e semplici alcoli alifatici — gli autori hanno convertito esteri boronici di bicyclo[1.1.0]butano in prodotti ciclobutanoli cis con rese elevate e ottimo controllo della chiralità. Il catalizzatore a base di iridio forma inizialmente un complesso allelico reattivo a partire da un carbonato allelico. Questo complesso attacca quindi il sistema teso del bicyclo[1.1.0]butano, formando un nuovo legame carbonio–carbonio mentre il minuscolo anello si apre. Crucialmente, invece di seguire immediatamente la via usuale della transmetallazione, l’intermedio contenente boro subisce una sottile rotazione del legame carbonio–boro, allineando il gruppo ossigeno in modo che possa spostarsi agevolmente su un atomo di carbonio vicino. Questa migrazione 1,2 dell’ossigeno fissa l’arrangiamento cis desiderato sul nuovo anello ciclobutano.
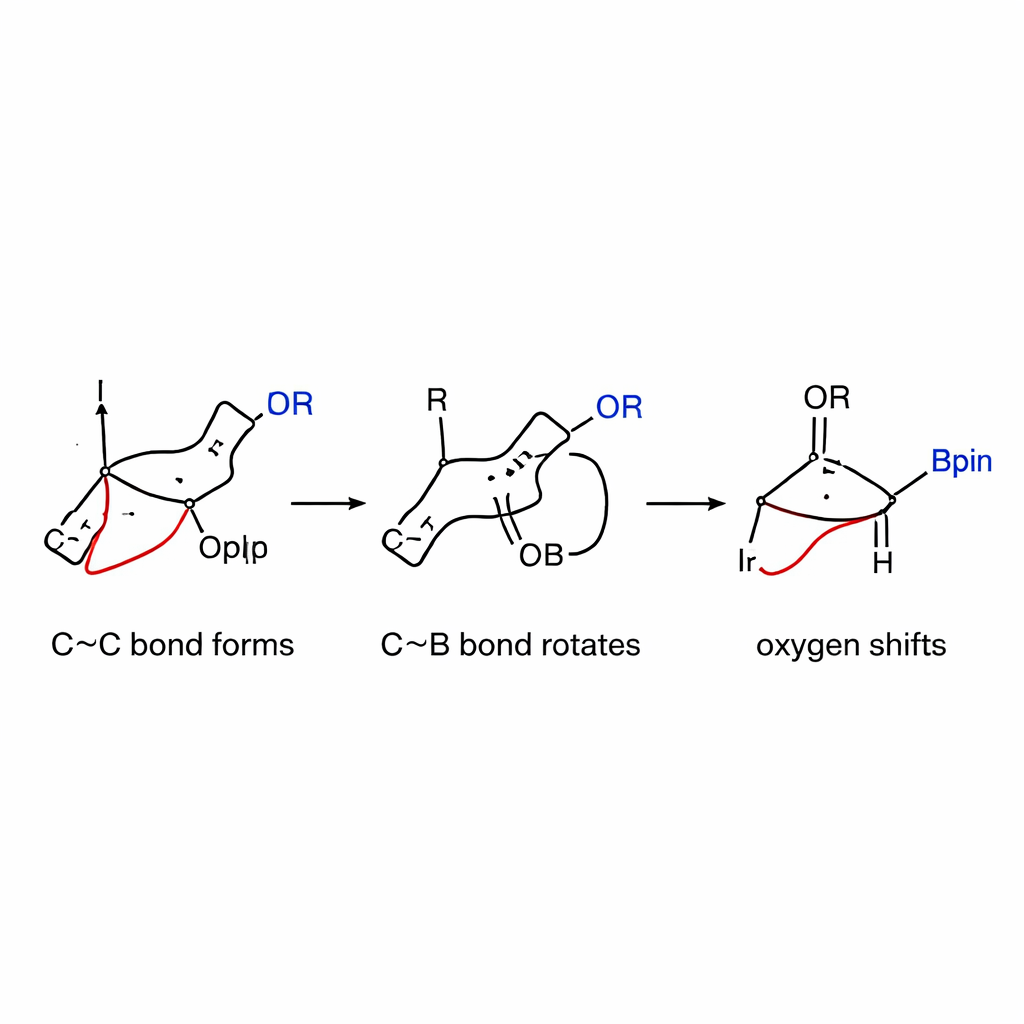
Uno sguardo sotto il cofano del meccanismo
Per capire perché la reazione è così selettiva, gli autori hanno combinato misure cinetiche con dettagliate simulazioni al calcolatore. Hanno scoperto che il passaggio lento e determinante della velocità è la formazione iniziale del legame carbonio–carbonio tra la specie iridio–allile e il complesso boronato teso, e non l’attivazione precedente del carbonato allelico. Test elettronici hanno mostrato che i partner allilici che stabilizzano carica positiva reagiscono più rapidamente, a sostegno di un meccanismo in cui si forma un intermedio parzialmente carico. I calcoli hanno inoltre rivelato che la rotazione attorno al legame carbonio–boro — prima ritenuta difficile — presenta una barriera energetica sorprendentemente bassa in questo sistema, grazie alla tensione immagazzinata nell’anello. Una volta che la rotazione ha allineato il gruppo ossigeno, lo spostamento 1,2 procede senza intoppi e preferenzialmente porta al prodotto cis piuttosto che alla forma trans più comune.
Nuovi strumenti per modellare i farmaci del futuro
Oltre a provare un punto meccanicistico, la reazione fornisce prodotti versatili. I ciclobutanoli mantengono un’unità di estere boronico, che può essere trasformata in molti altri gruppi funzionali tramite chimica consolidata. Gli autori hanno mostrato numerose modifiche in “fase tardiva”, come idrogenazione, ossidazione, metatesi di olefine e ulteriori accoppiamenti, preservando nel contempo la precisa forma tridimensionale dell’anello. In termini semplici, questo lavoro trasforma un percorso laterale un tempo problematico — la migrazione dell’ossigeno nei complessi boronati — in uno strumento sintetico potente. Sfruttando la tensione dell’anello e un catalizzatore a base di iridio finemente tarato, i ricercatori offrono ai chimici un modo affidabile per costruire ciclobutani chirali e complessi che potrebbero svolgere ruoli chiave nei farmaci di prossima generazione e nei materiali molecolari avanzati.
Citazione: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Parole chiave: ciclopentano, chimica degli organoborani, catalisi asimmetrica, bicyclobutano, migrazione dell’ossigeno