Clear Sky Science · it
I macrofagi CD19+ associati al tumore inducono un microambiente immunosoppressivo nel carcinoma epatocellulare
Perché i difensori del corpo a volte aiutano il cancro al fegato
Il cancro del fegato è tra i tumori più letali al mondo, in parte perché i tumori possono subvertire il sistema immunitario dell’organismo. Questo studio rivela un sorprendente sottogruppo di cellule immunitarie all’interno dei tumori epatici che, invece di combattere il cancro, lo aiutano attivamente a nascondersi e a proliferare. Capire chi sono queste cellule “traditrici” e come funzionano apre nuove strade per rendere l’immunoterapia più efficace per i pazienti con carcinoma epatocellulare, la forma più comune di cancro al fegato.
Un gruppo speciale di cellule immunitarie all’interno dei tumori
Gli autori si sono concentrati sui macrofagi associati al tumore, cellule immunitarie che normalmente inglobano germi e detriti ma che spesso vengono corrotte all’interno dei tumori. Analizzando campioni di tumore epatico provenienti da numerosi pazienti, hanno identificato un sottogruppo distinto di macrofagi che esprimono una molecola di superficie chiamata CD19, solitamente presente sulle cellule B e non sui macrofagi. Questi macrofagi CD19-positivi erano molto più abbondanti nei tumori del fegato rispetto al tessuto epatico sano circostante o al sangue, e risultavano arricchiti anche in diversi altri tumori solidi. Analisi a singola cellula hanno confermato che si tratta di veri macrofagi con un profilo genico e proteico unico, non di cellule B erroneamente identificate.
Come queste cellule modellano un quartiere favorevole al tumore
I pazienti i cui tumori contenevano molti macrofagi CD19-positivi tendevano ad avere tumori più grandi, più aggressivi e una sopravvivenza più breve. I campioni tumorali ricchi di queste cellule mostravano meno cellule CD8 T citotossiche e più cellule T regolatorie, un quadro tipico di un ambiente altamente immunosoppressivo. In modelli murini, l’aggiunta di macrofagi CD19-positivi a cellule di carcinoma epatico ha accelerato la crescita tumorale e ridotto la presenza di T cell utili, aumentando nel contempo altri tipi di cellule mieloidi soppressive. Importante, quando i ricercatori hanno impiegato cellule T ingegnerizzate che riconoscono CD19 per eliminare selettivamente questi macrofagi, i tumori epatici si sono ridotti anche in topi privi di normali cellule B, individuando così i macrofagi stessi come bersagli terapeutici.
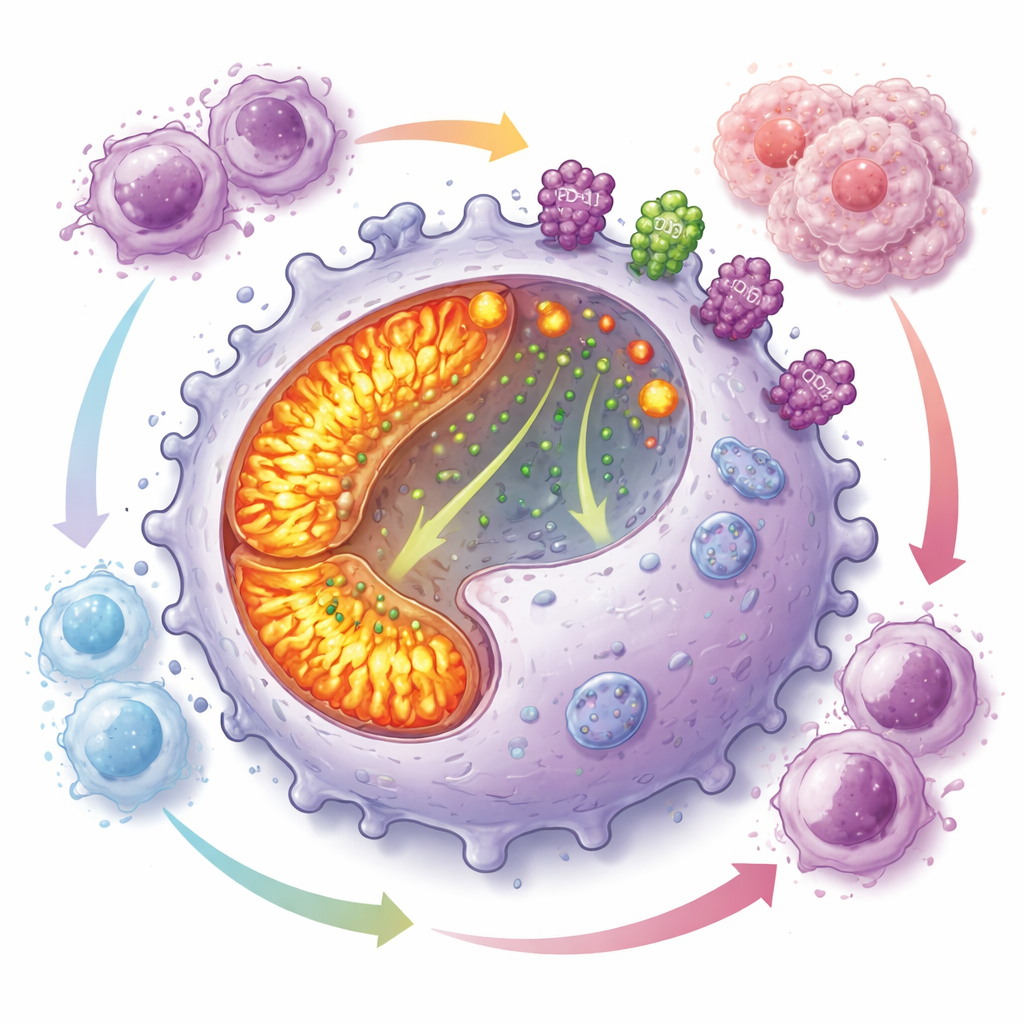
Un programma affamato di energia che smorza l’attacco immunitario
Approfondendo, il gruppo ha scoperto che i macrofagi CD19-positivi mantengono i loro “impianti di energia” interni a pieno regime. I loro mitocondri, gli organelli che generano energia, erano più numerosi e più attivi rispetto ad altri macrofagi, con un aumento della fosforilazione ossidativa e delle specie reattive dell’ossigeno. Nonostante questo stato energetico, queste cellule mostravano scarsa capacità di fagocitare bersagli ma si dividevano rapidamente, favorendo la loro accumulazione nei tumori. Allo stesso tempo, esibivano alti livelli di PD-L1 e CD73 sulla superficie — due molecole note per inibire le risposte delle cellule T e per generare adenosina, un mediatore che sopprime potentemente l’immunità. Esperimenti in co-coltura hanno mostrato che questi macrofagi inibiscono fortemente la proliferazione di diversi tipi di cellule T.
Il interruttore maestro dietro i macrofagi traditori
I ricercatori hanno identificato un fattore di trascrizione chiamato PAX5 come il motore centrale di questo programma macrofagico dannoso. PAX5 è noto soprattutto per guidare lo sviluppo delle cellule B, ma qui risultava molto attivo nei macrofagi CD19-positivi. Forzare l’espressione di PAX5 in cellule di tipo macrofagico ha aumentato la biogenesi mitocondriale, la produzione di energia e i livelli proteici — ma non di mRNA — di PD-L1, CD73 e CD19. Esperimenti meccanicistici hanno dimostrato che PAX5 favorisce l’ingresso di calcio nei mitocondri, abbassando il calcio nel citosol e impedendo a un regolatore chiave chiamato TFEB di entrare nel nucleo. Con TFEB bloccato, la produzione e la funzione dei lisosomi diminuiscono, quindi proteine come PD-L1 e CD73 non vengono più degradate efficacemente e si accumulano sulla superficie cellulare, intensificando la soppressione immunitaria.
Trasformare la scoperta in migliori opzioni terapeutiche
Poiché questi macrofagi dipendono fortemente dall’attività di CD73 e dal metabolismo mitocondriale, gli autori hanno testato se bloccare queste vie potesse migliorare l’efficacia dell’immunoterapia. Nel carcinoma epatocellulare murino, la combinazione del blocco di PD-L1 con anticorpi contro CD73 o con un inibitore di CD73 ha portato a tumori più piccoli, a un maggior infiltrato di cellule T e a una minore proliferazione delle cellule tumorali. Allo stesso modo, associare anticorpi anti–PD-L1 con un inibitore della fosforilazione ossidativa mitocondriale ha migliorato il controllo del tumore e favorito l’ingresso delle cellule immunitarie nel tumore. Colpisce che questi benefici scomparissero in topi i cui macrofagi erano privi di PAX5, confermando che gli effetti farmacologici erano legati alla disattivazione del programma macrofagico CD19-positivo guidato da PAX5. Nel complesso, il lavoro suggerisce che mirare selettivamente a questo sottogruppo di macrofagi — tramite terapie cellulari dirette contro CD19, inibizione di CD73 o farmaci metabolici — potrebbe aiutare a trasformare un tumore epatico immunologicamente “freddo” in uno più reattivo agli attuali trattamenti con inibitori dei checkpoint.
Citazione: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Parole chiave: carcinoma epatocellulare, macrofagi associati al tumore, immunoterapia, PD-L1 e CD73, metabolismo mitocondriale