Clear Sky Science · it
L'espressione tumorale specifica di HORMAD1 altera l'arresto mitotico e aumenta la sensibilità agli inibitori delle chinasi mitotiche
Perché è importante per il trattamento del cancro
Quando le nostre cellule si dividono, fanno affidamento su complessi controlli di sicurezza per trasmettere il corretto corredo cromosomico. Il cancro spesso dirotta o indebolisce questi meccanismi di salvaguardia, provocando genomi caotici che sia guidano la malattia sia modellano la risposta dei tumori ai farmaci. Questo studio rivela come una proteina insolita chiamata HORMAD1, normalmente attiva solo nelle cellule riproduttive, venga riattivata in molti tumori mammari aggressivi e in altri tipi tumorali. Sabotando in modo sottile un checkpoint chiave della divisione cellulare, HORMAD1 rende le cellule cancerose più instabili—ma anche sorprendentemente vulnerabili a una nuova classe di farmaci sperimentali.
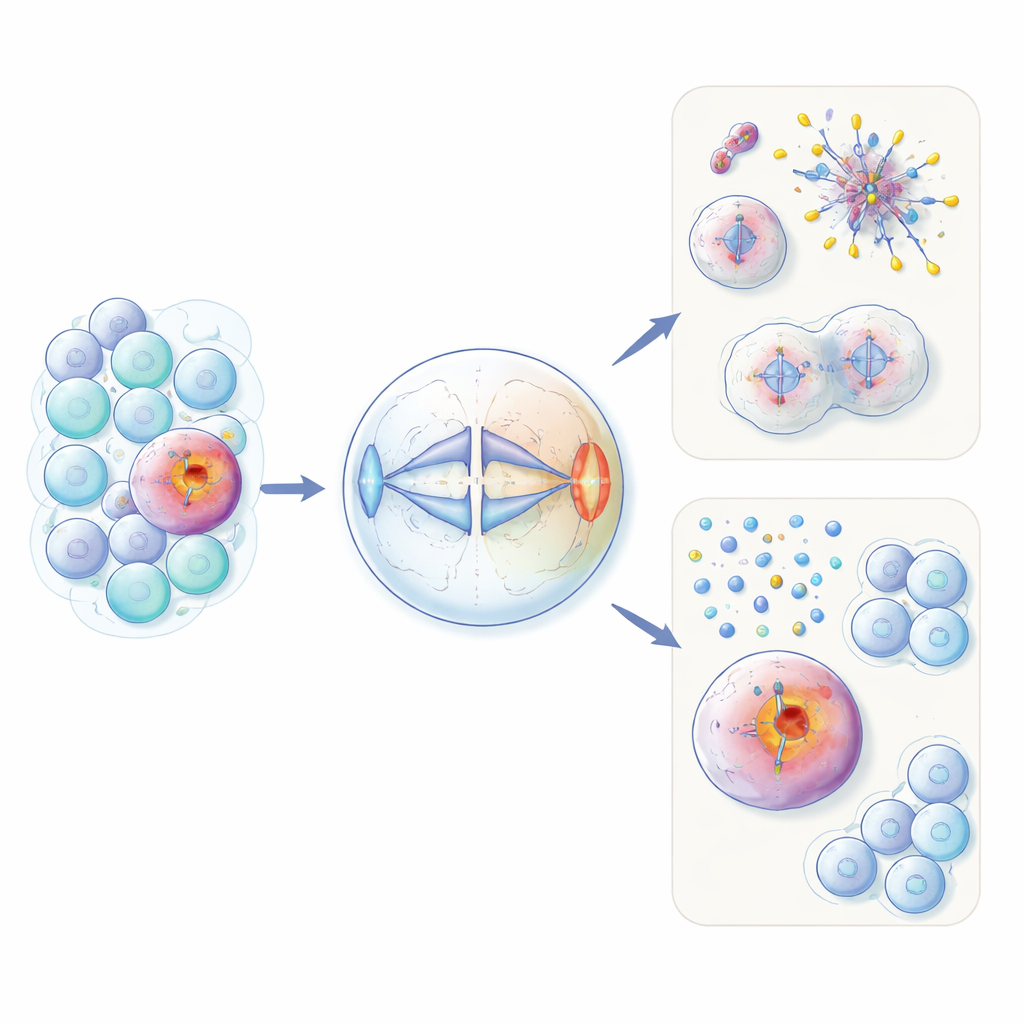
Una proteina della fertilità fuori posto nelle cellule tumorali
HORMAD1 è normalmente espressa solo nelle cellule germinali, dove si formano ovuli e spermatozoi. Lì aiuta a gestire il rimodellamento del DNA e il controllo di qualità durante la meiosi, il tipo speciale di divisione cellulare. Gli autori mostrano che in circa il 60% dei carcinomi mammari triplo negativi—e in sottogruppi di altri tumori—questa proteina viene riaccesa in modo inappropriato. Usando sia cellule non cancerose ingegnerizzate sia linee cellulari tumorali, hanno riscontrato che un eccesso di HORMAD1 altera la separazione uniforme dei cromosomi durante la mitosi ordinaria. Le cellule che esprimono HORMAD1 sviluppano più cromosomi in ritardo, aneuploidia (cromosomi in eccesso o mancanti) e piccole "micronuclei" contenenti DNA, tutti segni distintivi del caos genomico osservato nei tumori aggressivi.
Come funzionano normalmente i controlli sulla divisione cellulare
Per dividersi correttamente, una cellula assembla un fuso di microtubuli che si attaccano a ogni cromosoma. Un sistema di sorveglianza noto come checkpoint dell'assemblaggio del fuso funziona come un freno sensibile alla tensione: se qualche cromosoma non è collegato correttamente, il freno blocca la progressione, impedendo la separazione finché gli errori non vengono corretti. Diverse chinasi mitotiche, tra cui MPS1, Aurora B e BUB1, aiutano a rilevare gli attacchi errati e promuovono la “correzione degli errori” in modo che ogni cellula figlia riceva il giusto set di cromosomi. La compromissione di questo sistema può sia favorire lo sviluppo del cancro sia creare vulnerabilità specifiche sfruttabili con alcuni farmaci.
HORMAD1 indebolisce silenziosamente il freno
I ricercatori hanno scoperto che HORMAD1 mina questo freno di sicurezza in modo sottile ma significativo. Piuttosto che interferire con componenti classici del checkpoint come la proteina HORMA MAD2L1, HORMAD1 si lega direttamente alla chinasi Aurora B. Aurora B normalmente collabora con un'altra proteina, INCENP, per diventare pienamente attiva e fosforilare bersagli nei centromeri e nei cinetocori—siti critici sui cromosomi dove si attaccano le fibre del fuso. Quando HORMAD1 è presente nelle cellule tumorali in divisione, compete con INCENP per l'accesso ad Aurora B, riducendo la loro interazione e attenuando l'attività di Aurora B. Di conseguenza, i segnali di fosforilazione mediati da Aurora B su vari bersagli si indeboliscono, la correzione degli errori è meno efficace e il checkpoint diventa “perdente”: le cellule escono dalla mitosi troppo presto, anche quando gli attacchi sono difettosi, portando a una cattiva segregazione dei cromosomi e all'instabilità genomica.
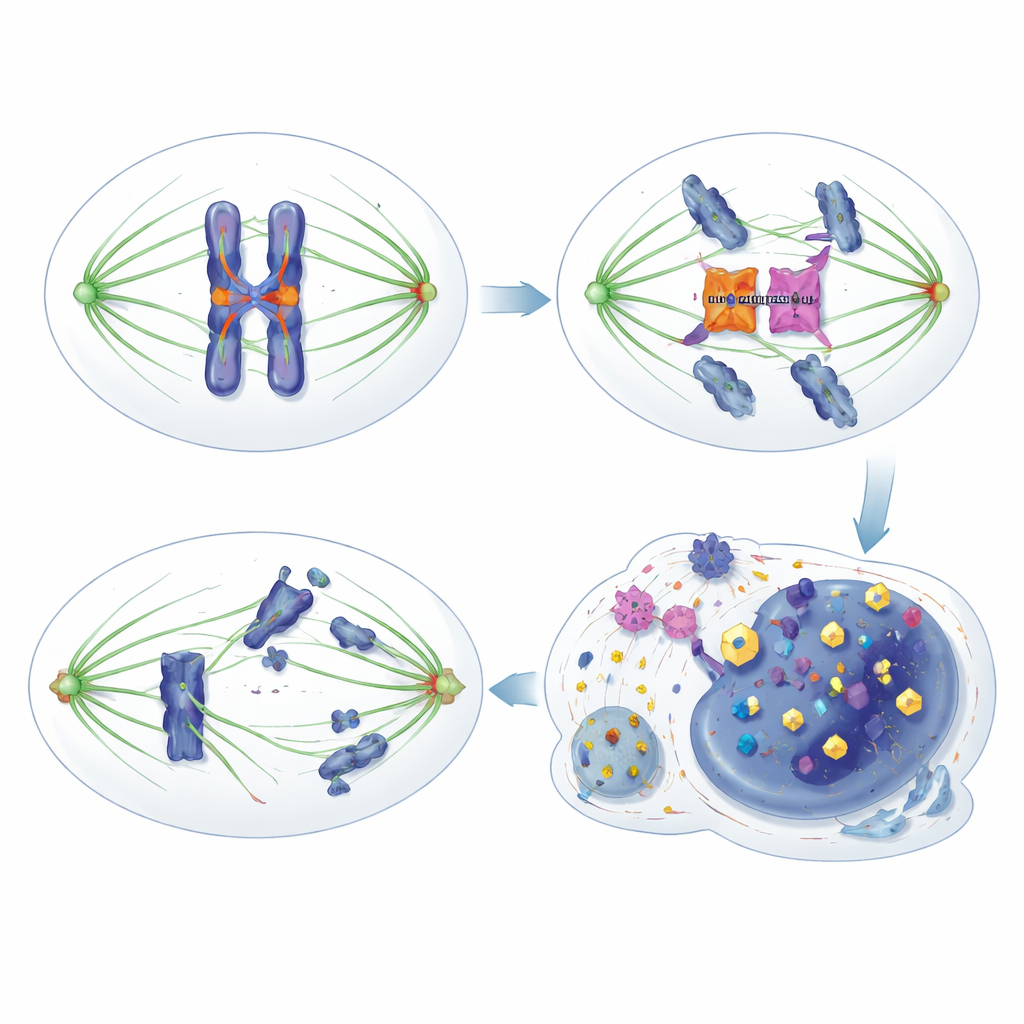
Dalla debolezza all'opportunità terapeutica
Poiché HORMAD1 disattiva solo parzialmente Aurora B e le altre salvaguardie correlate, le cellule tumorali restano appena sufficientemente vitali per proliferare, ma dipendono fortemente dalla funzione residua delle chinasi mitotiche per sopravvivere a divisioni difettose ripetute. Il gruppo ha verificato questo esponendo cellule positive e negative per HORMAD1 a inibitori sperimentali di MPS1, Aurora B e BUB1. In diversi modelli, l'espressione di HORMAD1 ha reso le cellule molto più sensibili a questi farmaci, riducendone drasticamente la capacità di proliferare o formare colonie. L'abbassamento genetico di BUB1 è risultato particolarmente letale solo in presenza di HORMAD1, rivelando una dipendenza selettiva e marcata. In modelli murini con tumori mammari triplo negativi derivati da pazienti, quelli con livelli elevati di HORMAD1 si sono ridotti o sono cresciuti più lentamente quando trattati con una formulazione nanoparticellare di un inibitore di Aurora B, mentre i tumori privi di HORMAD1 hanno in gran parte resistito allo stesso trattamento.
Cosa significa per i pazienti
Per un osservatore non specialista, HORMAD1 agisce come una lama a doppio taglio nel cancro: spinge le cellule tumorali verso un maggior disordine cromosomico, che può alimentare la malattia, ma rendendole allo stesso tempo precariamente dipendenti da poche salvaguardie residue della divisione cellulare. Lo studio mostra che questa proteina della fertilità fuori luogo indebolisce un checkpoint chiave deviando Aurora B, lasciando i tumori HORMAD1-positivi particolarmente vulnerabili a farmaci che mirano ad Aurora B, MPS1 o BUB1. Poiché HORMAD1 è in gran parte assente nei tessuti normali ma presente in un chiaro sottogruppo di tumori, potrebbe fungere da biomarcatore per identificare i pazienti più propensi a beneficiare di questi emergenti inibitori delle chinasi mitotiche, aprendo potenzialmente nuove vie di trattamento mirato per tumori difficili da curare come il carcinoma mammario triplo negativo.
Citazione: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Parole chiave: HORMAD1, carcinoma mammario triplo negativo, instabilità cromosomica, chinasi Aurora B, inibitori del checkpoint mitotico