Clear Sky Science · it
Polimeri proteomimetici eterobifunzionali per la degradazione mirata di MYC e KRAS
Nuovi strumenti per abbattere le proteine più ostinate del cancro
Molte delle proteine più pericolose che guidano il cancro, come MYC e KRAS, sono state a lungo definite «non farmacabili» perché i farmaci faticano ad aggrapparsi a esse. Questo studio svela un nuovo tipo di materiale sintetico morbido — chiamato polimeri HYDRAC — che può afferrare queste proteine scivolose e indirizzarle al sistema di smaltimento cellulare. Per il lettore, il lavoro offre uno sguardo su come chimica e nanotecnologia potrebbero aprire opzioni terapeutiche per tumori che hanno resistito ai farmaci tradizionali.
Uno scheletro flessibile invece di una singola pillola
La maggior parte dei farmaci oncologici mirati sono piccole molecole che si inseriscono in tasche sulla superficie di una proteina, come una chiave nella serratura. Ma proteine come MYC sono flessibili e prive di buone tasche, mentre KRAS muta spesso in modi che neutralizzano i farmaci classici. Gli autori hanno quindi progettato lunghe catene polimeriche costruite da unità ripetute. Lungo queste catene hanno fissato due tipi di componenti: brevi segmenti leganti la proteina che riconoscono un bersaglio come MYC o RAS, e segmenti «degron» che richiamano il macchinario cellulare di smaltimento. Poiché molte copie di ciascun componente decorano la stessa catena, una singola molecola HYDRAC può raggiungere più proteine ed enzimi contemporaneamente, qualcosa di difficile da ottenere con una singola molecola farmaco rigida.
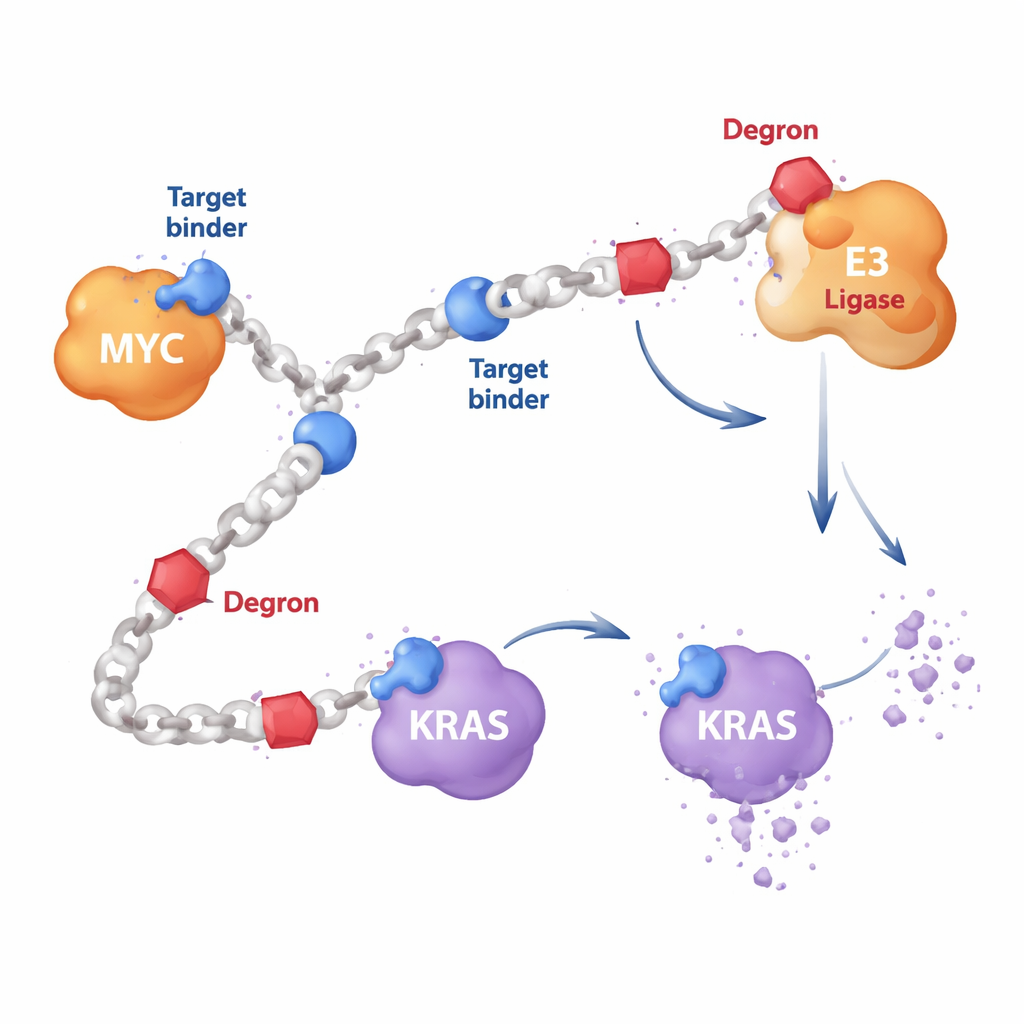
Insegnare alle cellule a sbriciolare MYC
Come primo test, i ricercatori si sono concentrati su MYC, un interruttore maestro che guida la crescita in molti tumori ma che ha resistito a un attacco diretto per decenni. Hanno costruito polimeri HYDRAC che esponevano un noto peptide legante MYC insieme a un semplice motivo degron che segnala le proteine per la distruzione da parte del proteasoma cellulare, il principale trituratore di proteine. In esperimenti in vitro questi polimeri si sono ripiegati in forme compatte, simili a proteine, e si sono legati saldamente a MYC ma non a proteine non correlate. Nelle cellule tumorali, gli HYDRAC sono entrati con facilità, hanno perturbato i programmi genici controllati da MYC e hanno innescato la morte cellulare — effetti che dipendevano dalla presenza di entrambi i componenti di targeting e degron sulla stessa catena polimerica.
Dalla coltura cellulare alla riduzione dei tumori
All’interno delle cellule, il trattamento con HYDRAC ha causato un calo netto dei livelli di proteina MYC senza ridurre l’RNA di MYC, indicando una vera distruzione anziché un semplice spegnimento. Il blocco del proteasoma o di enzimi chiave che attivano alcune vie di degradazione ha ripristinato i livelli di MYC, dimostrando che i polimeri agiscono reindirizzando i sistemi di smaltimento cellulare. Analisi su scala proteomica hanno rivelato che pochissime altre proteine erano colpite, suggerendo una selettività notevole. In modelli murini di tumori guidati da MYC, gli HYDRAC marcati con fluoroforo si sono accumulati preferenzialmente nei tumori dopo l’iniezione e sono rimasti lì per giorni. Dosi ripetute hanno rallentato la crescita tumorale senza perdita di peso significativa o danni tissutali evidenti, e i campioni tumorali mostravano meno cellule in divisione e più segni di morte cellulare programmata.
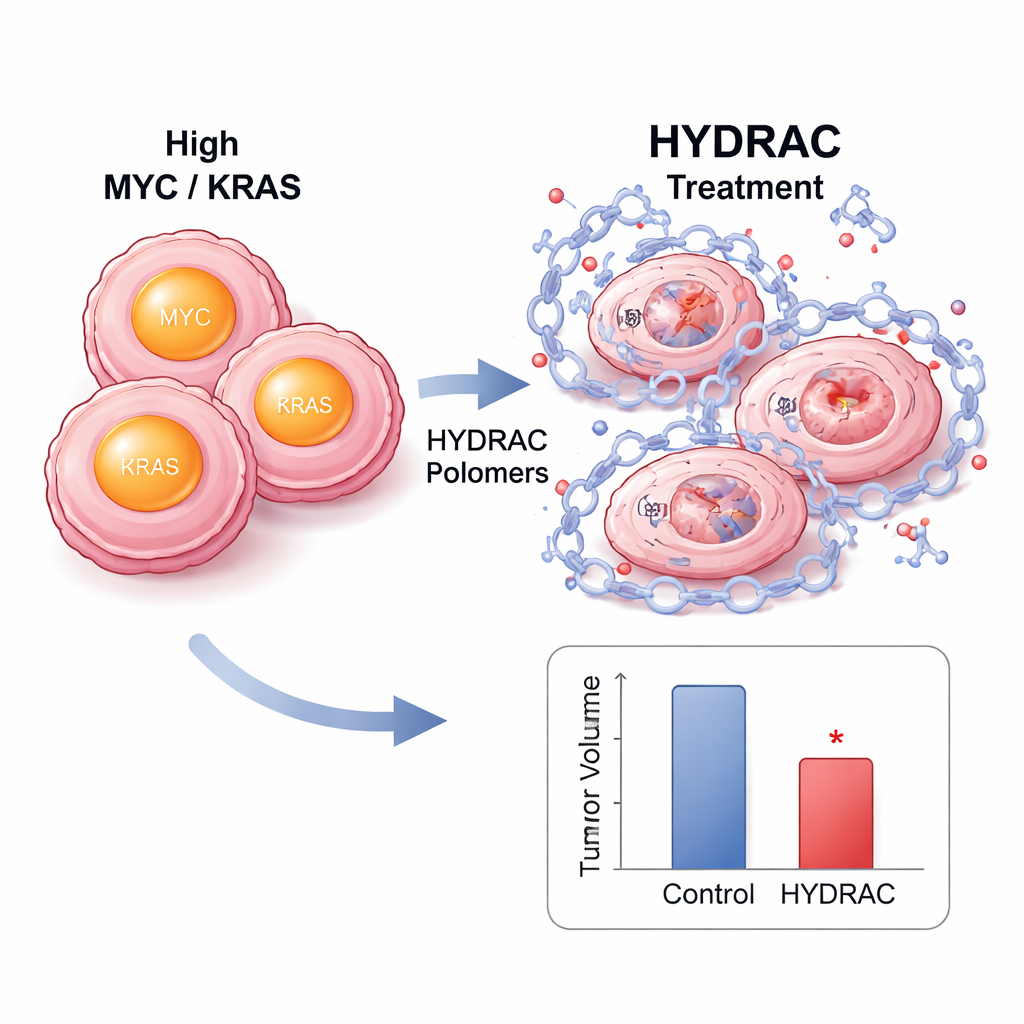
Una piattaforma plug-and-play per molti bersagli patologici
Uno dei punti di forza dell’approccio HYDRAC è che i gruppi laterali possono essere scambiati come parti intercambiabili. Il team ha sostituito il degron originale con altri elementi reclutanti che richiamano diversi enzimi cellulari, inclusi quelli che riconoscono il farmaco talidomide. Ogni versione degradava MYC solo quando l’enzima previsto era presente e funzionale, confermando che i polimeri possono essere sintonizzati per usare rotte cellulari distinte. Per testare la generalità, i ricercatori hanno poi costruito HYDRAC mirati a RAS usando un peptide che riconosce le proteine RAS. Questi costrutti hanno degradato con successo KRAS mutante in due diverse linee cellulari tumorali, suggerendo un potenziale «pan-KRAS» che non dipende da una singola mutazione — un passo importante per i tumori in cui coesistono molte varianti di KRAS.
Perché è importante per la cura del cancro futura
Questo lavoro introduce gli HYDRAC come una nuova classe di materiali programmabili che non si limitano a bloccare le proteine problematiche, ma aiutano le cellule a cancellarle. Combinando numerose unità di targeting e degradazione su un polimero flessibile, gli HYDRAC aggirano i limiti di progettazione dei tradizionali farmaci a piccola molecola e dei PROTAC, che tipicamente possono portare solo una singola unità di ciascun tipo. Pur restando molto da fare prima che questi materiali raggiungano la clinica, i risultati nei modelli guidati da MYC e KRAS suggeriscono che proteine tumorali a lungo considerate «non farmacabili» potrebbero, in realtà, essere vulnerabili quando la medicina somiglia più a una spazzola molecolare su misura che a una singola piccola pillola.
Citazione: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Parole chiave: degradazione proteica mirata, MYC, KRAS, terapici polimerici, nanomedicina oncologica