Clear Sky Science · it
Paesaggio epigenomico integrativo dei cervelli con malattia di Alzheimer rivela perturbazioni molecolari negli oligodendrociti correlate con la proteina tau
Perché questa ricerca sul cervello è importante
La malattia di Alzheimer è più nota per la perdita di memoria e l’accumulo nel cervello di due proteine problematiche: amiloide e tau. Tuttavia le persone con Alzheimer possono mostrare schemi di danno molto diversi, anche condividendo la stessa diagnosi. Questo studio pone una domanda fondamentale: quali interruttori all’interno delle cellule cerebrali aiutano a determinare quanto si accumulano queste proteine dannose e come colpiscono tipi cellulari diversi? Analizzando i segni chimici sul DNA in centinaia di cervelli, i ricercatori scoprono un collegamento sorprendente tra la tau e le cellule che rendono possibile il funzionamento dei cablaggi del cervello.
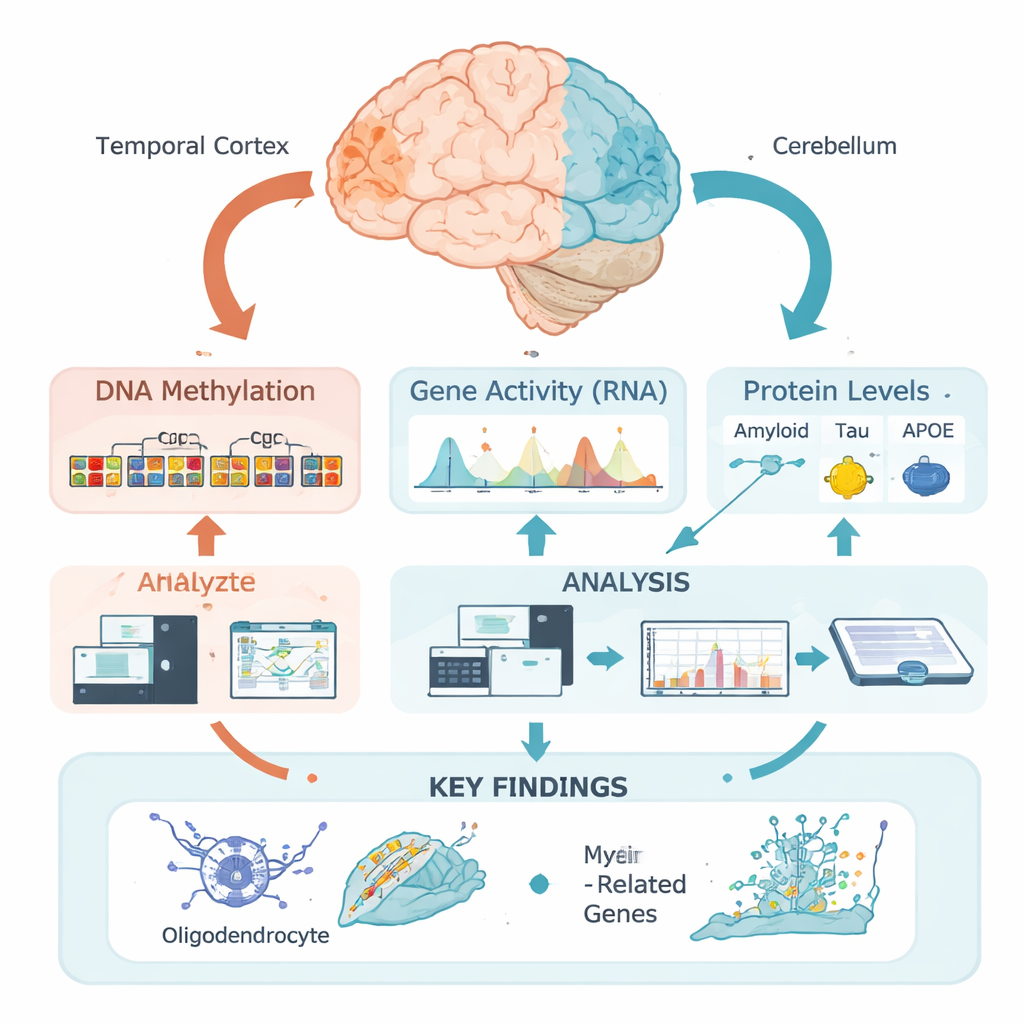
Segni chimici sul DNA come interruttori nascosti
Il nostro DNA porta le istruzioni di base per costruire e gestire le cellule cerebrali, ma queste istruzioni sono regolate da marchi epigenetici—segni chimici che possono aumentare o diminuire l’attività dei geni vicini senza alterare il codice genetico. Uno dei marchi più importanti è la metilazione del DNA, in cui piccoli gruppi chimici si legano a siti specifici del DNA. Invece di esaminare singoli siti isolati, questo gruppo ha usato un nuovo approccio “regionale”: ha raggruppato molti siti vicini in zone funzionali basate su come il DNA è impacchettato nella corteccia temporale, una regione fortemente colpita nell’Alzheimer, e nel cervelletto, relativamente risparmiato. Ciò ha permesso loro di chiedersi dove, in senso biologico, i modelli di metilazione cambiano in relazione alle caratteristiche della malattia.
Collegare i marchi del DNA alle proteine dell’Alzheimer
I ricercatori hanno analizzato tessuto cerebrale di 472 persone con Alzheimer confermato post mortem. Per ciascun campione di corteccia temporale, hanno misurato livelli dettagliati di amiloide, tau e proteine APOE in diverse forme biochimiche, oltre ai punteggi microscopici classici di placche amiloidi e grovigli tau. Hanno poi eseguito studi di associazione sull’intero epigenoma, testando se i livelli regionali di metilazione del DNA fossero correlati con queste misurazioni. In modo sorprendente, quasi tutte le forti associazioni trovate erano legate non all’amiloide, ma alla tau—in particolare alla tau totale solubile e a una forma fosforilata legata alla membrana (chimicamente modificata) ritenuta particolarmente tossica.
Un segnale forte nelle cellule del cablaggio cerebrale
Molte delle regioni di DNA collegate alla tau si trovavano in parti “attive” del genoma che influenzano i geni vicini. Combinando i dati di metilazione con le misurazioni dell’attività genica negli stessi cervelli, il gruppo ha mostrato che queste regioni spesso regolano geni usati dagli oligodendrociti—le cellule che avvolgono le fibre nervose con la mielina, permettendo ai segnali elettrici di viaggiare in modo rapido e affidabile. Gen importanti per la mielina come MBP, MAG e MYRF, insieme al gene di rischio per l’Alzheimer BIN1 e a un nuovo gene candidato chiamato LDB3, comparivano in questo insieme. Livelli più elevati della forma fosforilata tossica della tau tendevano a coincidere con maggiore metilazione in queste regioni e con una minore espressione dei geni associati agli oligodendrociti e alla mielina, mentre la frazione più benigna della tau totale solubile mostrava il pattern opposto.
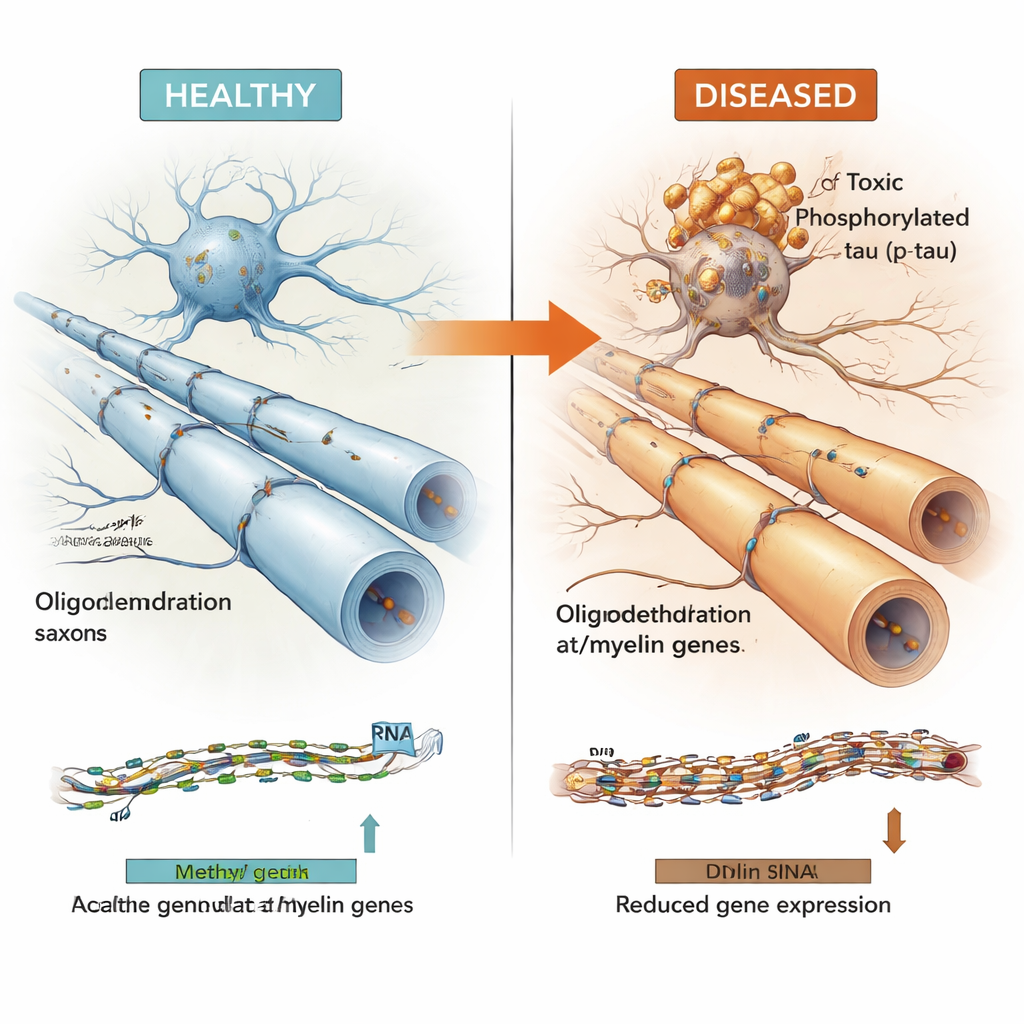
Un motivo osservato in diverse malattie cerebrali
Per verificare se questi risultati fossero robusti e generali, gli autori hanno esaminato grandi dataset indipendenti provenienti da altre collezioni di cervelli con Alzheimer e da cervelli colpiti da tauopatie primarie come la paralisi sopranucleare progressiva e la malattia di Pick. Anche se queste coorti sono state misurate con tecnologie diverse e spesso in regioni cerebrali differenti, molte delle stesse regioni di DNA e geni degli oligodendrociti mostravano un comportamento coerente: i loro livelli di metilazione erano correlati all’onere di grovigli tau e la loro espressione risultava ridotta nei cervelli malati e negli studi a singola cellula focalizzati specificamente sugli oligodendrociti. È importante notare che questi schemi non sembravano spiegabili semplicemente dalla genetica o dalla perdita complessiva di cellule, suggerendo un vero cambiamento epigenetico nella funzionalità degli oligodendrociti.
Cosa significa per la comprensione dell’Alzheimer
Nel complesso, i risultati supportano un modello in cui l’aumento dei livelli di tau dannosa è strettamente legato a cambiamenti epigenetici negli oligodendrociti che attenuano i geni legati alla mielina, indebolendo potenzialmente i cablaggi del cervello e contribuendo al declino cognitivo. Non è ancora chiaro cosa avvenga per primo—l’accumulo di tau o la perturbazione di questi geni della mielina—ma le associazioni strette e ripetute su migliaia di campioni e diverse malattie indicano un meccanismo condiviso. Mappando questi interruttori del DNA e integrandoli in un “Atlante Multiomico” pubblico, questo lavoro mette in luce gli oligodendrociti e la loro regolazione epigenetica come bersagli promettenti per future terapie mirate a stabilizzare i circuiti cerebrali, invece di concentrarsi esclusivamente sui neuroni o sulle placche amiloidi.
Citazione: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Parole chiave: malattia di Alzheimer, proteina tau, metilazione del DNA, oligodendrociti, mielina