Clear Sky Science · it
Basi strutturali della segnalazione e della modulazione del canale umano attivato dallo zinco (ZAC)
Come un metallo in tracce aiuta le cellule nervose a comunicare
Lo zinco è più noto come nutriente nelle compresse multivitaminiche, ma nell’organismo questo metallo agisce anche come un messaggero chimico rapido nel cervello. Lo studio descritto qui svela, a risoluzione atomica, come una proteina poco conosciuta chiamata canale attivato dallo zinco (ZAC) rilevi lo zinco all’esterno delle cellule e trasformi quel segnale in una risposta elettrica. Capire questo speciale varco nella membrana cellulare può chiarire come lo zinco modella l’attività cerebrale e suggerire nuovi modi per modulare i segnali nervosi in salute e malattia.
Un varco speciale per i segnali dello zinco
Molti messaggi rapidi tra le cellule nervose sono trasportati da molecole comuni come la serotonina o l’acetilcolina, che aprono canali ad anello nella membrana cellulare. ZAC è una parente distante di questi recettori, ma invece di rispondere a una molecola organica viene attivata da ioni metallici come zinco, rame e protoni. ZAC è presente in molti tessuti umani, incluso il cervello, ma è assente nei comuni animali da laboratorio come topo e ratto, il che ha rallentato i progressi. Questo lavoro usa la crio‑microscopia elettronica ad alta risoluzione per catturare diversi istantanei tridimensionali di ZAC umano: nella sua forma di riposo, con lo zinco legato e con due farmaci diversi che inattivano il canale. Insieme, queste strutture rivelano come lo zinco si ancora in cima al canale, come gli ioni lo attraversano e come gli inibitori serrano il varco o lo bloccano in uno stato non conduttivo.
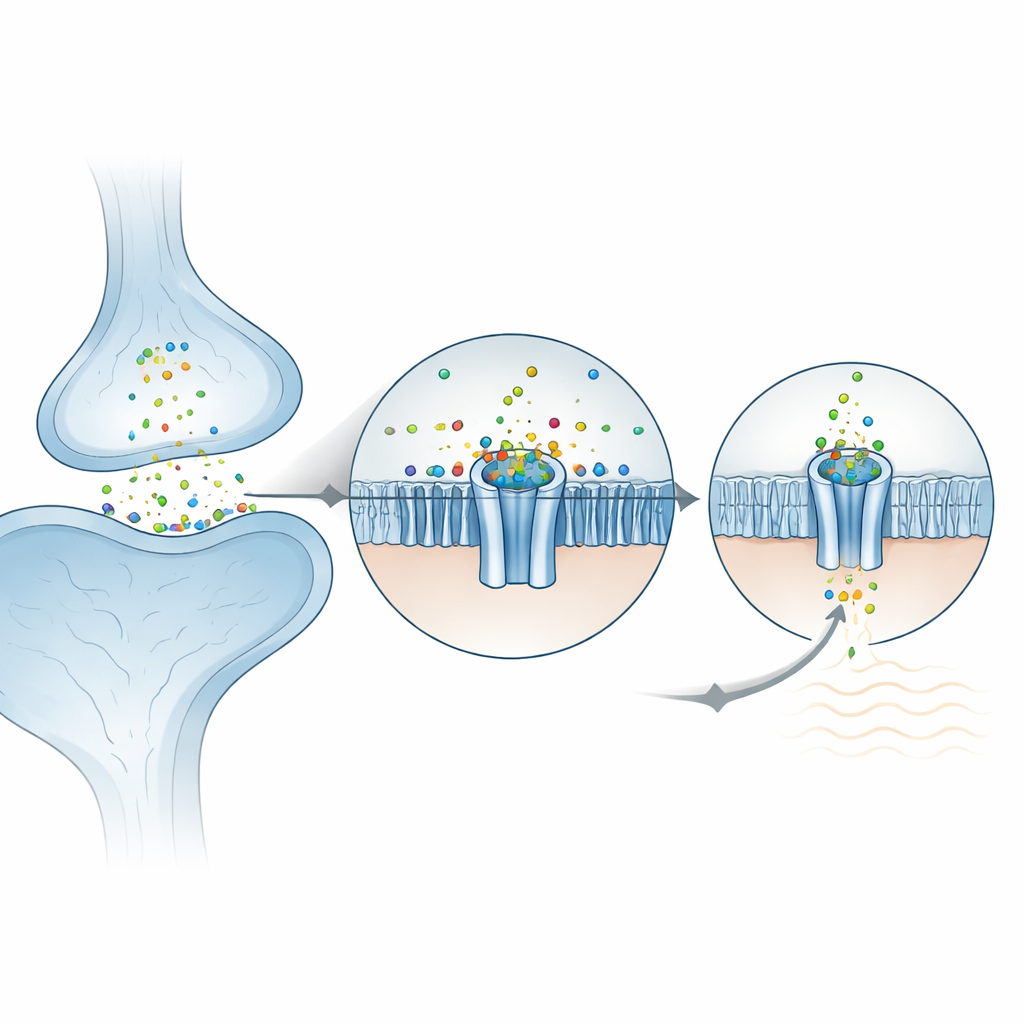
Come lo zinco si incastra nel canale
sulla superficie esterna della cellula, ZAC è formata da cinque subunità identiche che costituiscono una rosetta. I ricercatori hanno scoperto che ioni di zinco si sistemano in cinque tasche equivalenti, ciascuna situata tra due subunità vicine nel dominio esterno. Sorprendentemente, lo zinco non è trattenuto dagli usuali amminoacidi “afferra‑metallo” che comunemente legano i metalli (come istidina o cisteina). Invece, è cullato principalmente da due catene laterali aromatiche ad anello che stabilizzano l’ione carico positivamente tramite le cosiddette interazioni catione–π. Quando questi residui chiave sono stati mutati in cellule uovo di rana usate per registrazioni elettriche, il canale è diventato non reattivo allo zinco, confermando il loro ruolo centrale. L’ambiente circostante è già preorganizzato, il che aiuta a spiegare perché ZAC mostra una notevole attività spontanea anche senza zinco: la proteina si trova vicino al punto di equilibrio tra chiuso e aperto e lo zinco semplicemente sposta l’assetto.
Il percorso per gli ioni e una variante genetica comune
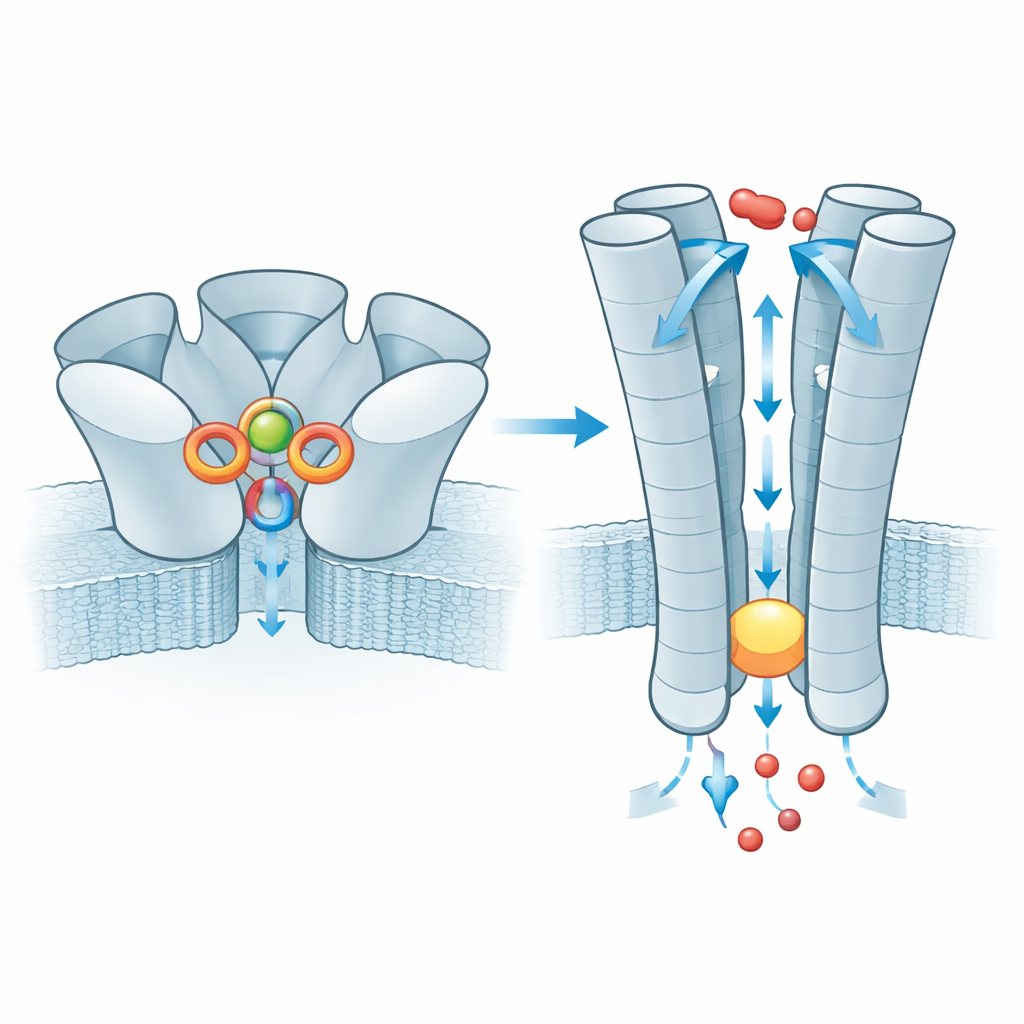
Una volta che lo zinco si è legato, l’effetto viene trasmesso alla parte transmembrana di ZAC, dove cinque eliche interne formano il poro. Nello stato di riposo questo tubo si restringe a livello di un anello di residui di leucina, creando un tappo idrofobico che blocca il movimento degli ioni. Con lo zinco legato, il tappo si allarga quel tanto che basta per permettere a piccoli ioni positivi come sodio e potassio di passare, mentre il rivestimento carico del poro contribuisce alla selettività per questi ioni. Il team ha anche studiato una variante umana molto comune di ZAC in cui un singolo amminoacido (treonina) è sostituito da alanina in un breve tratto sopra il tappo. Questo piccolo cambiamento indebolisce una rete di interazioni tra subunità vicine che normalmente aiuta a trasmettere il legame dello zinco al varco, e le misure elettriche mostrano che i canali costruiti con questa variante conducono correnti molto più piccole. La variante quindi agisce come convertitore di segnale meno efficiente, sebbene il suo impatto sulla fisiologia umana rimanga sconosciuto.
Come due farmaci silenziano il canale
Oltre allo zinco, lo studio esplora anche come due antagonisti, TTFB e d‑tubocurarina (d‑TC), inattivino ZAC. TTFB è una piccola molecola progettata ad hoc che si deposita profondamente nella regione della membrana, scivolando tra due delle eliche che formano il poro proprio sopra il varco. Lì interagisce con una tasca idrofobica aderente e con residui polari vicini, fungendo da supporto che impedisce alle eliche di muoversi verso uno stato completamente aperto e conduttivo. d‑TC, un farmaco più vecchio un tempo usato come miorilassante, agisce in modo più ampio. Una molecola di d‑TC si lega nella stessa tasca esterna che normalmente ospita lo zinco, imitando la carica positiva dello zinco ma impedendo al vero zinco di legarsi correttamente. Una seconda molecola di d‑TC si posiziona all’ingresso stesso del poro, ostruendo fisicamente il tunnel. Insieme, questi legami intrappolano ZAC in una conformazione desensibilizzata non conduttiva mentre la forma della proteina rimane relativamente aperta.
Cosa significano i risultati per lo zinco e la salute
Questo lavoro strutturale mostra in chiaro dettaglio molecolare che ZAC è un autentico sensore dello zinco, usando un insolito cuscinetto aromatico per rilevare il metallo nello stesso tipo di sito in cui altri membri della famiglia legano i neurotrasmettitori. Identifica inoltre specifiche reti di interazione che modulano quanto facilmente il canale si apre e si chiude, e mappa due distinti siti di legame dei farmaci che possono o inserire uno spessore tra le sbarre del varco o incastrare il poro. Per i non specialisti, il messaggio chiave è che lo zinco non è solo un nutriente statico ma un segnale attivo, e ZAC è uno dei suoi ricevitori dedicati. Mentre gli scienziati cercano i ruoli di ZAC nel corpo umano e nei disturbi neurologici collegati allo squilibrio dello zinco, queste mappe a livello atomico forniscono una guida per progettare molecole più precise per modulare questo canale e, potenzialmente, correggere la segnalazione dello zinco compromessa.
Citazione: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Parole chiave: segnalazione dello zinco, canali ionici gated da ligando, neuroscienze, struttura da crio‑EM, modulazione del canale