Clear Sky Science · it
La palmitoilazione di ASCT2 regolata dall’asse JNK1-ZDHHC14 orchestra il metabolismo del glutamine e la progressione del NSCLC
Alimentare il fuoco del cancro al polmone
Molti tumori polmonari a rapida crescita dipendono dal glutamine, un aminoacido comune che funge da carburante chiave e mattoncino per la sintesi cellulare. Questo studio svela come le cellule tumorali modulino una principale “porta” del glutamine sulla loro superficie e come interrompere questo sistema di controllo possa rallentare la crescita del cancro. Capire questa valvola nascosta del carburante aiuta a spiegare perché alcuni tumori sono così difficili da privare di nutrienti e indica nuove combinazioni farmacologiche che potrebbero interrompere in modo più efficace il loro approvvigionamento energetico.
Una porta cellulare per il glutamine
Il glutamine entra nelle cellule soprattutto attraverso una proteina trasportatrice chiamata ASCT2, che si trova nella membrana esterna e trasferisce il glutamine all’interno. Il carcinoma polmonare non a piccole cellule (NSCLC), la forma più comune di cancro al polmone, fa spesso grande affidamento sul glutamine per sostenere la rapida divisione e la sopravvivenza. Alti livelli di ASCT2 nei tumori sono collegati a malattia aggressiva e a esiti peggiori per i pazienti. Tuttavia ASCT2 è costantemente sintetizzato, modificato e degradato, sollevando la domanda: cosa determina quanto di questo guardiano rimane sulla superficie cellulare in un dato momento?
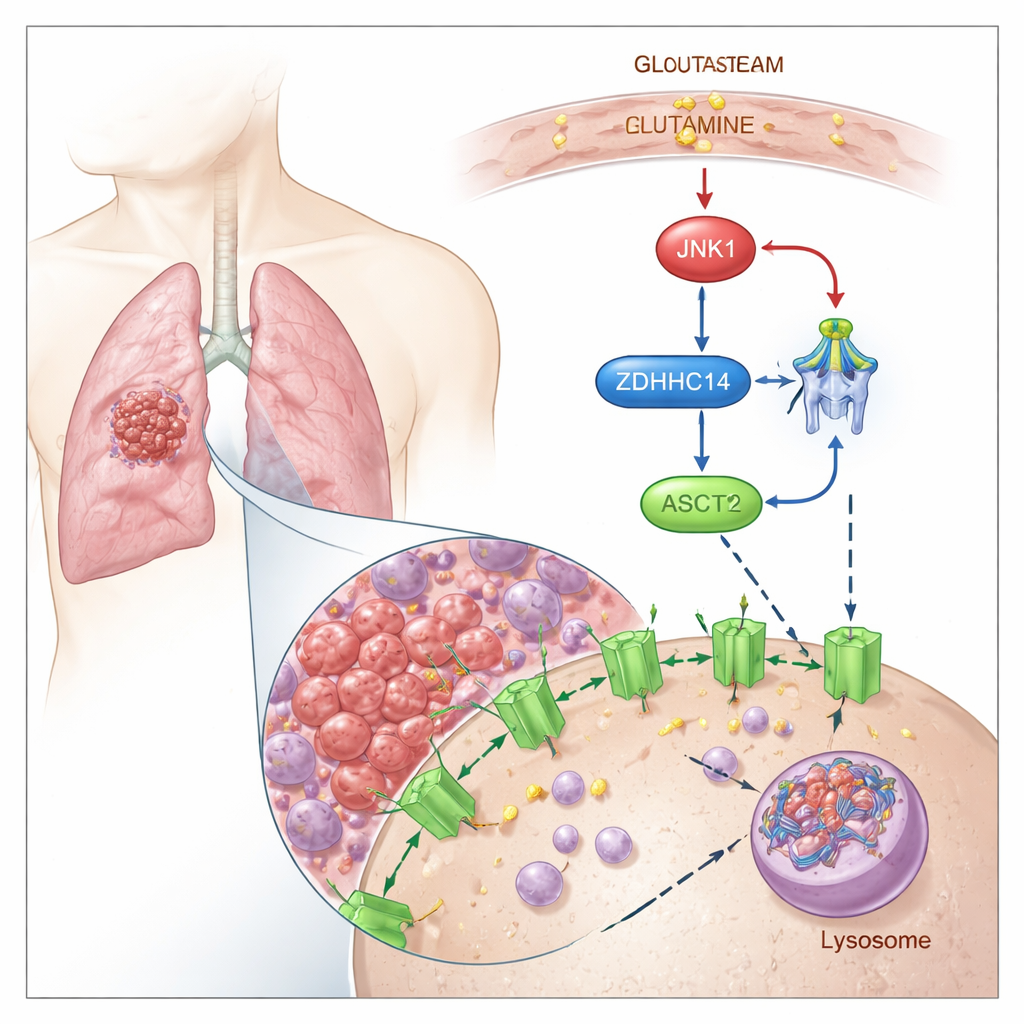
Marchiare ASCT2 per la degradazione
I ricercatori mostrano che ASCT2 è controllato da un “marchio” chimico chiamato palmitoilazione, in cui un acido grasso viene attaccato a specifici residui di cisteina nella proteina. Hanno scoperto che un enzima denominato ZDHHC14 aggiunge questo tag lipidico a due siti conservati su ASCT2 (Cys39 e Cys48). Una volta etichettata, ASCT2 viene deviata dalla superficie cellulare verso centri di riciclaggio chiamati lisosomi, dove viene degradata. Bloccare la palmitoilazione impedisce che ASCT2 venga marcata e degradata, portando a livelli proteici di ASCT2 più elevati e a un aumento dell’assorbimento di glutamine, senza modificare l’attività genica sottostante.
Un contro-enzima che protegge la porta
In opposizione a ZDHHC14 agisce un altro enzima, ABHD17B, che rimuove il tag lipidico da ASCT2. Quando ABHD17B è attivo, ASCT2 è meno palmitoilata, più stabile e più propensa a essere riciclata sulla superficie cellulare anziché diretta al lisosoma. Questo continuo mettere e togliere il marchio funziona come una manopola finemente regolata sul flusso di glutamine: ZDHHC14 spinge ASCT2 verso la distruzione, mentre ABHD17B la recupera e mantiene il trasporto del glutamine. Nelle cellule di cancro polmonare, spostare questo equilibrio verso una minore palmitoilazione aumenta l’assorbimento di glutamine e favorisce la crescita tumorale in colture e nei topi.
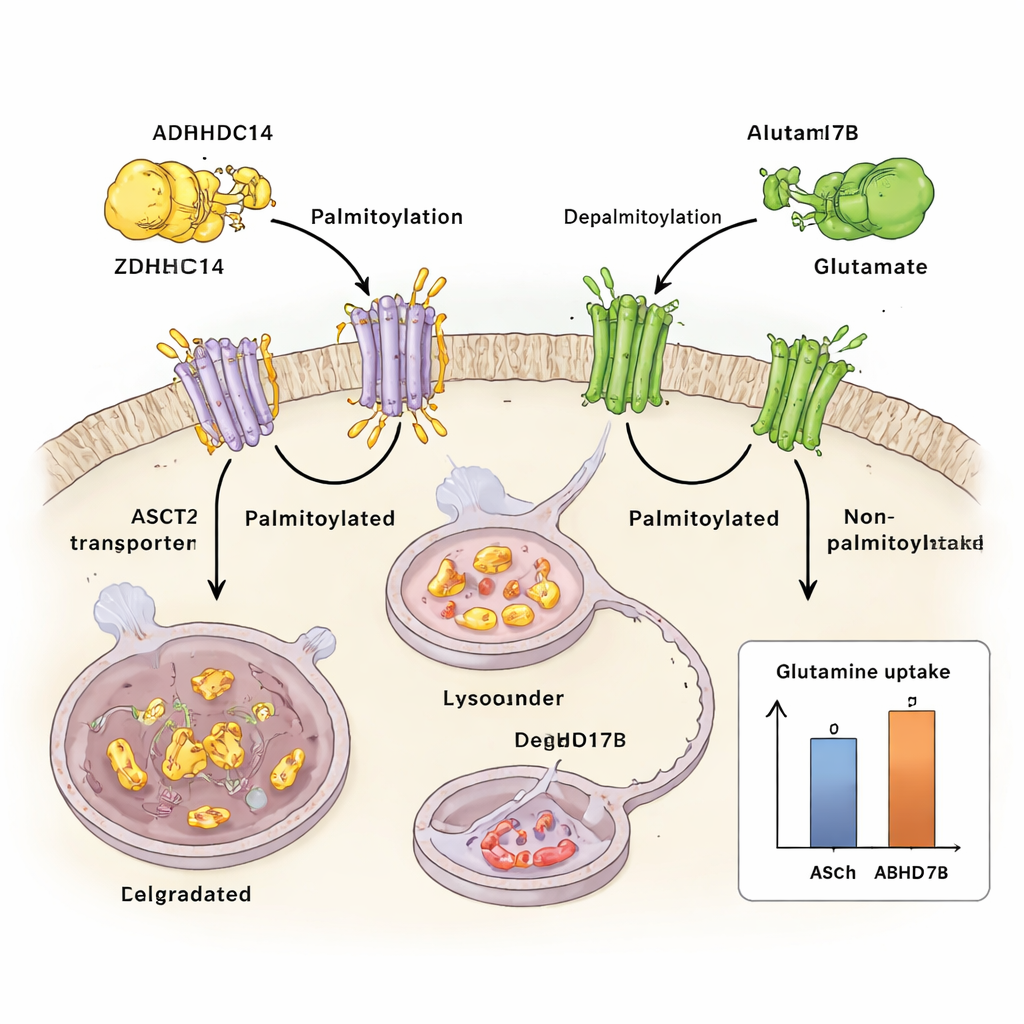
Come lo stress nutritivo riorganizza il sistema
Il gruppo ha poi esaminato cosa accade quando le cellule tumorali rimangono a corto di glutamine. In condizioni di deprivazione di glutamine, una proteina di segnalazione sensibile allo stress chiamata JNK1 si attiva. JNK1 si lega fisicamente a ZDHHC14 e aggiunge un gruppo fosfato in un sito specifico (Thr440), segnando ZDHHC14 per la sua degradazione lisosomiale. Con la riduzione dei livelli di ZDHHC14, ASCT2 riceve meno tag di palmitoilazione, evita la degradazione e si accumula sulla superficie cellulare—proprio nel momento in cui la cellula ha più bisogno di recuperare il glutamine scarso. Mutare questo singolo sito sensibile a JNK1 stabilizza ZDHHC14, ripristina l’etichettatura di ASCT2 e riduce l’assorbimento di glutamine, sottolineando quanto strettamente lo stress nutritivo sia integrato in questo circuito di controllo.
Traslare il meccanismo in terapia
Dato che ASCT2 è così importante per il metabolismo tumorale, farmaci che lo bloccano, come il composto sperimentale V9302, sono in fase di esplorazione come trattamenti contro il cancro. Questo studio rivela che la segnalazione JNK1 può contrastare la distruzione di ASCT2, proteggendo di fatto la porta del glutamine. In modelli cellulari e murini di NSCLC, la combinazione di un inibitore di JNK con V9302 ha ridotto più efficacemente l’assorbimento di glutamine, la crescita delle cellule tumorali e le dimensioni del tumore rispetto a ciascun farmaco somministrato singolarmente. Campioni di pazienti e set di dati pubblici mostrano inoltre che bassi livelli di ZDHHC14 e alti livelli di ASCT2 sono comuni nel NSCLC e associati a una sopravvivenza peggiore, suggerendo che questo profilo molecolare potrebbe aiutare a identificare i pazienti più propensi a beneficiare del targeting di questa via.
Cosa significa per i pazienti
In termini pratici, questo lavoro mostra che alcuni tumori polmonari controllano il loro carburante preferito regolando una valvola molecolare sulla loro superficie. Un trio di attori—JNK1, ZDHHC14 e ABHD17B—decide se la porta del glutamine ASCT2 venga marchiata per la distruzione o mantenuta aperta. Quando il glutamine è scarso, il sistema si sposta per preservare ASCT2 e mantenere il flusso di carburante, aiutando i tumori a sopravvivere in condizioni difficili. Bloccando congiuntamente ASCT2 e la via JNK che lo protegge, i ricercatori sono riusciti a privare le cellule tumorali di nutrienti in modo più efficace in modelli di laboratorio e animali. Pur richiedendo ulteriori verifiche, questo asse fosforilazione–palmitoilazione offre un nuovo e promettente approccio per terapie volte a tagliare le linee vitali di nutrienti dei tumori polmonari affamati di glutamine.
Citazione: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Parole chiave: metabolismo del glutamine, carcinoma polmonare non a piccole cellule, trasportatore ASCT2, palmitoilazione delle proteine, segnalazione JNK