Clear Sky Science · it
I meccanismi molecolari e le potenziali implicazioni terapeutiche dell’interazione tra metilazione del DNA e riprogrammazione metabolica nel cancro tiroideo
Perché questa ricerca conta oltre il laboratorio
Il cancro della tiroide è uno dei tumori in più rapido aumento a livello globale. Sebbene molti casi siano curabili, le forme più aggressive spesso smettono di rispondere allo iodio radioattivo, una terapia fondamentale, lasciando i pazienti con poche buone opzioni. Questo articolo di revisione spiega come due forze invisibili all’interno delle cellule—marcatori chimici sul DNA e cambiamenti nell’uso del carburante da parte delle cellule tumorali—collaborino per promuovere la crescita del cancro tiroideo e la resistenza alle terapie. Comprendere questa partnership nascosta potrebbe aprire la strada a trattamenti più precisi e duraturi.
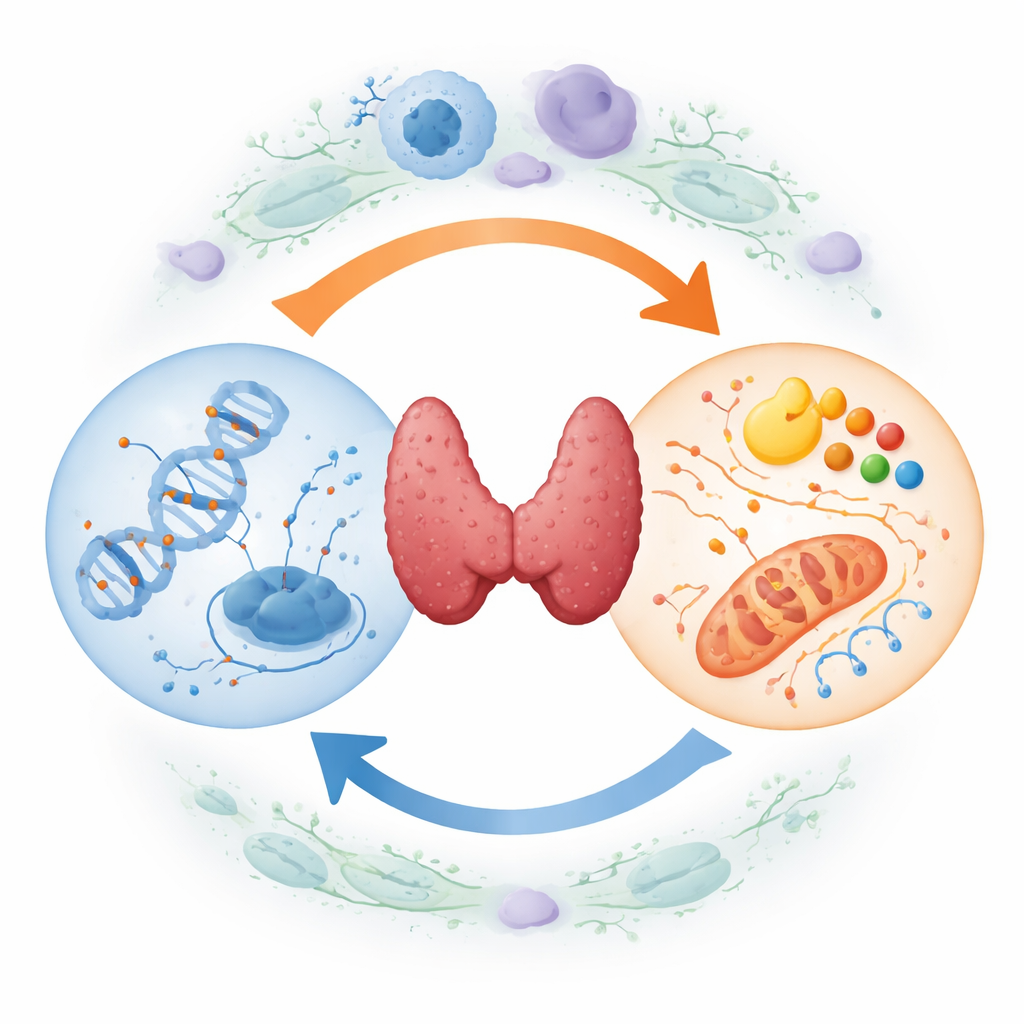
Come le cellule tumorali riscrivono il loro manuale di istruzioni
Ogni cellula porta lo stesso DNA, ma marcatori chimici chiamati gruppi metile possono accendere o spegnere i geni senza modificare il codice genetico stesso. Nel cancro della tiroide, questa “correzione” del DNA è profondamente alterata. Ampi tratti del genoma perdono marcatori metilici, il che può destabilizzare i cromosomi, mentre freni chiave della crescita e della funzione tiroidea vengono ipermetilati e silenziati. Tra questi vi sono geni oncosoppressori e geni specifici della tiroide che normalmente aiutano le cellule ad assorbire lo iodio. Il risultato è un libro delle istruzioni genetiche dove molti capitoli di sicurezza sono cancellati, favorendo una crescita incontrollata e la perdita dell’identità tiroidea normale.
Come le cellule tumorali riallacciano le loro linee di carburante
Contemporaneamente, le cellule tumorali tiroidee riorganizzano il modo in cui ottengono e usano energia. Invece di bruciare principalmente il carburante in modo efficiente nei mitocondri, si affidano fortemente alla rapida ma inefficiente degradazione degli zuccheri, generando sottoprodotti acidi che le aiutano a eludere il sistema immunitario. Inoltre aumentano la sintesi e l’ossidazione dei grassi e ridistribuiscono aminoacidi come serina e glutamina per sostenere la rapida divisione. Questi cambiamenti non sono casuali: sono guidati da segnali che promuovono il cancro e creano una rete metabolica flessibile che permette alle cellule tumorali di sopravvivere a basso ossigeno, resistere ai farmaci e colonizzare nuovi siti.
Traffico bidirezionale tra marcatori del DNA e metabolismo cellulare
Un messaggio centrale dell’articolo è che la marcatura del DNA e l’uso del carburante non sono storie separate—formano un circuito che si auto-rinforza. Da un lato, il metabolismo alterato delle cellule tumorali produce specifiche piccole molecole che agiscono come interruttori per gli enzimi che aggiungono o rimuovono i gruppi metile dal DNA. Quando i livelli di queste molecole cambiano, possono spingere il genoma verso una maggiore o minore metilazione in siti sensibili. Dall’altro lato, la metilazione del DNA può silenziare direttamente o potenziare geni che controllano l’uso degli zuccheri, la gestione dei lipidi e il trasporto di aminoacidi. Col tempo, questo traffico bidirezionale cristallizza uno stato favorevole al cancro in cui marcature anomale del DNA e metabolismo distorto si rafforzano reciprocamente.
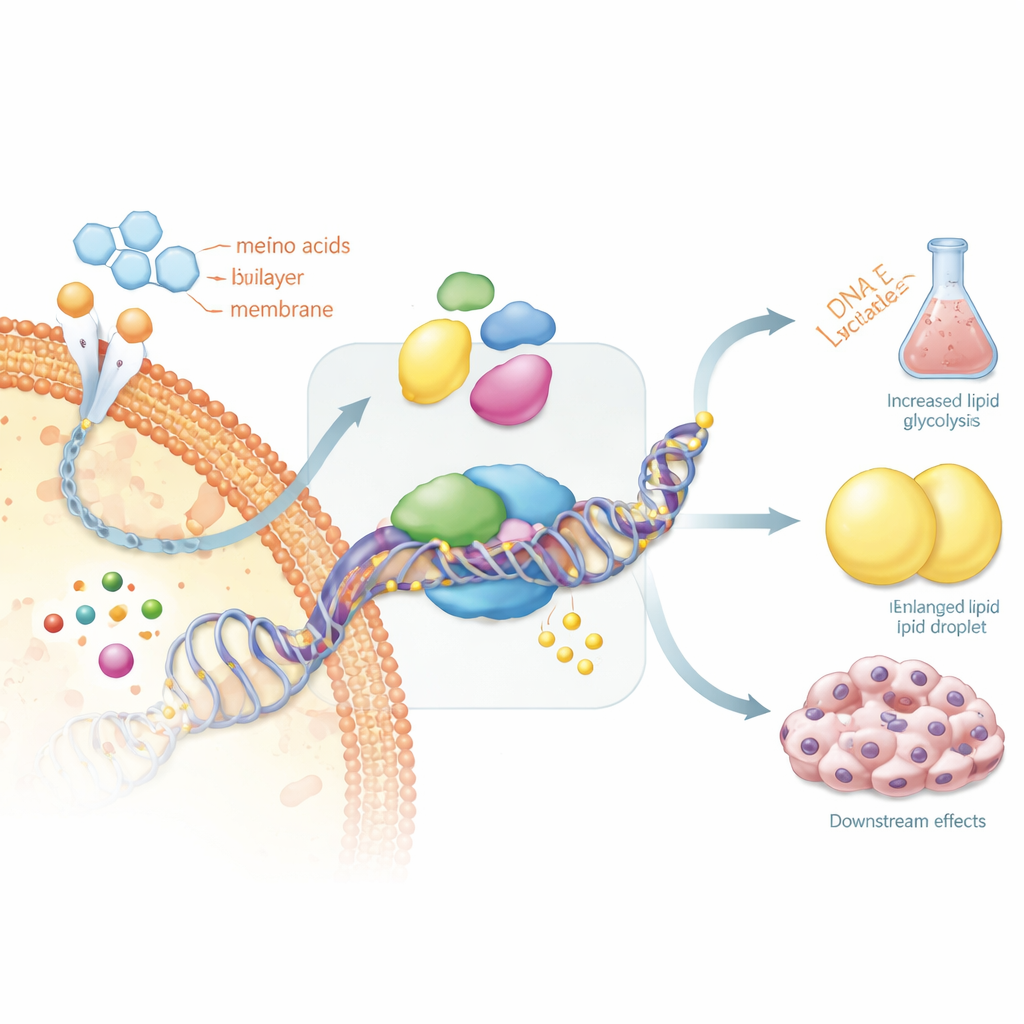
Perché alcuni tumori tiroidei smettono di “bere” iodio
Questo circuito di retroazione ha conseguenze molto pratiche per i pazienti. La terapia con iodio radioattivo funziona solo se le cellule tumorali mantengono la macchina molecolare necessaria per importare lo iodio. La revisione sottolinea che geni tiroidei chiave responsabili di ciò, incluso il recettore del TSH (ormone stimolante la tiroide) e il trasportatore sodio–iodio, vengono spesso spenti da un’ipermetilazione delle loro regioni di controllo. Una volta che ciò avviene, le cellule tumorali “dimenticano” di essere cellule tiroidee e non assorbono più lo iodio, rendendo inefficace la terapia standard. Gli autori propongono che invertire con cura queste marcature del DNA, o bloccare le vie metaboliche che le sostengono, potrebbe riattivare l’assorbimento di iodio e ripristinare la sensibilità al trattamento.
Nuove idee terapeutiche basate su una visione integrata
Considerare il cancro della tiroide come una malattia dell’“asse metilazione del DNA–metabolismo” porta a nuove strategie terapeutiche. Piuttosto che affidarsi a farmaci singoli, gli autori sostengono approcci combinati che colpiscano più punti del circuito contemporaneamente—farmaci epigenetici che allentano marcature del DNA dannose, farmaci metabolici che interrompono rotte energetiche chiave e farmaci che bloccano segnali che guidano il cancro. L’aggiunta di immunoterapie moderne e di sistemi avanzati di veicolazione dei farmaci, come nanoparticelle intelligenti, potrebbe ulteriormente spostare l’equilibrio rimodellando l’ambiente immunitario del tumore e limitando gli effetti collaterali. Dati preliminari di laboratorio e clinici suggeriscono che attacchi coordinati di questo tipo possono rallentare la malattia, ripristinare l’assorbimento di iodio in alcuni pazienti e ritardare la comparsa di resistenza.
Cosa significa per le cure future
Per un lettore non specialista, la conclusione è che i tumori tiroidei aggressivi potrebbero essere curabili non cercando una singola soluzione miracolosa, ma comprendendo e interrompendo il circolo vizioso tra marcature del DNA e metabolismo cellulare. Mappando in dettaglio questo asse e monitorando questi cambiamenti nel sangue e nei campioni tumorali, i medici potrebbero un giorno abbinare i pazienti a combinazioni su misura di terapie epigenetiche, metaboliche, mirate e immunitarie. Se avrà successo, questo approccio integrato potrebbe trasformare i tumori tiroidei più ostinati di oggi in condizioni nuovamente trattabili—e possibilmente impedirne l’evoluzione verso forme così aggressive fin dall’inizio.
Citazione: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Parole chiave: cancro della tiroide, metilazione del DNA, metabolismo del cancro, resistenza allo iodio radioattivo, terapia mirata