Clear Sky Science · it
Inibire HSP27 attiva l’interazione XBP1s/CerS1, che provoca una mitofagia guidata da DRP1, proteggendo così dalla morte cellulare e promuovendo il ciclo litico del KSHV nelle cellule di linfoma da effusione primaria
Quando lo stress cellulare diventa un’arma a doppio taglio
Le nostre cellule sopravvivono agli insulti quotidiani attivando programmi d’emergenza che riparano i danni e le mantengono in vita. Le cellule tumorali, tuttavia, possono dirottare quegli stessi programmi per crescere e proteggere virus latenti. Questo articolo esplora come bloccare una singola proteina protettiva dallo stress in un raro linfoma non solo spinga le cellule tumorali verso la morte, ma fornisca anche a un virus nascosto al loro interno una finestra per riattivarsi e moltiplicarsi. Comprendere questo delicato equilibrio potrebbe aiutare a progettare terapie che eliminino il cancro negando al tempo stesso al virus la possibilità di diffondersi.
Un virus nascosto in un linfoma aggressivo
Il linfoma da effusione primaria è un tumore molto aggressivo delle cellule B, un tipo di globuli bianchi. La maggior parte di queste cellule tumorali ospita un passeggero dormiente: il virus dell’herpes associato al sarcoma di Kaposi (KSHV). In uno stato silente, o latente, il virus produce solo poche proteine e si nasconde nel genoma dell’ospite. Alcuni stress possono spingerlo in una fase attiva, litica, in cui copia se stesso e produce nuove particelle virali, solitamente uccidendo la cellula ospite. Le cellule tumorali dipendono da vari sistemi di risposta allo stress, incluse le cosiddette heat shock protein e la risposta alle proteine non ripiegate, che le aiutano a gestire proteine mal ripiegate, alterazioni del metabolismo lipidico e danni ai mitocondri, le loro centrali energetiche. 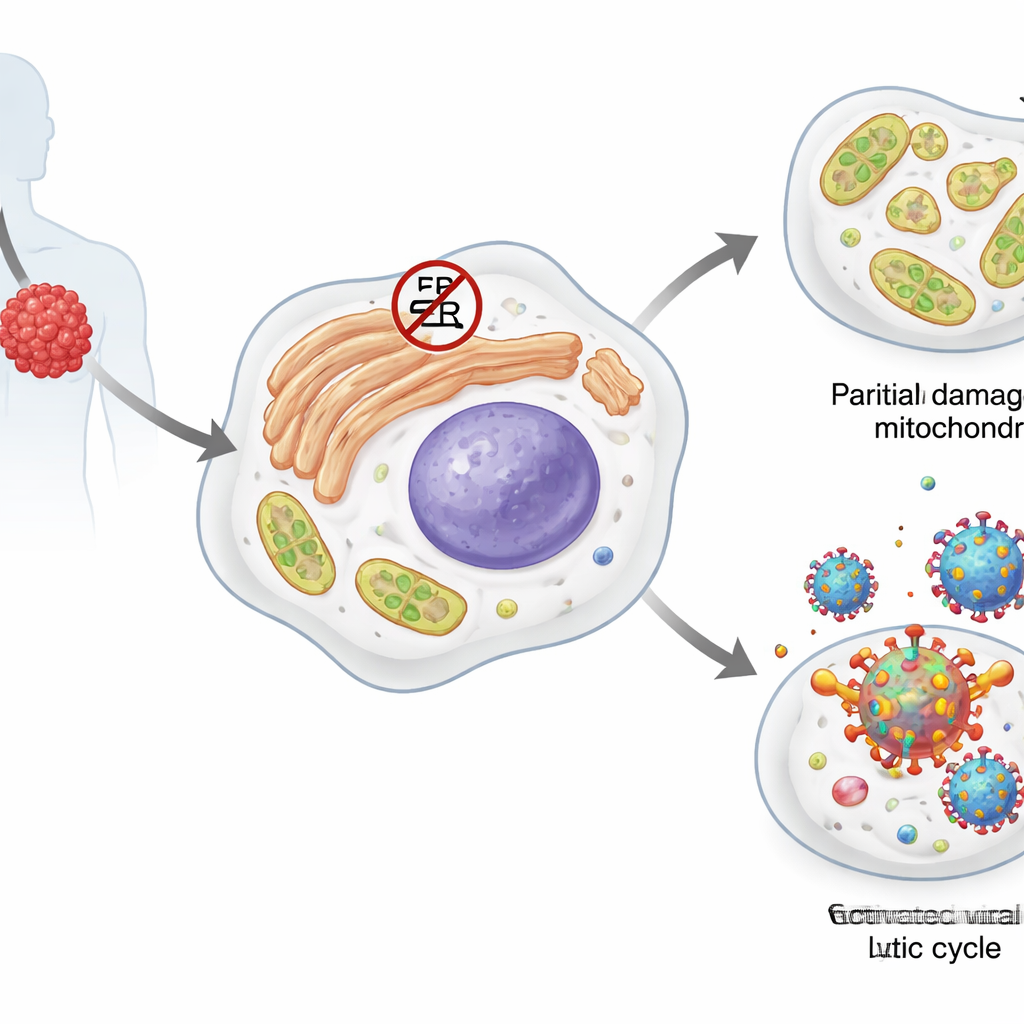
Bloccare una guardia del corpo cellulare
I ricercatori si sono concentrati su HSP27, una piccola heat shock protein nota per proteggere le cellule dallo stress. Usando un inibitore chimico chiamato J2 o silenziando il gene con piccoli RNA, hanno ridotto l’attività di HSP27 in cellule di linfoma coltivate in laboratorio. Questo ha reso le cellule meno propense a sopravvivere e ha innescato un forte segnale di stress in una rete membranosa interna chiamata reticolo endoplasmatico. Marker di questa risposta, incluse molecole protettive e pro‑morte, sono aumentati, e un interruttore chiave chiamato XBP1s è stato attivato. Allo stesso tempo, le cellule hanno mostrato maggiori segni di morte cellulare programmata, confermando che eliminare HSP27 le spinge verso un punto di non ritorno tra sopravvivenza e morte.
Un circuito di stress che comunica con i lipidi cellulari
Lo stress nel reticolo endoplasmatico è strettamente intrecciato con la gestione dei lipidi da parte della cellula. Il gruppo ha scoperto che bloccare HSP27 aumentava i livelli di CerS1, un enzima che produce una specifica molecola lipidica chiamata C18‑ceramide. Quando hanno chimicamente bloccato XBP1s, l’aumento di CerS1 è scomparso, dimostrando che XBP1s contribuisce ad attivare il gene CerS1 in queste condizioni. Colpisce che l’inibizione di CerS1 riducesse a sua volta XBP1s, rivelando un circuito di retroazione positiva: ciascun fattore sostiene l’altro. Questa stretta cooperazione molecolare non solo rimodella il metabolismo lipidico ma rafforza anche la capacità della cellula di adattarsi allo stress del reticolo endoplasmatico, pur mentre segnali di morte si accumulano.
I mitocondri riciclati invece che distrutti
Lo stress in una parte della cellula spesso si propaga ai mitocondri, le piccole centrali che generano energia. Dopo il blocco di HSP27, le cellule di linfoma hanno prodotto più specie reattive dell’ossigeno, segno di problemi mitocondriali, e livelli aumentati di DRP1, una proteina che frammenta i mitocondri in pezzi più piccoli. Gli autori hanno mostrato che il circuito XBP1s–CerS1 era responsabile dell’aumento di DRP1. Questo, a sua volta, ha innescato la mitofagia, un processo di controllo qualità in cui i mitocondri danneggiati vengono avvolti da membrane e consegnati ai "centri di riciclaggio" cellulare detti lisosomi. Usando coloranti fluorescenti e marker proteici, hanno confermato che i mitocondri venivano rimossi selettivamente. Quando hanno bloccato DRP1 chimicamente o geneticamente, questa mitofagia è diminuita e le cellule sono morte più rapidamente, il che significa che il riciclo mitocondriale stava in realtà aiutando le cellule tumorali stressate a resistere. 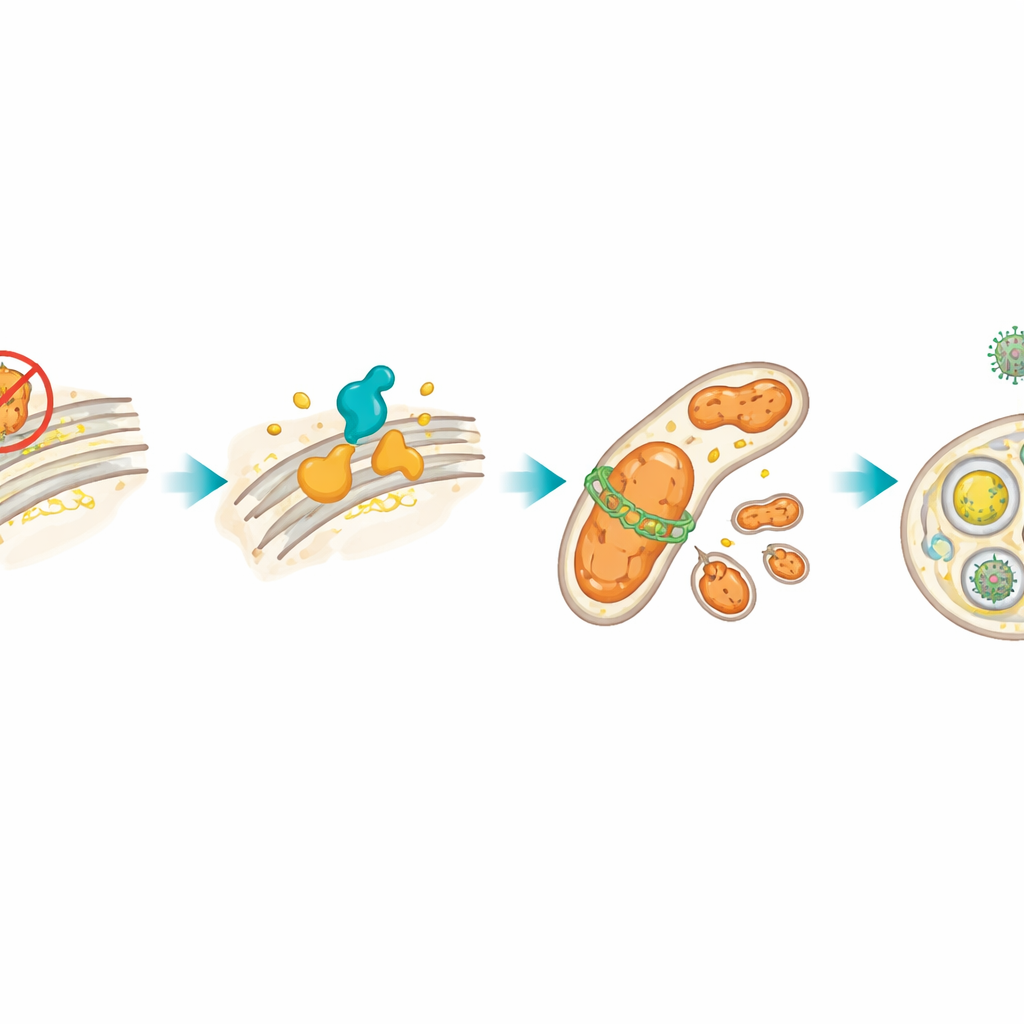
Dare al virus il tempo di scappare
La stessa mitofagia che proteggeva le cellule tumorali ha anche avvantaggiato il KSHV. L’attivazione di XBP1s, l’accumulo di C18‑ceramide e l’aumento della fissione mitocondriale sono stati tutti collegati alla riattivazione di questo virus. Qui, quando HSP27 è stato inibito, più cellule hanno espresso proteine virali precoci e tardive, chiari segni di replicazione litica. Bloccare DRP1, e quindi la mitofagia, ha ridotto questa riattivazione virale. Gli autori suggeriscono che prolungando leggermente la sopravvivenza cellulare sotto stress, la mitofagia dia al KSHV il tempo di completare il suo ciclo replicativo e lasciare la cellula morente, potenzialmente infettando nuovi bersagli e contribuendo allo sviluppo del cancro.
Cosa significa per i trattamenti futuri
Per un non specialista, il messaggio chiave è che HSP27 funge da regista centrale per il modo in cui le cellule di linfoma affrontano lo stress, riciclano mitocondri danneggiati e per il momento in cui un virus associato al cancro decide di riattivarsi. Spegnere HSP27 scatena una catena di eventi che sia compromette la sopravvivenza cellulare sia, paradossalmente, protegge temporaneamente le cellule tramite mitofagia permettendo al KSHV di replicarsi. Dal punto di vista terapeutico, combinare l’inibizione di HSP27 con farmaci che bloccano la mitofagia guidata da DRP1 potrebbe indurre le cellule tumorali a morire più rapidamente e limitare la possibilità di diffusione virale, offrendo una strategia a doppio binario contro questo linfoma letale.
Citazione: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Parole chiave: linfoma da effusione primaria, virus di Kaposi, risposta allo stress cellulare, mitofagia, proteina da shock termico HSP27