Clear Sky Science · it
Un modello murino vitale con RIPK3 cinasi-inattiva D143N rivela la sua funzione di impalcatura nell’indurre disordini infiammatori mediati da TNF
Perché questo studio sui topi è importante per l’infiammazione
Molte malattie gravi, dalle infezioni letali alle riacutizzazioni autoimmuni, sono guidate non solo da agenti patogeni o da varianti genetiche, ma anche da una risposta infiammatoria incontrollata dell’organismo. Una proteina chiamata RIPK3 è stata a lungo considerata un esecutore chiave di una forma violenta di morte cellulare che alimenta questa infiammazione, rendendola un bersaglio farmacologico interessante. Tuttavia, RIPK3 svolge anche altri ruoli meno compresi all’interno delle cellule. Questo studio descrive un nuovo tipo di topo da laboratorio che separa in modo netto l’attività uccidente di RIPK3 dal suo ruolo di “impalcatura” di segnalazione, rivelando come ciascuno contribuisca all’infiammazione e indicando nuove strategie terapeutiche.
Due modalità d’azione di una proteina della morte
Le cellule possono morire in modi ordinati o turbolenti. Nella morte cellulare ordinata e “silenziosa”, l’organismo ricicla le componenti cellulari senza molta allerta. In una forma più disordinata detta necroptosi, le cellule si rompono e riversano il loro contenuto, scatenando forti risposte immunitarie. RIPK3 è centrale nella necroptosi: quando attivata, stimola un’altra proteina che crea fori nella membrana cellulare. Studi precedenti avevano però suggerito che RIPK3 può anche favorire la suicidio cellulare classico mediato da caspasi e può potenziare la segnalazione infiammatoria anche senza causare la morte cellulare. Separare questi ruoli è stato difficile perché le forme inattive di RIPK3 finora disponibili o uccidevano gli embrioni o riducevano drasticamente i livelli della proteina, rendendo complesso studiarne il normale comportamento come impalcatura.
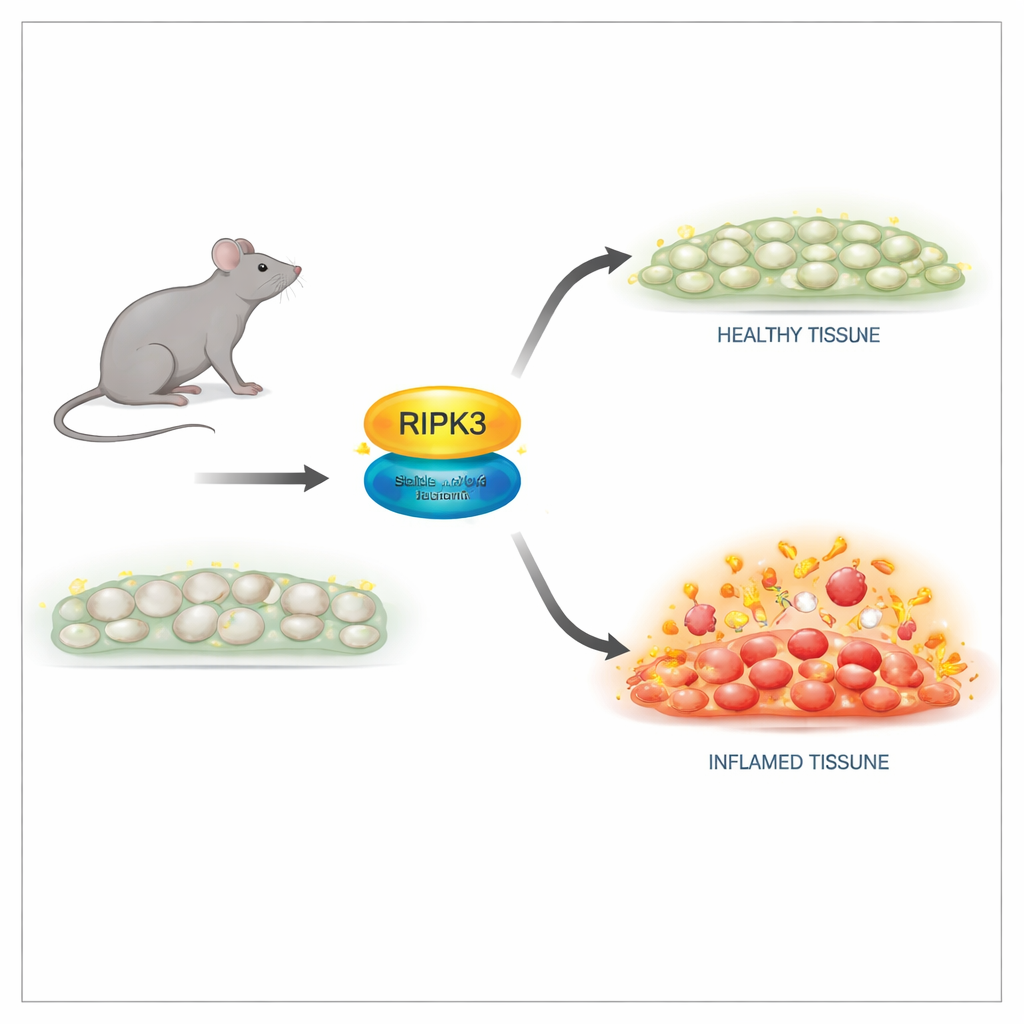
Un modo più sicuro per disattivare la funzione uccidente
I ricercatori hanno ingegnerizzato topi portatori di una modifica sottile nella proteina RIPK3 in una singola posizione, denominata D143N, che abolisce la sua attività enzimatica preservandone la struttura. Nelle cellule di questi topi, i livelli di RIPK3 e l’architettura tissutale apparivano normali, e gli animali sono nati e cresciuti come i loro fratelli sani. Importante, le cellule con la versione D143N erano completamente resistenti a molteplici stimoli di necroptosi, inclusi segnali da tumor necrosis factor (TNF), recettori toll-like e infezione virale. RIPK3 mutante non riusciva più ad attivare il partner a valle né a formare il complesso distruttivo necessario alla rottura della membrana, ma non provocava apoptosi spontanea, evitando gli effetti letali osservati in precedenti mutanti di RIPK3.
Separare lo sviluppo dalla malattia
Uno dei ruoli meglio noti di RIPK3 riguarda gli embrioni privi di un’altra proteina chiave, la caspasi-8: senza caspasi-8, la necroptosi mediata da RIPK3 uccide l’embrione. In questo studio, l’introduzione della versione D143N di RIPK3 ha completamente salvato questi topi altrimenti non vitali. Si sono sviluppati normalmente e sono risultati fertili, dimostrando che l’attività uccidente di RIPK3 è superflua per lo sviluppo normale se la sua struttura è conservata. Tuttavia, quando i topi adulti sono stati sfidati con alte dosi di TNF per indurre una sindrome infiammatoria simile a shock, lo scenario è cambiato. Gli animali totalmente privi di RIPK3 erano fortemente protetti dalla morte, dal danno tissutale e dalle molecole infiammatorie nel sangue. I topi con la versione D143N, pur privi di necroptosi, risultavano solo parzialmente protetti. Questo indicava che il ruolo di impalcatura non uccidente di RIPK3 contribuiva comunque a promuovere l’infiammazione.
Segnalazione da impalcatura che alimenta l’infiammazione
Per comprendere questo contributo non letale, il gruppo ha esaminato l’attività genica nell’intestino di topi trattati con TNF. Negli animali privi di RIPK3, molti geni infiammatori risultavano fortemente attenuati. Nei topi D143N, invece, l’attenuazione era più debole e geni collegati alle risposte interferoniche e immunità innata restavano più attivi. A livello proteico, il TNF attivava in modo robusto le vie di segnalazione JAK–STAT1 ed ERK nei topi normali e in quelli D143N, ma questa attivazione era quasi completamente assente quando RIPK3 veniva eliminata del tutto. Ciò dimostrava che, anche senza la sua funzione uccidente, la presenza fisica di RIPK3 nei complessi di segnalazione aiuta a trasmettere i segnali di TNF verso un programma pro-infiammatorio tramite JAK–STAT1.
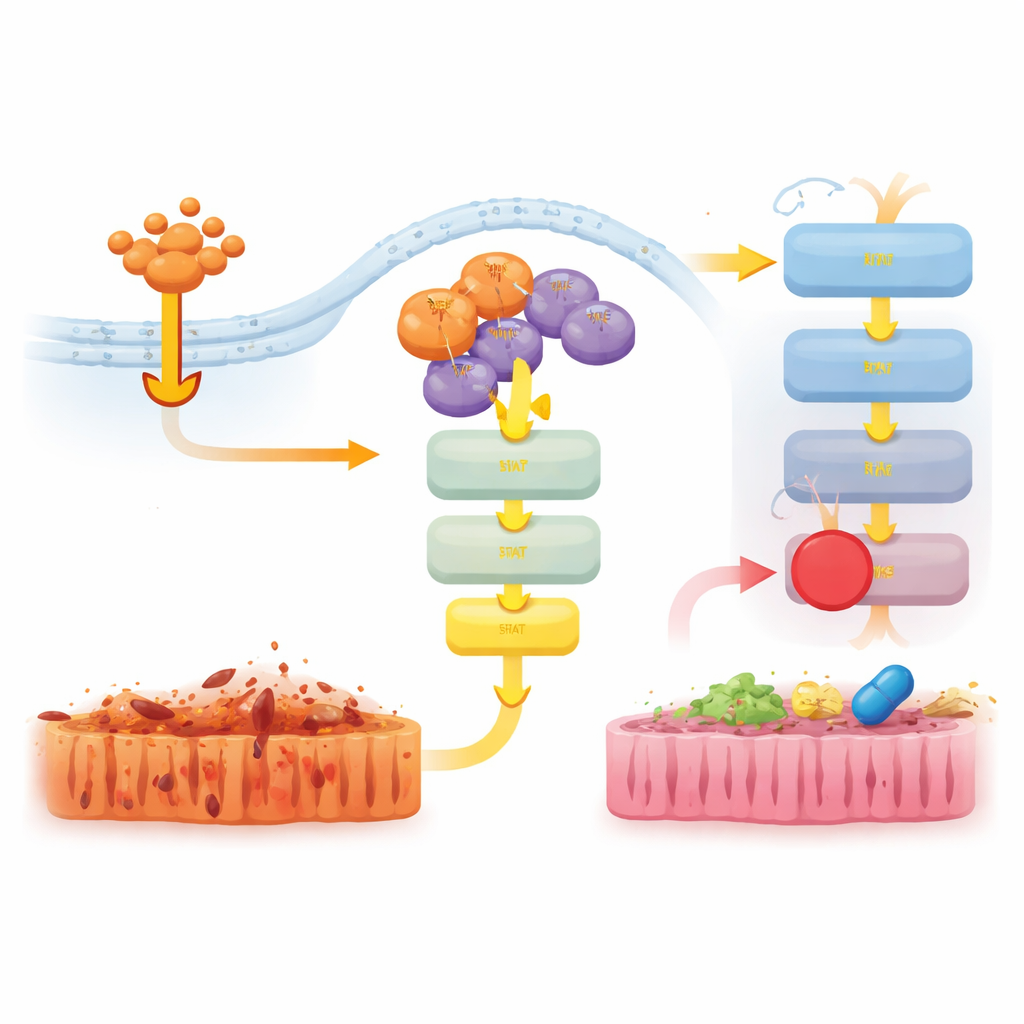
Attenuare segnali dannosi con farmaci mirati
I ricercatori hanno quindi testato se bloccare queste vie a valle potesse attenuare la malattia nei topi D143N sottoposti a shock indotto da TNF. Il trattamento con un inibitore JAK1/2, ma non con un inibitore di ERK, ha ridotto la perdita di temperatura corporea, abbassato i livelli della molecola infiammatoria IL-6 e diminuito il danno tissutale intestinale e la morte cellulare. Un altro inibitore mirato a RIPK1 ha anch’esso fornito una protezione marcata e attenuato l’attivazione di JAK–STAT1 ed ERK. Nel complesso, questi risultati suggeriscono che la funzione di impalcatura di RIPK3 agisce in collaborazione con RIPK1 per attivare JAK–STAT1 e promuovere l’infiammazione, e che interrompere questa segnalazione può ridurre il danno tissutale anche quando la necroptosi è già bloccata.
Implicazioni per i trattamenti futuri
Per anni RIPK3 è stata vista principalmente come l’interruttore di una forma tossica di morte cellulare, e lo sviluppo farmacologico si è concentrato sul bloccarne l’attività enzimatica. Questo studio mostra che ciò potrebbe non essere sufficiente: RIPK3 può ancora agire come piattaforma fisica che amplifica i segnali infiammatori attraverso JAK–STAT1, contribuendo a shock e danno tissutale. Il nuovo modello murino D143N rivela con chiarezza questi ruoli duali, stabilendo uno strumento potente per studiare quando e come ciascuna funzione conta in diverse malattie. Per i pazienti, il lavoro suggerisce che combinare farmaci che prendono di mira RIPK3 o RIPK1 con inibitori di JAK–STAT1 potrebbe calmare più efficacemente l’infiammazione dannosa in condizioni guidate da TNF e citochine correlate.
Citazione: Du, Y., Li, J., Zhao, C. et al. A viable kinase-inactive RIPK3 D143N mouse model reveals its scaffold function in driving TNF-induced inflammatory disorder. Cell Death Discov. 12, 107 (2026). https://doi.org/10.1038/s41420-026-02962-x
Parole chiave: RIPK3, necroptosi, infiammazione, shock da TNF, JAK-STAT1