Clear Sky Science · it
L’asse AdipoR1–AMPK sopprime il cancro al seno attraverso sottotipi molecolari tramite vie multimodali di morte cellulare, inclusi ferroptosi e apoptosi
Perché le cellule adipose contano nel cancro al seno
La maggior parte di noi pensa al grasso corporeo come a una riserva passiva di energia, ma le cellule adipose sono fabbriche attive che rilasciano ormoni e molecole segnalatrici nel flusso sanguigno. Questo studio esplora come uno di questi segnali derivati dal tessuto adiposo, che agisce tramite una molecola chiamata AdipoR1 sulle cellule del cancro al seno, possa rallentare la crescita tumorale. Il lavoro è importante perché suggerisce un nuovo modo di trattare molte forme di cancro al seno sfruttando la comunicazione tra il tessuto adiposo e i tumori, potenzialmente potenziando gli effetti dei farmaci esistenti.
Uno sguardo su molti tumori
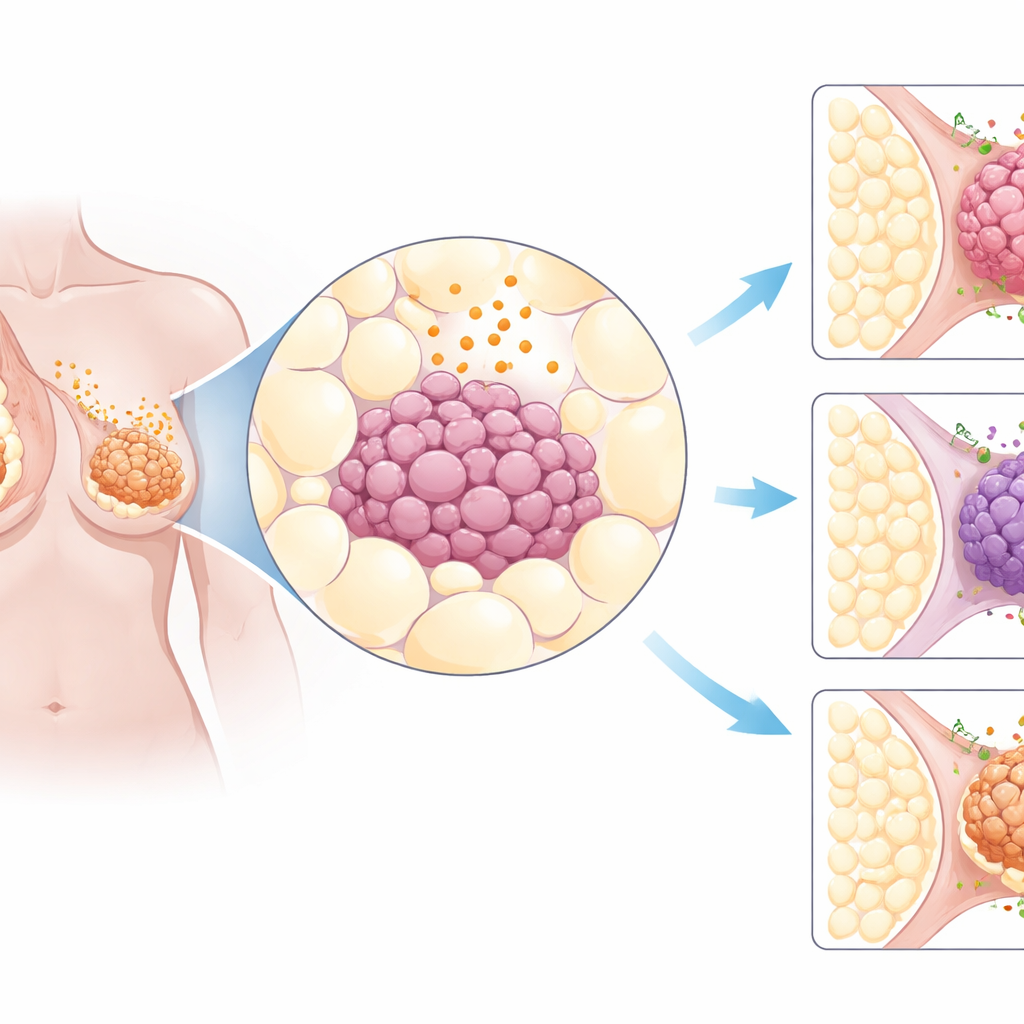
I ricercatori hanno iniziato setacciando grandi banche dati pubbliche sul cancro che contengono informazioni genetiche provenienti da migliaia di tumori di pazienti. Si sono concentrati su circa tre dozzine di geni coinvolti nei segnali provenienti dal tessuto adiposo e nelle strutture cellulari che ricevono tali segnali. Confrontando i tumori provenienti da 31 diversi organi con il tessuto sano, è emerso un modello chiaro: i tumori al seno mostravano variazioni particolarmente marcate in questi segnali legati al grasso. In particolare, il recettore AdipoR1 risultava spesso espresso a livelli superiori al normale nei tumori mammari, indipendentemente dal fatto che fossero guidati da ormoni, HER2‑positivi o del più aggressivo tipo triplo negativo. Campioni tissutali di oltre 600 carcinomi mammari hanno confermato che la proteina AdipoR1 era ampiamente presente nelle cellule tumorali.
Testare un farmaco che imita il segnale adiposo sulle cellule tumorali
Per capire cosa faccia effettivamente AdipoR1 all’interno dei tumori, il team ha utilizzato linee cellulari di cancro al seno coltivate in laboratorio, rappresentative di diversi sottotipi comuni. Hanno trattato queste cellule con AdipoRon, una piccola molecola che attiva AdipoR1. AdipoRon ha rapidamente acceso un noto interruttore di rilevamento energetico nelle cellule chiamato AMPK, dimostrando che il segnale transitava correttamente. All’aumentare della dose di AdipoRon, le cellule tumorali si dividevano più lentamente, si muovevano meno nei test di guarigione delle ferite e molte andavano incontro all’autodistruzione programmata. Quando i ricercatori riducevano deliberatamente i livelli di AdipoR1 nelle cellule, l’effetto di AdipoRon si riduceva notevolmente, mentre potenziare AdipoR1 rendeva il farmaco più efficace, collegando direttamente l’effetto a questo recettore.
Molteplici modi per spingere le cellule tumorali verso la morte
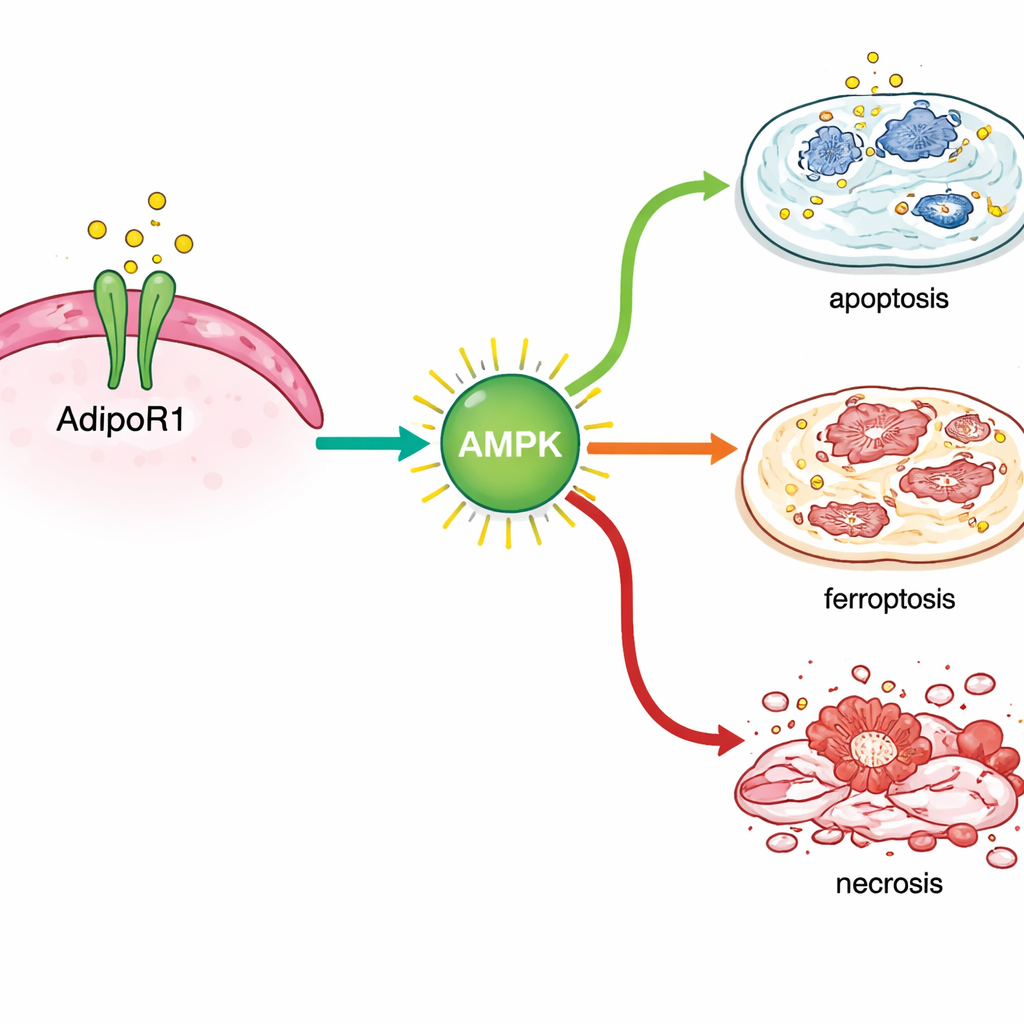
Analizzando l’attività genica dopo il trattamento, gli scienziati hanno scoperto che AdipoRon attivava risposte di stress all’interno delle cellule di cancro al seno. Ha acceso geni legati alla morte cellulare programmata classica così come quelli coinvolti in una forma più recentemente riconosciuta di distruzione cellulare dipendente dal ferro chiamata ferroptosi. Marcatori chiave di questo processo aumentavano sia a livello di RNA sia di proteina, specialmente nelle cellule di cancro al seno sensibili agli ormoni, e i rilevamenti chimici dei lipidi cellulari danneggiati supportavano questa osservazione. Allo stesso tempo, AdipoRon riduceva i livelli di proteine che normalmente aiutano le cellule tumorali a sopravvivere, inclusi fattori della riparazione del DNA (BRCA1 e BRCA2), il recettore per gli estrogeni che guida la crescita in molti tumori, e TROP2, una molecola di superficie associata a comportamenti aggressivi.
Un aiuto per i trattamenti attuali, non un sostituto
Il team si è poi chiesto se l’attivazione di AdipoR1 potesse integrare i farmaci standard. Nelle cellule di cancro al seno sensibili agli ormoni, la combinazione di AdipoRon e tamoxifene ha prodotto una soppressione della crescita maggiore rispetto a ciascun farmaco usato singolarmente. Nelle linee triplo negative, AdipoRon ha potenziato gli effetti di comuni agenti chemioterapici come paclitaxel e doxorubicina. Passando a modelli murini portatori di tumori mammari sensibili agli ormoni, i ricercatori hanno somministrato AdipoRon per via orale. I tumori negli animali trattati crescevano più lentamente e presentavano aree morte più ampie all’esame istologico. È importante sottolineare che i topi non hanno mostrato effetti collaterali evidenti in termini di comportamento, peso o salute epatica durante il periodo di trattamento.
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati suggeriscono che attivare AdipoR1 nelle cellule di cancro al seno mette in moto diverse vie sovrapposte verso la morte cellulare indebolendo al contempo sistemi chiave di sopravvivenza, e che questo approccio funziona attraverso differenti forme genetiche della malattia. Piuttosto che sostituire le terapie attuali, farmaci che mirano AdipoR1 come AdipoRon potrebbero fungere da aggiunte che rendono i tumori più vulnerabili alla terapia ormonale, alla chemioterapia o a futuri agenti mirati. Prima che questa strategia possa arrivare in clinica, i ricercatori dovranno sviluppare attivatori di AdipoR1 più potenti e selettivi, chiarire in quali pazienti i tumori esprimono il recettore in modo più marcato e valutare accuratamente la sicurezza. Ciononostante, questo lavoro indica un’idea interessante: i segnali provenienti dal nostro tessuto adiposo potrebbero essere reindirizzati per aiutare a combattere il cancro al seno invece di favorirne la crescita.
Citazione: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Parole chiave: cancro al seno, adipokine, AdipoR1, vie di morte cellulare, metabolismo del cancro