Clear Sky Science · it
Ruolo delle lipid rafts nello signaling oncogenico mediato da FGFR2c tramite il coinvolgimento del canale TRPA1 nelle cellule di adenocarcinoma duttale pancreatico
Perché contano queste piccole isole nelle membrane cellulari
Il cancro del pancreas è uno dei tumori più letali, in parte perché le sue cellule sono particolarmente abili nello staccarsi dal tumore primario e invadere i tessuti circostanti. Questo studio esamina piccole “isole” nella superficie esterna delle cellule tumorali, composte da colesterolo e lipidi, e pone una domanda semplice ma di grande portata: queste isole favoriscono l’attivazione di un segnale di crescita che rende il cancro pancreatico più aggressivo, e la loro perturbazione può rallentare il processo?
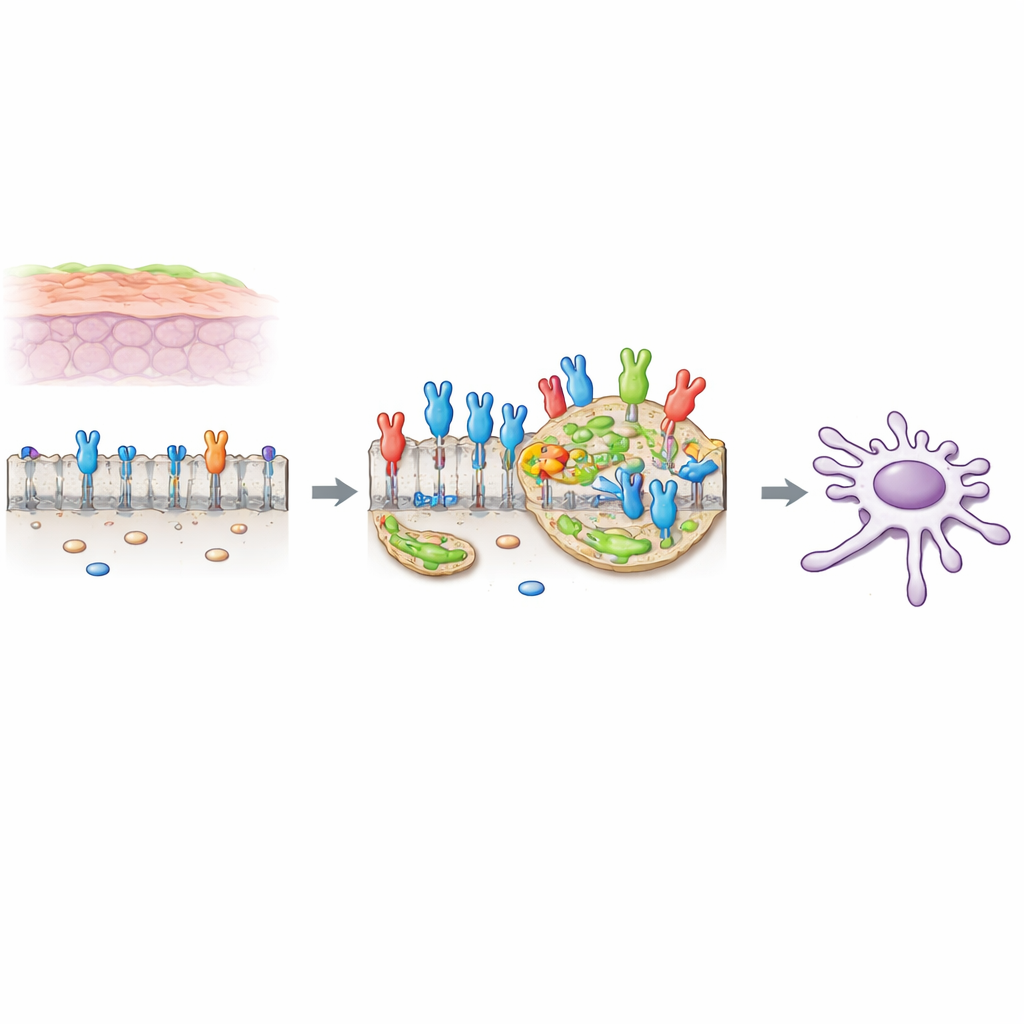
Un interruttore che promuove il cancro sulla superficie cellulare
Molte cellule possiedono interruttori sulla loro superficie che rispondono a segnali di crescita. Uno di questi interruttori, chiamato FGFR2c, è una variante normalmente presente in cellule più flessibili e mobili, ma diventa anormalmente abbondante nelle cellule di adenocarcinoma duttale pancreatico (PDAC). Quando questo interruttore viene attivato dalla sua molecola partner nell’ambiente, induce cambiamenti noti come transizione epitelio-mesenchimale (EMT), che rendono le cellule meno aderenti e più capaci di muoversi e invadere. Lavori precedenti degli autori hanno mostrato che, nelle cellule PDAC, FGFR2c attiva una catena di messaggeri intracellulari che coinvolge una proteina chiamata PKCε e diverse vie classiche di crescita, aumentando la sopravvivenza, la motilità e l’invasività cellulare.
Isole ricche di colesterolo come amplificatori del segnale
La membrana esterna di una cellula non è uniforme. Contiene piccole zone ricche di colesterolo chiamate lipid rafts, che funzionano come piattaforme in miniatura in cui le molecole di segnalazione possono raggrupparsi e comunicare in modo più efficiente. I ricercatori hanno scoperto che quando FGFR2c viene attivato dal suo segnale esterno, una quantità maggiore del recettore si sposta in queste lipid rafts. Usando marcatori fluorescenti e frazionamento biochimico, hanno dimostrato che FGFR2c attivato si concentra in queste patch, mentre la sua distribuzione al di fuori delle rafts passa da uno schema uniforme a uno puntinato, coerente con il clustering del recettore su queste isole.
Distruggere le isole indebolisce i tratti cancerosi
Per verificare se queste isole lipidiche siano essenziali per gli effetti promuoventi il cancro di FGFR2c, il team ha usato un composto (metil-β-ciclodestrina) che rimuove selettivamente il colesterolo dalla membrana e destabilizza le lipid rafts senza uccidere le cellule. Nelle cellule PDAC ricche di FGFR2c, la perturbazione delle rafts ha fortemente ridotto l’attivazione di molecole chiave a valle del recettore e attenuato il programma EMT: geni e proteine associati a uno stato mobile e invasivo sono diminuiti, mentre le caratteristiche epiteliali sono state in parte ripristinate. Lo stesso trattamento ha anche abbassato i livelli di proteine legate all’invasione come MCL-1, SRC e enzimi degradanti la matrice, e ha ridotto la capacità delle cellule tumorali di muoversi e penetrare in un gel che simula il tessuto circostante. Le cellule con pochissimo FGFR2c hanno mostrato quasi nessuna risposta, sottolineando quanto sia centrale questa partnership recettore–raft in questi tumori.
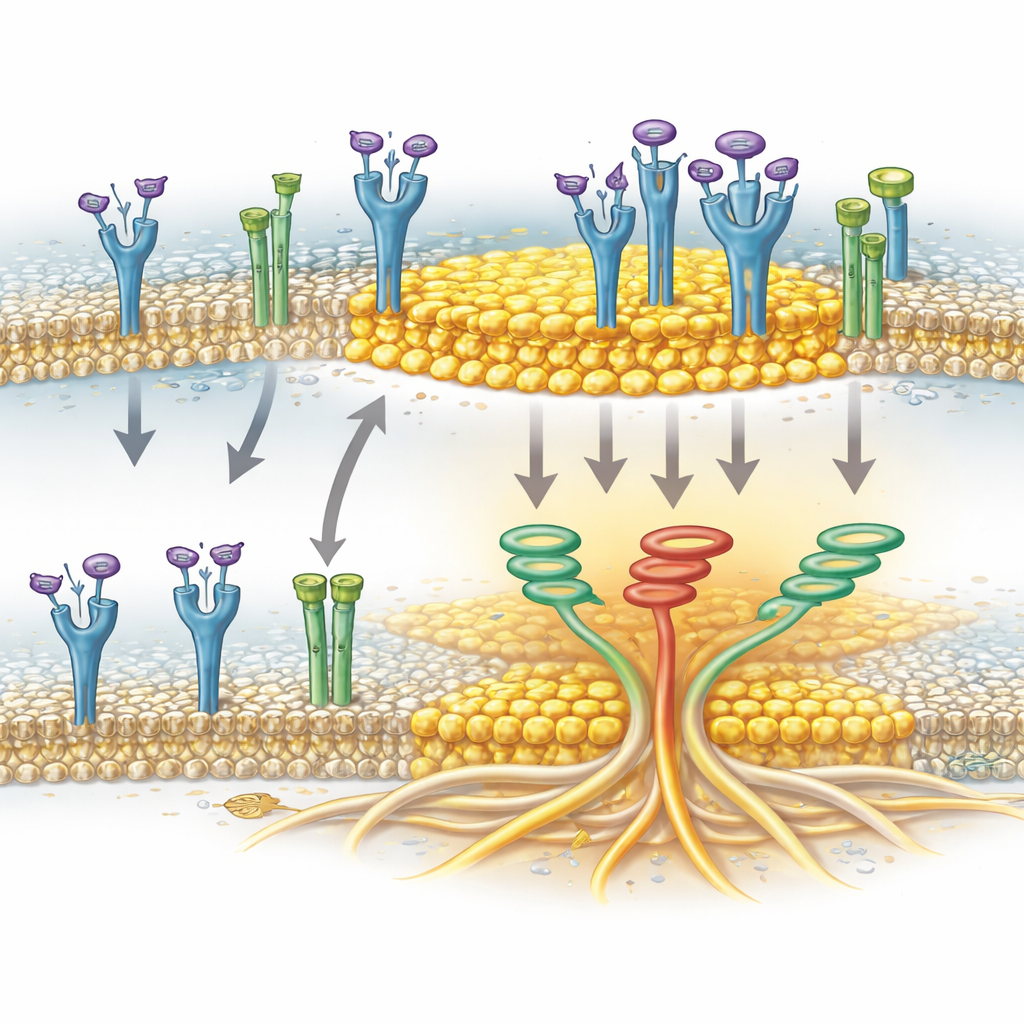
Un canale ionico come facilitatore del clustering
Lo studio identifica anche un sorprendente alleato: TRPA1, una proteina canale nota soprattutto per rilevare irritanti e stress ossidativo nei nervi. Nelle cellule del cancro pancreatico, TRPA1 è presente alla membrana e può risiedere nelle lipid rafts. Gli autori hanno mostrato che TRPA1 si associa fisicamente a FGFR2c quando il recettore è attivato e che questa associazione coincide con l’arricchimento di FGFR2c nelle frazioni di raft. Quando i livelli di TRPA1 sono stati ridotti, FGFR2c attivato non si è più accumulato efficientemente nelle regioni di raft, anche se le raft stesse restavano intatte. Ciò indica che TRPA1 non è un semplice passeggero passivo, ma aiuta attivamente a scortare o stabilizzare FGFR2c all’interno di queste piattaforme ricche di colesterolo, dove il recettore può attivare in modo più efficace la rete di segnalazione invasiva.
Cosa significa questo per i trattamenti futuri
Nel complesso, il lavoro descrive un quadro in cui FGFR2c, TRPA1 e le lipid rafts formano un’unità cooperativa che rafforza il comportamento invasivo delle cellule del cancro pancreatico. FGFR2c fornisce il segnale di crescita, le lipid rafts offrono il palcoscenico fisico dove si assemblano i complessi di segnalazione, e TRPA1 contribuisce a portare il recettore su quel palcoscenico. Per il lettore non specialistico, la conclusione chiave è che non sono importanti solo le molecole che causano il cancro, ma anche i minuscoli paesaggi di membrana che occupano, i quali possono determinare quanto diventi pericoloso un tumore. Mirare a FGFR2c, TRPA1 o alla stabilità di queste isole ricche di colesterolo—da soli o in combinazione—potrebbe permettere a terapie future di indebolire la macchina invasiva delle cellule del cancro pancreatico in modo più preciso e specifico per il tumore.
Citazione: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Parole chiave: cancro del pancreas, lipid rafts, FGFR2c, canale TRPA1, invasione cellulare