Clear Sky Science · it
Mirare i mutanti p53 del cancro Y220C, Y220N e Y220S con lo stabilizzatore a piccola molecola rezatapopt
Perché questo è importante per i futuri trattamenti del cancro
Il cancro spesso disattiva p53, una proteina talvolta definita il “guardiano” della cellula, mutandola in modo che non riesca più a tenere sotto controllo le cellule pericolose. Una particolare alterazione di p53, nota come Y220C, è comune nei tumori solidi ed è diventata un caso di prova per farmaci che mirano a riparare p53 difettoso piuttosto che uccidere le cellule direttamente. Questo studio pone una domanda pratica, centrata sul paziente: un promettente farmaco sperimentale, rezatapopt, già in sperimentazioni cliniche per Y220C, può anche aiutare persone i cui tumori portano varianti più rare ma strettamente correlate nella stessa posizione di p53?
Un farmaco progettato per tamponare una crepa in p53
Molte mutazioni di p53 fanno sì che la proteina si apra e perda la sua forma precisa. Nella mutazione Y220C, la modifica crea una piccola cavità sulla superficie della proteina — un difetto che i chimici hanno capito si potrebbe “tappare” con piccole molecole su misura per stabilizzare p53. Rezatapopt è una di queste molecole, progettata partendo da serie chimiche precedenti che si legano in questa cavità e agiscono come una staffa molecolare. Gli autori si concentrano su altre due mutazioni nello stesso residuo amminoacidico, Y220S e Y220N, che anch’esse creano una tasca simile ma destabilizzano p53 ancora più della Y220C. Se rezatapopt potesse tamponare anche queste varianti, potrebbe estendere questo approccio di medicina di precisione a migliaia di pazienti in più ogni anno. 
Misurare quanto rezatapopt afferra e stabilizza p53 mutante
Per testarlo, il team ha purificato il dominio centrale di p53 che lega il DNA con le varianti Y220C, Y220S o Y220N ed ha esposto ciascuna a rezatapopt (e a congeneri chimici vicini). Utilizzando saggi basati sul calore, hanno mostrato che tutte e tre le proteine mutanti diventano più stabili quando il farmaco si lega, con Y220C e Y220S che recuperano efficacemente una robustezza simile al tipo selvatico. Per contro, Y220N recupera solo parte della stabilità perduta. Una seconda tecnica che misura il calore rilasciato al legame ha rivelato il perché: rezatapopt si attacca molto strettamente a Y220C (ordine di qualche decina di nanomolare), un po’ meno fortemente a Y220S e più debolmente a Y220N, sebbene tutte le affinità rientrino in intervalli che i chimici farmaceutici considerano promettenti.
Vedere la toppa molecolare a livello atomico
Strutture cristallografiche ad alta risoluzione hanno fornito una spiegazione visiva. In tutti e tre i mutanti, rezatapopt si annida nella fessura creata dalla mutazione con una posa conservata: il suo impianto centrale riempie la cavità, un’estremità raggiunge in profondità la tasca con un cluster di atomi di fluoro e l’altra estremità interagisce con un anello proteico vicino. Il farmaco stabilisce una rete di contatti, incluso un atomo di fluoro posizionato strategicamente che interagisce con lo scheletro della proteina. Per Y220S queste interazioni si mantengono con solo spostamenti minori, permettendo una forte stabilizzazione. Per Y220N, invece, il legame del farmaco costringe la catena laterale dell’asparagina al nucleo lipofobico della proteina in modo energeticamente sfavorevole e alcuni contatti con l’“ancora” fluorurata del farmaco vengono persi. Questo adattamento forzato spiega sia il legame più debole sia il recupero incompleto della stabilità. 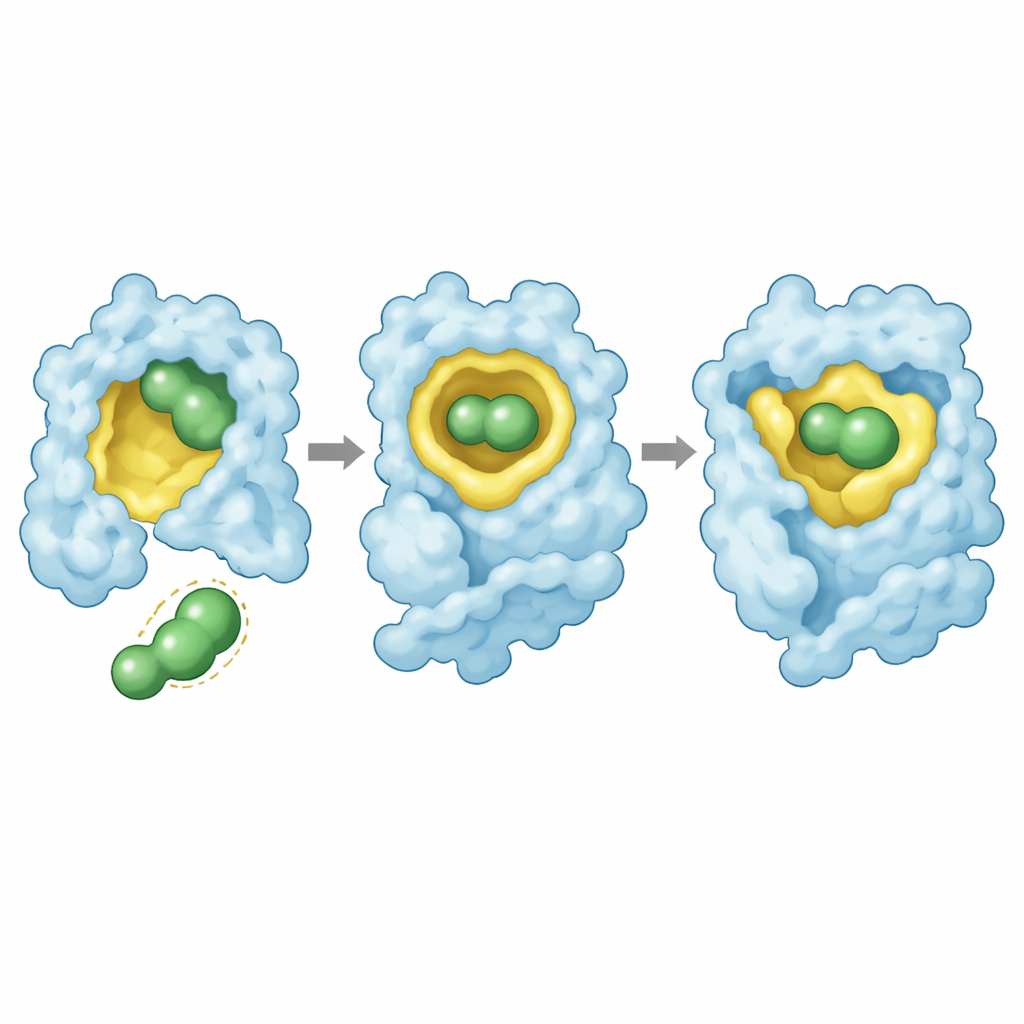
Dalla riparazione della proteina al comportamento cellulare
La prova cruciale è se tale stabilizzazione riesce a riattivare il ruolo protettivo di p53 all’interno di cellule vive. I ricercatori hanno ingegnerizzato cellule di carcinoma polmonare prive di p53 endogeno per esprimere le varianti Y220C, Y220S, Y220N o Y220H. Trattate con rezatapopt, le cellule portatrici di Y220C hanno mostrato una forte attivazione dei classici geni bersaglio di p53 coinvolti nell’arresto del ciclo cellulare e nell’induzione della morte cellulare. Le cellule Y220S hanno mostrato un quadro molto simile — recupero della forma ripiegata e attiva di p53, forte attivazione genica, rallentamento della proliferazione e aumento della morte cellulare — ma solo a concentrazioni del farmaco oltre dieci volte superiori a quelle necessarie per Y220C. Le cellule Y220N, per confronto, non hanno mostrato una chiara attivazione dei geni bersaglio a dosi tollerate e sono rimaste in gran parte nello stato mal ripiegato, sebbene lievi effetti tardivi sulla crescita suggeriscano un recupero funzionale solo parziale.
Cosa significa per i pazienti e per il disegno di farmaci futuri
Per le persone con tumori che portano la mutazione Y220S, questi risultati sono cautamente incoraggianti: rezatapopt può, in linea di principio, ripristinare le funzioni protettive di p53, ma solo a dosi sostanzialmente più elevate, che potrebbero essere difficili da raggiungere in sicurezza nei pazienti. Per Y220N, l’attuale farmaco sembra insufficiente a riparare pienamente p53 in condizioni realistiche. Tuttavia, i modelli strutturali di questo lavoro delineano perché l’attuale progettazione sottoperforma e come le molecole future potrebbero essere aggiustate per coinvolgere tutte e tre le catene laterali mutate senza forzarle in posizioni sfavorevoli. In altre parole, creare un vero farmaco “pan-Y220” per la riparazione di p53 appare sfidante ma realizzabile, e amplierebbe modestamente il numero di pazienti che potrebbero beneficiare di questa strategia emergente di riparare, piuttosto che sostituire, il soppressore tumorale endogeno.
Citazione: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Parole chiave: riattivazione di p53, rezatapopt, mutazione Y220C, medicina di precisione oncologica, stabilizzazione proteica