Clear Sky Science · it
La deubiquitinazione da parte di OTUD4 stabilizza EGFR e attiva la via PI3K/AKT per promuovere l’invasività del carcinoma mammario triplo-negativo
Perché questa ricerca è importante per il carcinoma mammario
Il carcinoma mammario triplo-negativo è una delle forme più difficili da trattare perché manca dei marcatori ormonali e di crescita comunemente bersagliati dai farmaci. Questo studio svela una molecola “protettiva” nascosta che aiuta le cellule tumorali a mantenere attivo un potente interruttore di crescita. Comprendendo questo sistema di supporto invisibile, gli scienziati potrebbero trovare nuovi modi per interrompere i segnali che alimentano la crescita e la diffusione del tumore.
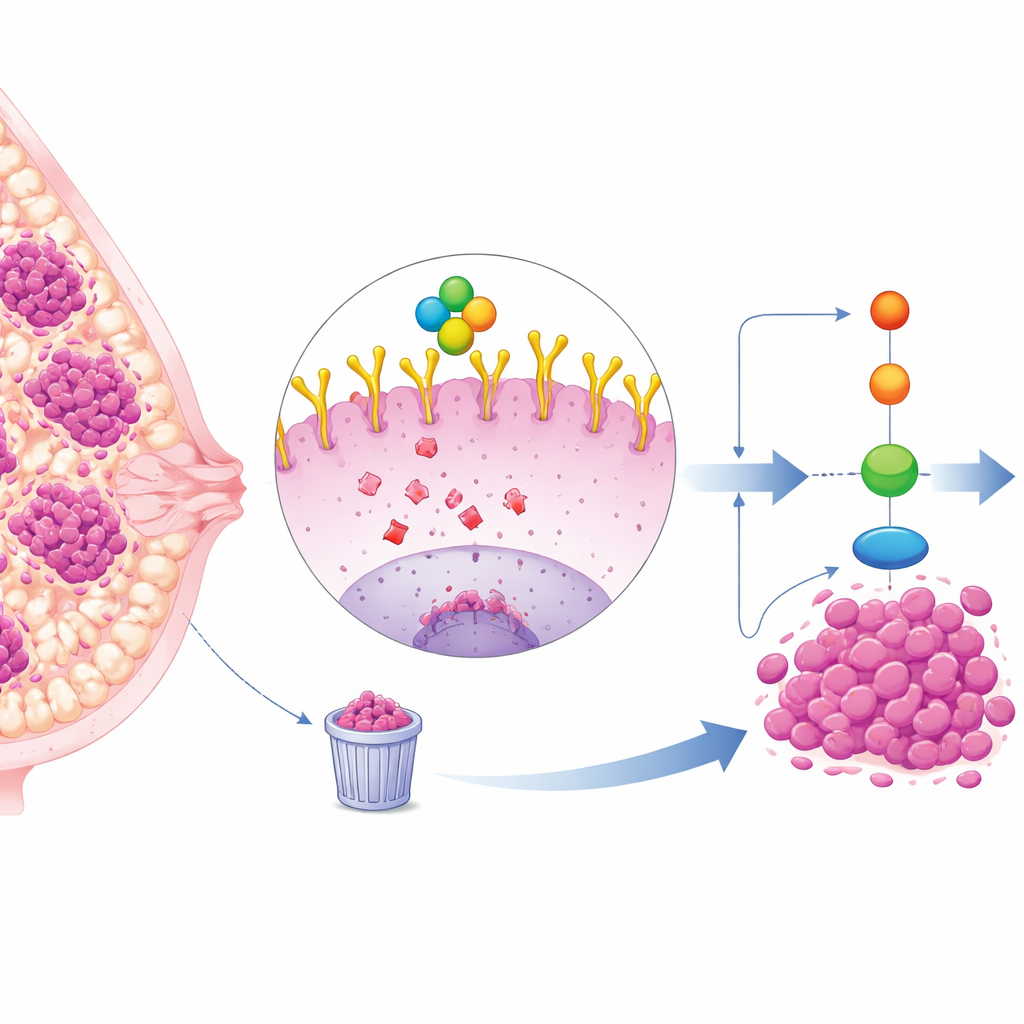
Un sottotipo di carcinoma mammario difficile da trattare
Il carcinoma mammario triplo-negativo (TNBC) rappresenta circa un quarto dei casi di cancro al seno e tende a crescere e metastatizzare più rapidamente rispetto ad altri sottotipi. Poiché le cellule TNBC non esprimono i recettori per estrogeni, progesterone o HER2, le terapie mirate standard sono meno efficaci, lasciando che chemioterapia e chirurgia rimangano le opzioni principali. Molti tumori TNBC, tuttavia, mostrano elevati livelli di una proteina di superficie cellulare chiamata EGFR, che funziona come un’antenna per ricevere segnali di crescita e sopravvivenza. Livelli elevati di EGFR sono associati a prognosi sfavorevole, ma i farmaci che bloccano direttamente EGFR hanno dato risultati deludenti in clinica, suggerendo che esistono livelli più profondi di regolazione.
Alla ricerca di un aiuto nascosto per la crescita tumorale
I ricercatori si sono concentrati su OTUD4, un enzima che rimuove piccoli segnali proteici chiamati ubiquitine da altre proteine. Questi segnali spesso indicano lo smaltimento, marcando le proteine per la degradazione; rimuovendoli si può stabilizzare e proteggere la proteina marcata. Utilizzando ampi database sul cancro e campioni tissutali di pazienti, il gruppo ha mostrato che OTUD4 è presente a livelli più alti nei tumori e nelle linee cellulari TNBC rispetto al tessuto mammario normale. I pazienti i cui tumori esprimevano maggiore OTUD4 tendevano ad avere sopravvivenza peggiore, suggerendo che OTUD4 si comporta come un oncogene, un gene che favorisce la progressione del cancro.
Come OTUD4 rende le cellule tumorali più aggressive
Per testare cosa faccia concretamente OTUD4 nelle cellule TNBC, gli scienziati ne hanno ridotto i livelli in due linee cellulari TNBC ampiamente studiate. Quando OTUD4 veniva silenziato, le cellule tumorali crescevano più lentamente, formavano meno colonie e avevano una minore capacità di migrare in saggi di guarigione di ferite e Transwell, tutti segni di ridotta aggressività. Quando invece OTUD4 veniva sovraespresso, si osservava l’effetto opposto: le cellule proliferavano più rapidamente e migravano con maggiore facilità, rafforzando l’idea che OTUD4 guidi comportamenti maligni. Nei topi, i tumori derivati da cellule prive di OTUD4 crescevano più lentamente e mostravano marcatori ridotti di divisione cellulare e segnali di crescita, confermando questi effetti in organismi viventi.
Uno scudo molecolare che protegge EGFR
Approfondendo il meccanismo, il gruppo ha utilizzato screening di interazione proteica e saggi biochimici per identificare EGFR come partner di legame diretto di OTUD4. Hanno trovato che OTUD4 si attacca a una regione specifica di EGFR e rimuove catene di ubiquitina legate in K48, il tipo di segnale che normalmente marca le proteine per la distruzione da parte del sistema di riciclo cellulare. Quando OTUD4 veniva ridotto, EGFR veniva degradato più rapidamente, mentre l’attività del suo gene rimaneva invariata, mostrando che OTUD4 agisce dopo la sintesi della proteina, non a livello del DNA o dell’RNA. Bloccare il sistema di smaltimento proteico della cellula ristabiliva i livelli di EGFR, sottolineando che il passaggio cruciale è la protezione dalla degradazione. Con EGFR più stabile sulla superficie cellulare, una via di segnalazione interna principale, la via PI3K/AKT/mTOR, rimane attivata, promuovendo crescita e sopravvivenza cellulare.
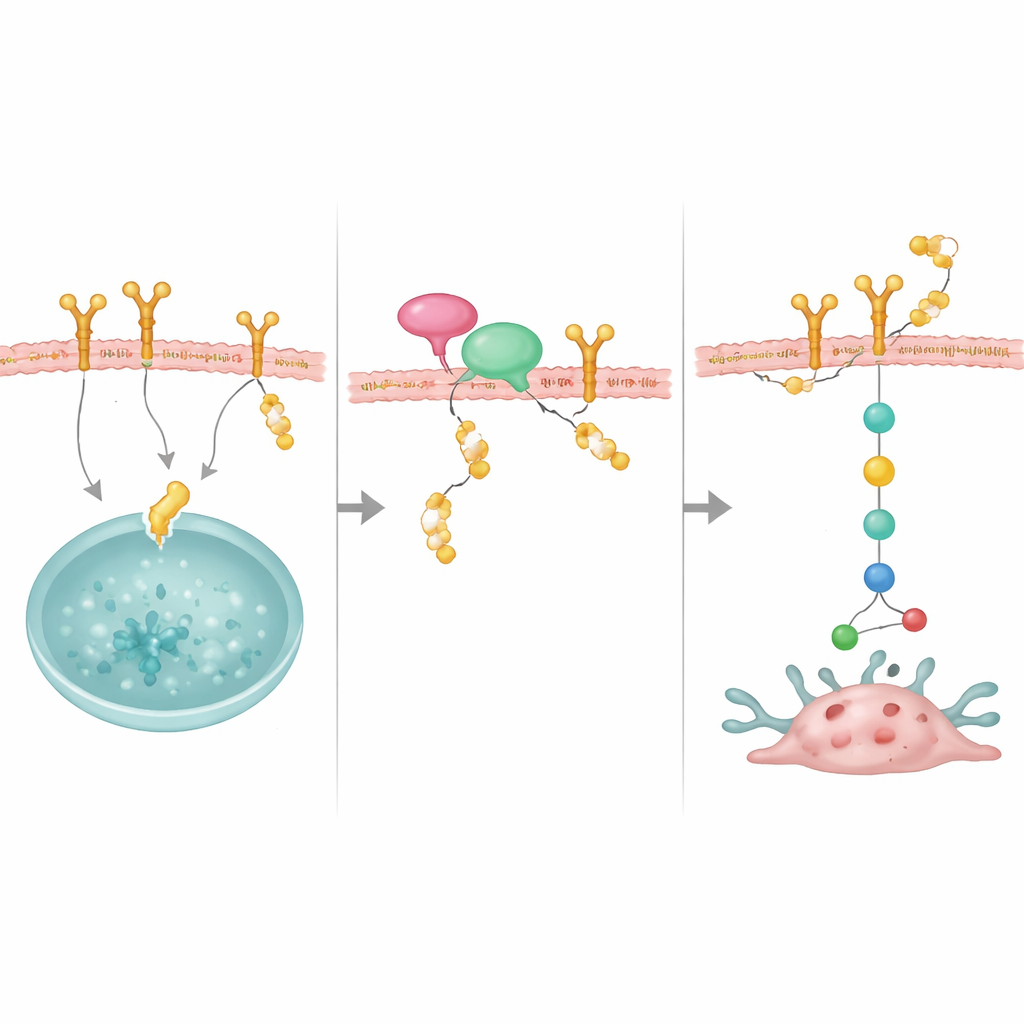
Un adattatore che porta il protettore al suo bersaglio
Lo studio ha anche scoperto un partner importante, NRP1, una proteina di membrana precedentemente collegata a forme aggressive di cancro al seno. NRP1 lega sia OTUD4 sia EGFR e aiuta a posizionare OTUD4 affinché salvi EGFR dalla distruzione. Quando NRP1 veniva ridotta, EGFR diventava meno stabile e i suoi segnali di crescita si indebolivano, anche se i livelli di OTUD4 non cambiavano. La sovraespressione di OTUD4 poteva in parte compensare la perdita di NRP1, suggerendo che NRP1 funge da piattaforma di aggancio che recluta OTUD4 su EGFR. Insieme, queste molecole formano un complesso stabilizzante che mantiene EGFR abbondante sulla superficie cellulare.
Cosa significa per i trattamenti futuri
Svelando come OTUD4 e NRP1 lavorino insieme per proteggere EGFR dalla degradazione, questo studio identifica un nuovo punto di controllo per un segnale di crescita chiave nel carcinoma mammario triplo-negativo. Invece di tentare di bloccare l’attività di EGFR al suo sito attivo, le terapie future potrebbero mirare a interrompere le azioni protettive di OTUD4 o il suo reclutamento da parte di NRP1, abbassando i livelli di EGFR e attenuando la via PI3K/AKT che alimenta la crescita tumorale. Pur chiedendo ulteriori studi per trovare inibitori di OTUD4 sicuri ed efficaci e per comprendere possibili vie di fuga adottate dalle cellule tumorali, i risultati aprono prospettive promettenti per trattamenti più mirati contro questo sottotipo di cancro al seno particolarmente impegnativo.
Citazione: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Parole chiave: carcinoma mammario triplo-negativo, segnalazione EGFR, OTUD4, via PI3K AKT, degradazione proteica