Clear Sky Science · it
La deidrogenasi degli acil-CoA a catena corta avvia la demetilazione e la fuoriuscita di mtDNA per alimentare l’immunità antitumorale nel cancro colorettale
Perché le nostre stesse cellule a volte nascondono il cancro al sistema immunitario
Il cancro colorettale è uno dei tumori più letali al mondo, in parte perché le difese immunitarie dell’organismo spesso non riescono a riconoscerlo e attaccarlo. Questo studio svela un collegamento inatteso tra il modo in cui le cellule tumorali bruciano i grassi, come le loro piccole centrali energetiche (mitocondri) gestiscono il proprio DNA e se il sistema immunitario viene avvisato della presenza del tumore. Tracciando questa catena di eventi, i ricercatori mettono inoltre in luce un composto naturale già noto, l’ipericina, come possibile modo per riattivare l’attacco immunitario nel cancro colorettale.
Un “guardiano” mitocondriale assente nei tumori del colon
Il gruppo ha iniziato cercando in ampi dataset umani e murini geni metabolici che cambiassero in modo coerente nel cancro colorettale. È emerso un enzima in particolare: la deidrogenasi degli acil‑CoA a catena corta, o ACADS, che normalmente aiuta i mitocondri a degradare gli acidi grassi a corta catena. Nei campioni di pazienti e in diversi modelli murini, i livelli di ACADS risultavano marcatamente più bassi nel tessuto tumorale rispetto al colon sano adiacente. Quando gli scienziati riducevano ACADS in cellule di cancro del colon murino, i tumori crescevano più rapidamente e in modo più aggressivo; aumentare ACADS rallentava la crescita tumorale. Topi ingegnerizzati per essere privi di ACADS specificamente nell’epitelio intestinale sviluppavano più tumori e di maggiori dimensioni in un modello chimico di cancro associato a colite, a sostegno dell’idea che ACADS agisca come soppressore tumorale nell’intestino.
Come i tumori spengono i segnali d’allarme immunitari
Questi effetti sulla crescita non potevano essere spiegati semplicemente dalla velocità di proliferazione delle cellule tumorali in coltura, che cambiava poco. Invece, la perdita di ACADS promuoveva la crescita tumorale solo negli animali con sistema immunitario intatto, indicando modifiche nel microambiente tumorale. Analisi a singola cellula di tumori colorettali umani hanno mostrato che i tumori con bassa espressione di ACADS erano circondati da più cellule tumorali e da cellule immunitarie soppressive—come cellule soppressive derivate da mieloide, alcuni macrofagi e cellule T regolatorie—andavano incontro a una riduzione delle cellule T effettrici e delle cellule natural killer. Questo schema indica un “vicinato immunosoppressivo” che protegge il tumore dall’attacco. 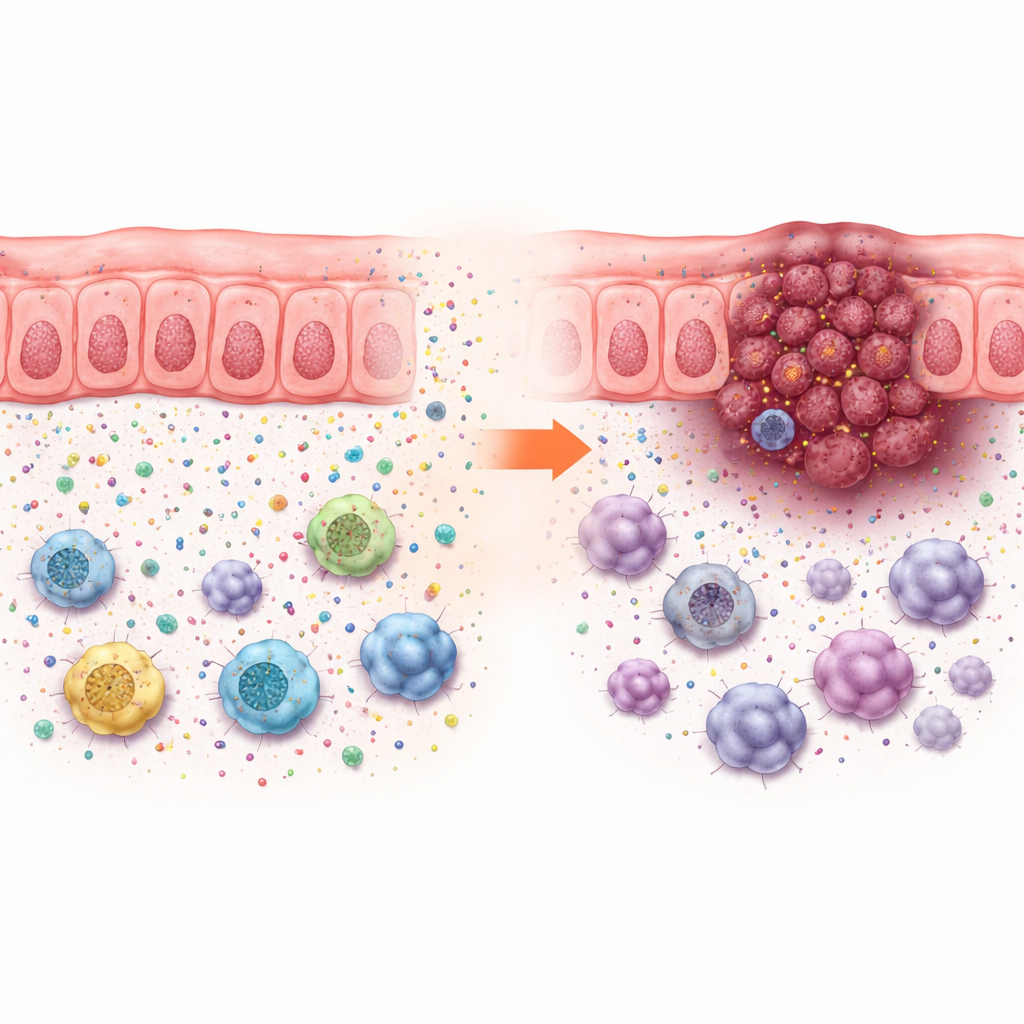
La fuoriuscita di DNA mitocondriale come innesco nascosto
Cosa collega un enzima che brucia grassi a un sensore immunitario del DNA? La risposta risiede nel DNA mitocondriale (mtDNA). Sotto stress, frammenti di mtDNA possono fuoriuscire dai mitocondri nel fluido circostante della cellula, dove cGAS li rileva come segnale di pericolo. I ricercatori hanno mostrato che le cellule tumorali carenti di ACADS avevano meno mtDNA in questo compartimento, pur senza variazioni nel mtDNA totale. Bloccare la fuoriuscita di mtDNA nelle cellule con alti livelli di ACADS spegneva la via cGAS–STING, confermando che questi frammenti di DNA sfuggiti sono l’allarme critico. Sorprendentemente, fattori classici di stress mitocondriale come specie reattive dell’ossigeno, incrementi di calcio e grandi cambiamenti nella morfologia mitocondriale non potevano spiegare completamente la differenza. Lo studio indica piuttosto le “porte” nella membrana mitocondriale e, soprattutto, i marchi chimici sul mtDNA stesso. 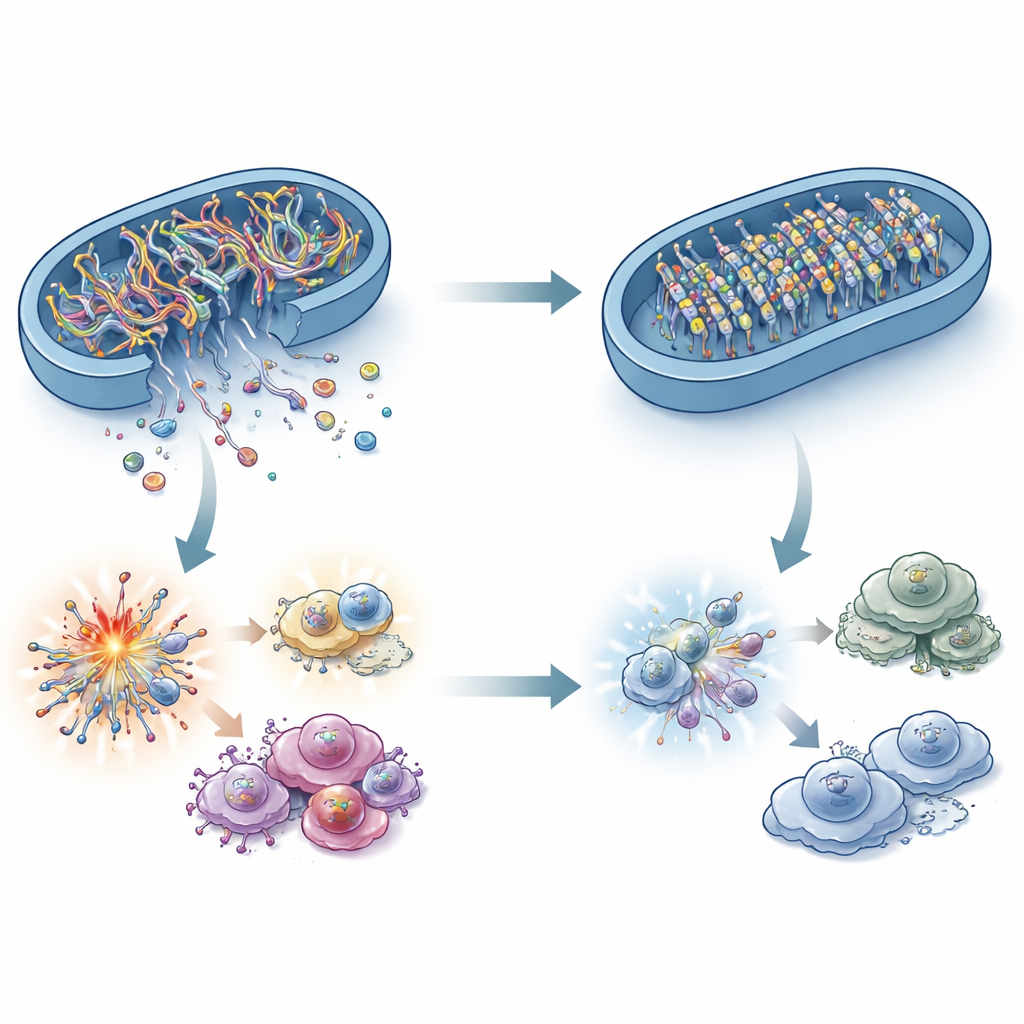
Un partner metilante del DNA che chiude l’allarme dall’interno
Attraverso screening di interazioni proteiche, ACADS è risultato associarsi a una forma dell’enzima di metilazione del DNA DNMT1 che si localizza nei mitocondri. Quando ACADS veniva perso, questo DNMT1 mitocondriale si accumulava, aggiungendo gruppi metile al mtDNA. Questi marchi rendono il mtDNA più stabile e meno incline a rompersi e fuoriuscire. Sovraccaricare le cellule con DNMT1 mitocondriale riduceva la fuga di mtDNA, attenuava la segnalazione cGAS–STING e accelerava la crescita tumorale, mentre bloccare DNMT1 con il farmaco decitabina ripristinava la fuoriuscita di mtDNA e rallentava i tumori privi di ACADS. I campioni dei pazienti rispecchiavano questi risultati: basso ACADS coincideva con alto DNMT1 mitocondriale, segnalazione STING più debole, meno cellule T effettrici, più cellule immunosoppressive e una previsione di risposta peggiore all’immunoterapia con checkpoint.
Riattivare le difese immunitarie con un vecchio composto
Per verificare se questa via potesse essere sfruttata terapeuticamente, i ricercatori hanno usato screening computazionali per cercare molecole che si legassero ad ACADS. Hanno identificato l’ipericina, un pigmento naturale già testato come trattamento attivato dalla luce per alcuni linfomi cutanei. Nelle cellule di cancro colorettale, l’ipericina aumentava i livelli di ACADS, riduceva il DNMT1 mitocondriale, aumentava la fuoriuscita di mtDNA e riattivava la segnalazione cGAS–STING—cambiamenti che dipendevano dalla presenza di ACADS. In modelli tumorali murini e in colture a breve termine di tumori colorettali umani, il trattamento con ipericina ha ridotto le dimensioni dei tumori o ha spostato le cellule immunitarie verso uno stato più attivo e ricco di cellule T. Sebbene siano necessari ulteriori studi prima dell’uso clinico, questi risultati suggeriscono che “riaccendere” farmacologicamente ACADS potrebbe aiutare a convertire un tumore freddo e immunosoppresso in uno più reattivo all’immunoterapia.
Cosa significa questo per i pazienti e i trattamenti futuri
In termini pratici, questo lavoro mostra che alcuni tumori colorettali crescono in parte perché silenziano un enzima mitocondriale che normalmente favorisce la fuoriuscita di minuscoli frammenti di DNA nell’interno della cellula, dove funzionano come segnali per richiamare il sistema immunitario. Permettendo a un partner metilante del DNA di fissare quel DNA mitocondriale al suo posto, i tumori privi di ACADS tengono nascosti questi segnali e sfuggono al riconoscimento immunitario. Ripristinare l’attività di ACADS, per esempio con farmaci simili all’ipericina, potrebbe riaprire questo sistema d’allarme mitocondriale, rafforzare l’immunità antitumorale e migliorare le risposte alle immunoterapie esistenti. ACADS, il DNMT1 mitocondriale e l’attività della via STING potrebbero quindi servire come biomarcatori utili e come bersagli nella ricerca di trattamenti più efficaci per il cancro colorettale.
Citazione: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Parole chiave: cancro colorettale, immunità tumorale, DNA mitocondriale, metabolismo dei lipidi, via cGAS-STING