Clear Sky Science · it
Colpire fused in sarcoma (FUS): una nuova strategia antisenso per trattare la fibrosi polmonare idiopatica
Perché i polmoni cicatrizzati contano
La fibrosi polmonare idiopatica (IPF) è una malattia polmonare inesorabile in cui i delicati alveoli si trasformano lentamente in tessuto cicatriziale rigido, rendendo ogni respiro più difficile. I farmaci attuali possono rallentare questa formazione di cicatrici, ma non possono arrestarla o invertire il processo. Questo studio esplora un nuovo bersaglio chiamato FUS, una proteina che aiuta le cellule a gestire i loro messaggi genetici, e valuta se spegnerla con un filamento progettato di materiale simile al DNA possa attenuare la formazione di cicatrici e favorire la riparazione dei polmoni danneggiati.
Un controllore del traffico cellulare che va fuori strada
FUS è una proteina che normalmente risiede nel nucleo cellulare, dove contribuisce a regolare come l’RNA — la copia operativa dei nostri geni — viene processato e utilizzato. In malattie cerebrali come la SLA, FUS può comportarsi in modo anomalo, uscire dal nucleo, aggregarsi nelle regioni più esterne della cellula e disturbare le funzioni normali. Gli autori si sono chiesti se un simile malfunzionamento potesse guidare la formazione di cicatrici nella IPF. Hanno studiato fibroblasti polmonari — le cellule del tessuto connettivo che depositano materiale cicatriziale — provenienti da pazienti con IPF e da donatori sani. Nelle cellule IPF, i livelli di FUS erano complessivamente più alti e, soprattutto, molto più FUS si trovava nel citoplasma rispetto alle cellule sane. Utilizzando la microscopia elettronica ad alta risoluzione, hanno confermato che questa proteina era anormalmente abbondante fuori dal nucleo, suggerendo che il suo controllo sull’RNA potrebbe essere distorto nei polmoni fibrotici. 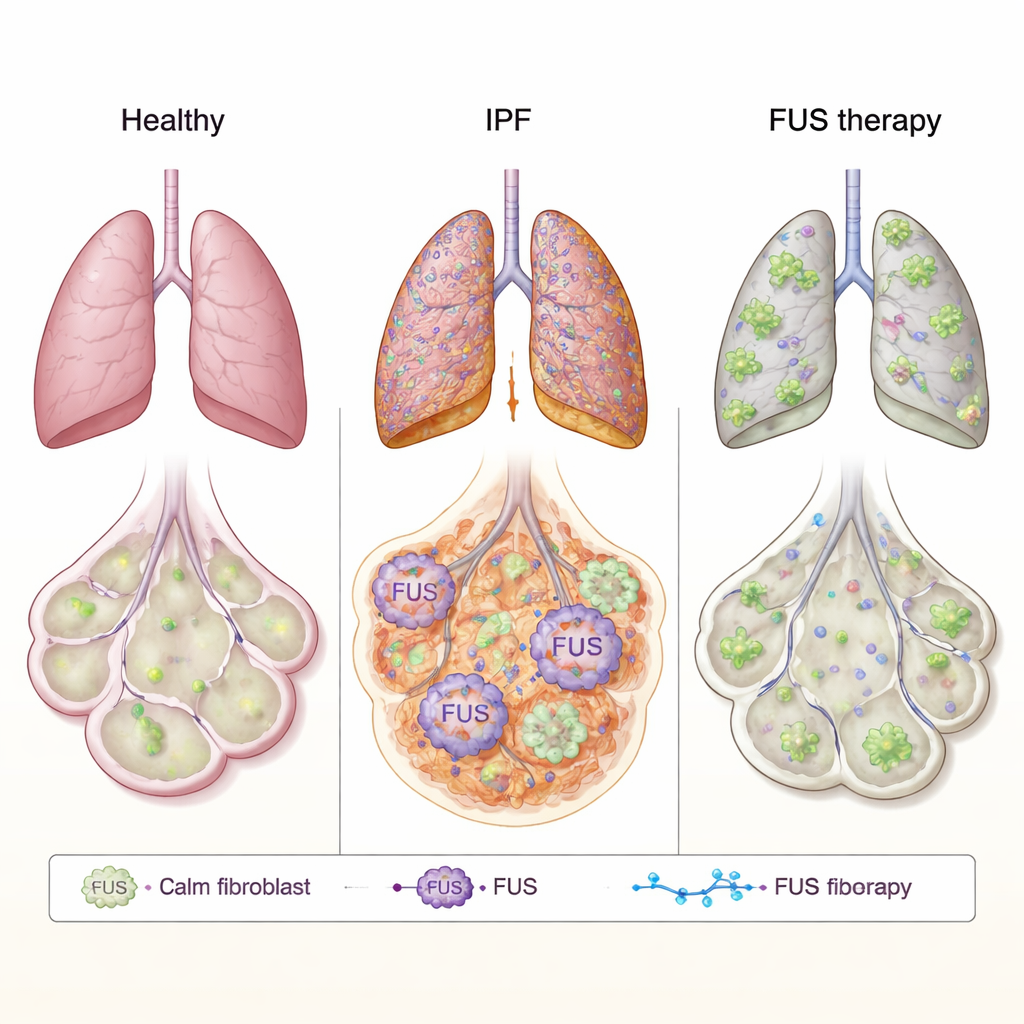
Come FUS alimenta le cellule che formano cicatrici
Per capire cosa fa realmente questa proteina disfunzionale, i ricercatori hanno aumentato l’espressione di FUS in fibroblasti sani e l’hanno ridotta in fibroblasti IPF. Un eccesso di FUS spingeva le cellule sane a dividersi più rapidamente, mentre la riduzione di FUS nelle cellule IPF rallentava la loro crescita e il loro movimento — due comportamenti centrali nella formazione di cicatrici. Il gruppo ha poi usato una tecnica che “congela” le associazioni proteina–RNA e legge quali RNA sono legati a FUS. Nei fibroblasti IPF, FUS è risultato legato a molti messaggi genetici che promuovono la fibrosi, inclusi quelli che codificano per il collagene, fattori di crescita come TGF‑β e segnali infiammatori. In altre parole, FUS agiva come un hub che connetteva un’intera rete di messaggi pro‑cicatrizzazione.
Silenziare il segnale con un farmaco di precisione
Lo studio ha testato un oligonucleotide antisenso chiamato ION363 — un breve filamento chimicamente modificato progettato per legarsi all’RNA di FUS e innescarne la distruzione. Quando i fibroblasti IPF sono stati trattati con ION363, i livelli di FUS sono diminuiti, le cellule hanno rallentato proliferazione e migrazione e i geni chiave per la costruzione della cicatrice si sono spenti. Importante, questo effetto non dipendeva dall’uccidere le cellule o dall’indurle a uno stato di senescenza; piuttosto, sembrava ripristinare il loro comportamento. Quando lo stesso trattamento è stato applicato a fette sottili di tessuto polmonare IPF mantenute vitali in laboratorio, grandi gruppi di geni legati alla matrice extracellulare, all’infiammazione e al rivestimento epiteliale anomalo sono stati attenuati, mentre sono aumentati i geni associati alla produzione di surfattante e alla funzione alveolare sana. Il trattamento ha anche ridotto la colorazione del collagene e aumentato i marcatori delle cellule di superficie polmonare funzionali, suggerendo uno spostamento dalla cicatrizzazione verso la riparazione.
Aiutare la rigenerazione degli alveoli danneggiati
Poiché le piccole cellule che rivestono gli alveoli, note come cellule alveolari di tipo II, sono cruciali per la riparazione polmonare, i ricercatori hanno costruito “alveolosfere” tridimensionali a partire da cellule di pazienti per imitare unità polmonari in miniatura. Nelle colture derivanti da pazienti IPF, queste strutture normalmente sopravvivono male. Con il trattamento ION363, si sono formate più alveolosfere, sono cresciute di più e hanno mostrato maggiore attività lisosomiale — un segno di rinnovamento attivo. Colorazioni dettagliate hanno rivelato più cellule con marcatori di cellule mature scambianti gas, indicando che silenziare FUS non solo placava i fibroblasti ma incoraggiava anche l’epitelio danneggiato a ricostruire una superficie più sana. 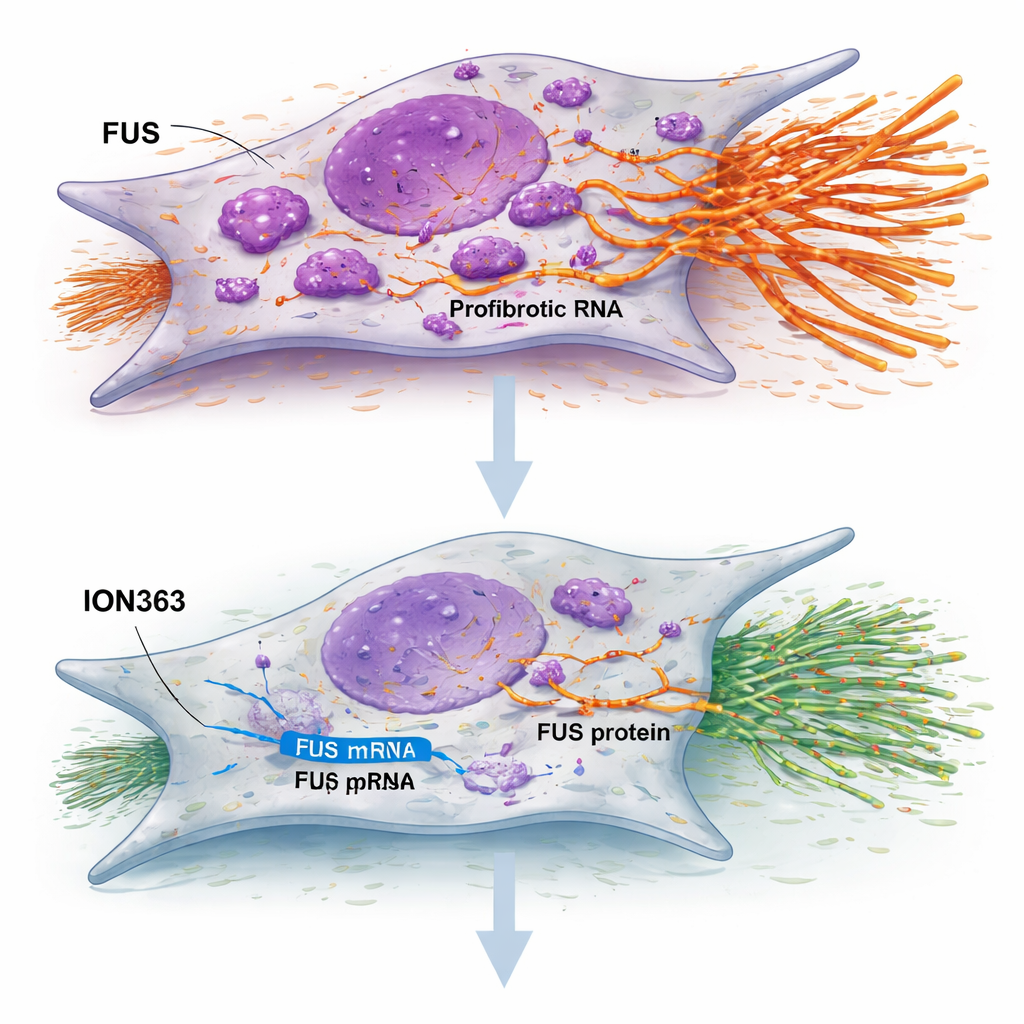
Cosa potrebbe significare per i pazienti
Nel complesso, il lavoro dipinge FUS come un interruttore maestro nella IPF che collega fibroblasti iperattivi nella formazione di cicatrici con il fallimento della riparazione dei delicati alveoli. Riducendo l’espressione di FUS con un farmaco antisenso mirato, i ricercatori sono riusciti a ridurre i programmi genetici profibrotici, attenuare l’accumulo di collagene e promuovere la rigenerazione in modelli polmonari derivati da pazienti. Sebbene questo approccio sia ancora a livello di laboratorio e richieda test approfonditi in modelli animali e studi clinici, suggerisce che un giorno la IPF potrebbe essere trattata non solo rallentando la fibrosi, ma riequilibrando direttamente i programmi cellulari che controllano il danno e la riparazione polmonare.
Citazione: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Parole chiave: fibrosi polmonare idiopatica, oligonucleotide antisenso, proteina FUS, fibrosi polmonare, riparazione alveolare