Clear Sky Science · it
Troncamento parziale del dominio C-terminale di PTCH1 nel cancro promuove la tumorigenesi mediante attivazione non canonica di un circuito GLI-PI3K
Perché una piccola modifica proteica conta nel cancro del colon
Il cancro del colon di solito nasce da un accumulo lento di errori genetici. Questo studio si concentra su una modifica sorprendentemente piccola in una proteina di superficie chiamata PTCH1 e mostra come il taglio di parte della sua coda possa aiutare le cellule tumorali del colon a proliferare più rapidamente, a diffondersi più facilmente e potenzialmente a resistere ad alcuni farmaci esistenti. Comprendere questo interruttore di crescita nascosto potrebbe aprire la strada a trattamenti nuovi e più mirati per una sottopopolazione di pazienti.
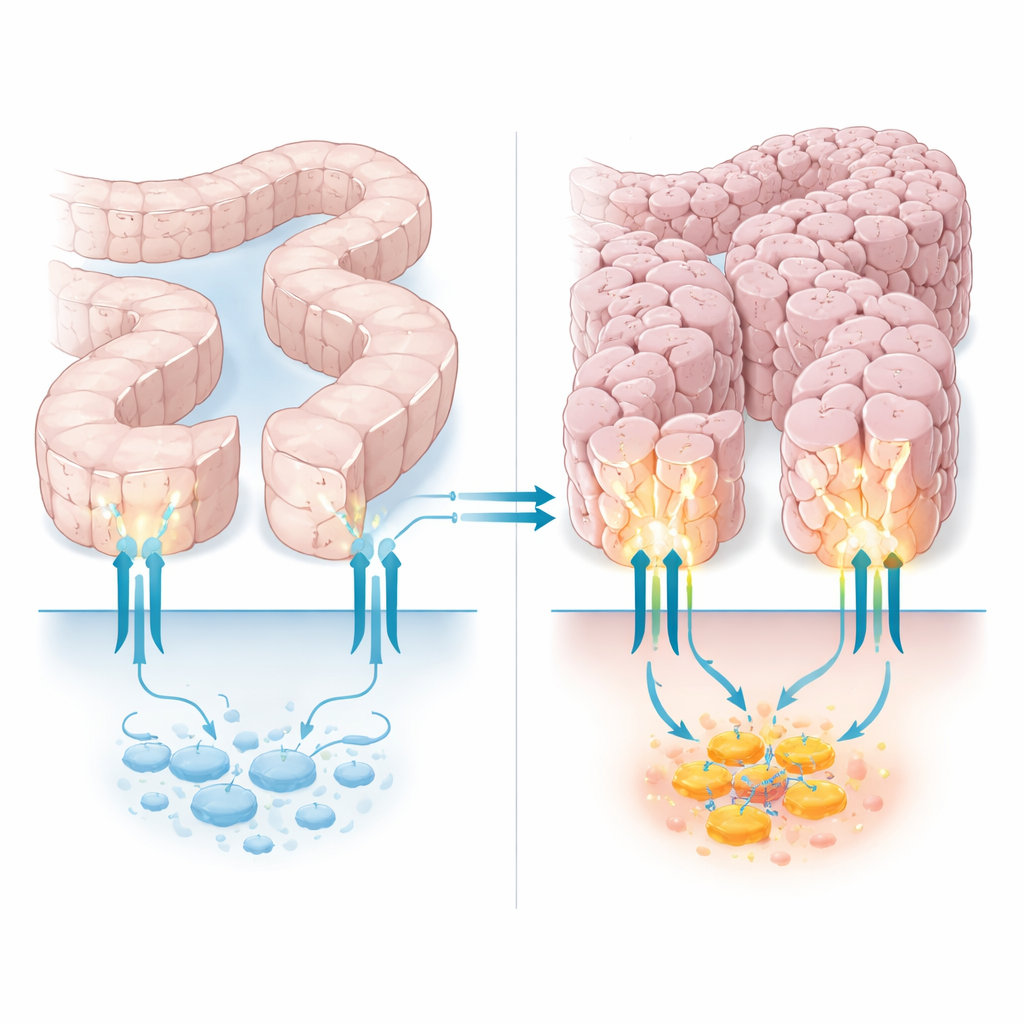
Il guardiano della cellula con un lavoro nascosto
PTCH1 è meglio conosciuto come il guardiano della via Hedgehog, una linea di comunicazione che le cellule usano durante lo sviluppo e la riparazione tissutale. Nel suo ruolo classico, PTCH1 mantiene sotto controllo una proteina partner, Smoothened, regolando così una famiglia di regolatori del DNA chiamati GLI. Ma PTCH1 ha anche una lunga coda flessibile che penetra all’interno della cellula, fungendo da piattaforma di ancoraggio per altre proteine che influenzano la morte cellulare, il riciclo dei componenti cellulari e altro. Lavori precedenti hanno mostrato che alcuni tumori del colon, dello stomaco e dell’utero presentano mutazioni che recidono parte di questa coda interna. Quelle mutazioni non sembravano interrompere l’interruttore Hedgehog classico ma rendevano le cellule tumorali più resistenti allo stress, suggerendo che quel segmento di coda contribuisce silenziosamente al ruolo oncosoppressore di PTCH1.
Ingegnerizzare cellule tumorali per testare l’impatto
Per capire cosa fanno davvero queste mutazioni che accorciano la coda, i ricercatori hanno usato l’editing genetico CRISPR/Cas9 per ricrearle in una linea cellulare di cancro del colon. Hanno confrontato due cloni modificati, ciascuno con un diverso troncamento nella coda di PTCH1, con cellule altrimenti identiche che portavano PTCH1 normale. Le cellule mutate si dividevano più velocemente, formavano molte più colonie e sopravvivevano anche quando dovevano crescere senza attaccarsi—un comportamento associato alla capacità di metastatizzare nell’organismo. Impiantate in topi, le cellule con la coda troncata produssero tumori molto più grandi in poche settimane, con più cellule in fase di divisione. È importante notare che le cellule editate continuavano a produrre PTCH1 e conservavano la sua funzione di controllo principale, a dimostrazione che l’aggressività aggiuntiva deriva dalla perdita delle funzioni interne specializzate della coda e non dalla rimozione completa di PTCH1.
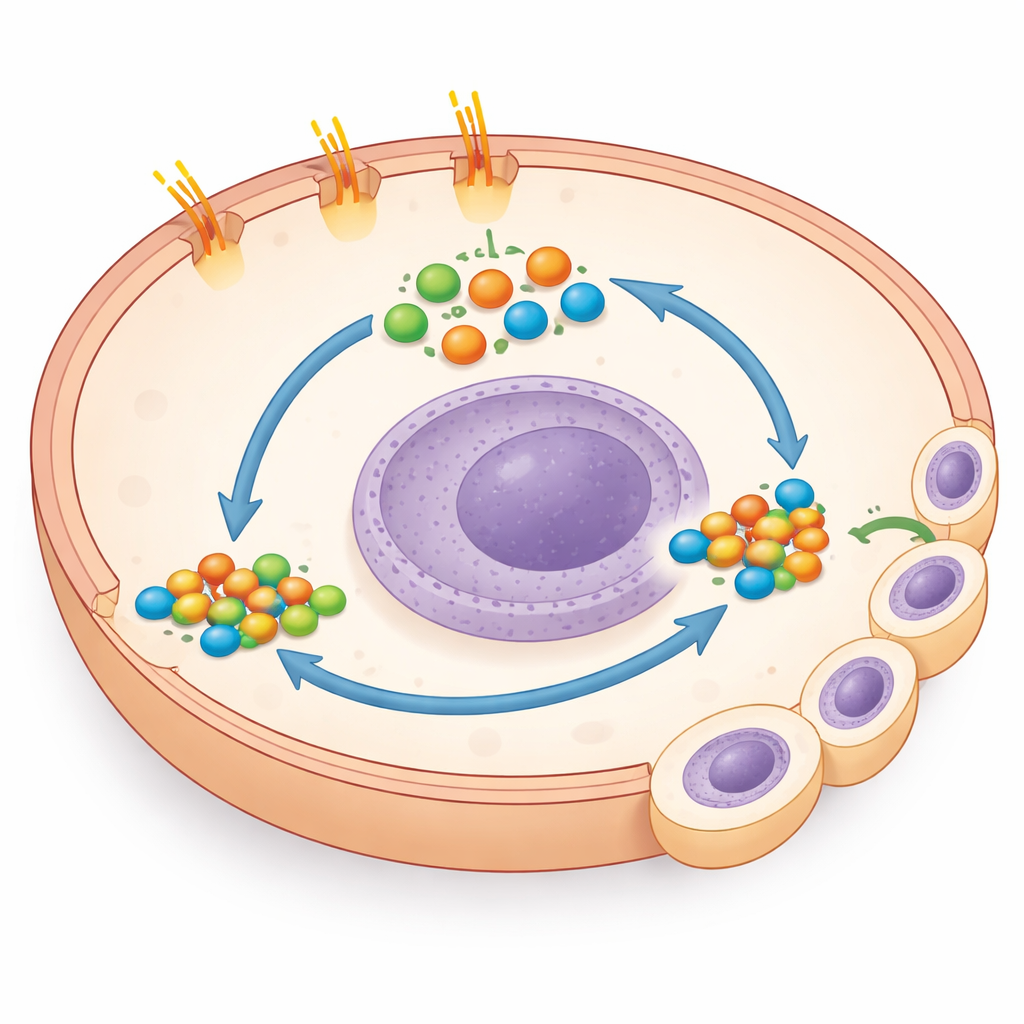
Una scorciatoia sorprendente verso un potente interruttore di crescita
Analizzando la biologia sottostante, il gruppo fece una scoperta inaspettata: le cellule con la coda troncata mostravano livelli fortemente aumentati di GLI1 e GLI2, fattori chiave di programmi genici che promuovono crescita e sopravvivenza. Normalmente, l’attività di GLI aumenta quando Smoothened viene liberato, ma bloccare Smoothened qui non aveva effetto. Invece, bloccare direttamente GLI con una piccola molecola, o abbassare GLI1 con strumenti genetici, riduceva nettamente la crescita delle cellule mutate in coltura e anche in altre linee tumorali del colon che naturalmente presentano mutazioni nella coda di PTCH1. Questo dimostrava che la perdita della coda attiva GLI tramite una via “non canonica” che bypassa l’interruttore Hedgehog abituale, e che le cellule tumorali diventano fortemente dipendenti da questa scorciatoia per il loro comportamento aggressivo.
Molte vie di crescita si attivano, ma una domina
Sequenziando l’RNA delle cellule, i ricercatori hanno trovato migliaia di geni la cui attività cambiava quando la coda di PTCH1 veniva troncata. Molti appartenevano a circuiti tumorali ben noti, inclusi quelli controllati dal recettore del fattore di crescita epidermico (EGFR), da Ras e da sistemi di segnalazione che regolano il metabolismo cellulare e proprietà simili a quelle staminali. Le cellule mutate mostravano maggiore attività di EGFR e dei suoi ligandi e un’aumentata attivazione in due importanti vie a valle: MAPK e PI3K/Akt. Tuttavia, quando gli scienziati bloccarono EGFR o il suo ramo MAPK, le cellule mutate rallentavano solo parzialmente. Al contrario, basse dosi di inibitori della PI3K ne limitarono fortemente la crescita e la formazione di colonie e ridussero i livelli di GLI1, indicando la via PI3K/Akt come partner critico in questo nuovo meccanismo di attivazione di GLI.
Un circuito auto-rinforzante che alimenta la crescita tumorale
Ulteriori esperimenti rivelarono un ciclo di retroazione: il troncamento della coda di PTCH1 aumenta l’attività di GLI; GLI, a sua volta, mantiene alta la segnalazione PI3K/Akt; e PI3K/Akt contribuisce a stabilizzare e attivare GLI. Interrompere sia GLI che PI3K spezzava questo circuito e privava le cellule mutate del loro vantaggio proliferativo, mentre aumentare semplicemente PI3K/Akt non poteva superare un blocco diretto di GLI. Le cellule mostravano inoltre una riduzione dell’attività di PKA, un enzima che normalmente marca le proteine GLI per l’inattivazione, il che probabilmente sposta ulteriormente l’equilibrio verso i programmi guidati da GLI.
Cosa potrebbe significare per il trattamento futuro
Per i pazienti, il messaggio chiave è che alcuni carcinomi del colon presentano mutazioni nella coda di PTCH1 che silenziosamente cablano un circuito di retroazione positivo GLI–PI3K, aiutando i tumori a crescere ed eludere farmaci che prendono di mira l’interruttore Hedgehog più familiare o la via EGFR–MAPK. Questi tumori potrebbero invece risultare particolarmente vulnerabili a terapie che bloccano direttamente GLI o colpiscono PI3K/Akt. Il lavoro suggerisce che il sequenziamento di PTCH1 nei tumori del colon—soprattutto in quelli del colon destro, dove tali mutazioni sono più frequenti—potrebbe aiutare a identificare pazienti che potrebbero beneficiare di strategie mirate a PI3K o GLI, trasformando un sottile accorciamento proteico in un utile indizio terapeutico.
Citazione: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Parole chiave: cancro del colon, segnalazione Hedgehog, mutazioni di PTCH1, fattori di trascrizione GLI, via PI3K Akt