Clear Sky Science · he
הביטוי הספציפי לגידול של HORMAD1 מחריג עיכוב מיטוטי ומגביר רגישות למעכבי קינאזות מיטוטיות
מדוע זה חשוב לטיפול בסרטן
כאשר התאים שלנו מתחלקים, הם מסתמכים על בדיקות בטיחות מורכבות כדי להעביר את מערך הכרומוזומים הנכון. הסרטן לעיתים חוטף או מחליש את מערכות ההגנה הללו, מה שמוביל לגנום כאוטי שמזין את המחלה וגם מעצב את תגובת הגידולים לתרופות. המחקר הזה חושף כיצד חלבון לא שגרתי בשם HORMAD1, שנמצא בדרך כלל פעיל רק בתאי רבייה, נדלק מחדש ברבים ממקרי סרטן שד אגרסיביים ובגידולים אחרים. על ידי פגיעה עדינה בנקודת בדיקה מרכזית של חלוקת התא, HORMAD1 מגדיל את חוסר היציבות בתאי הסרטן — אך גם עושה אותם פגיעים מבחינה יוצאת דופן לסוג חדש של תרופות ניסיוניות.
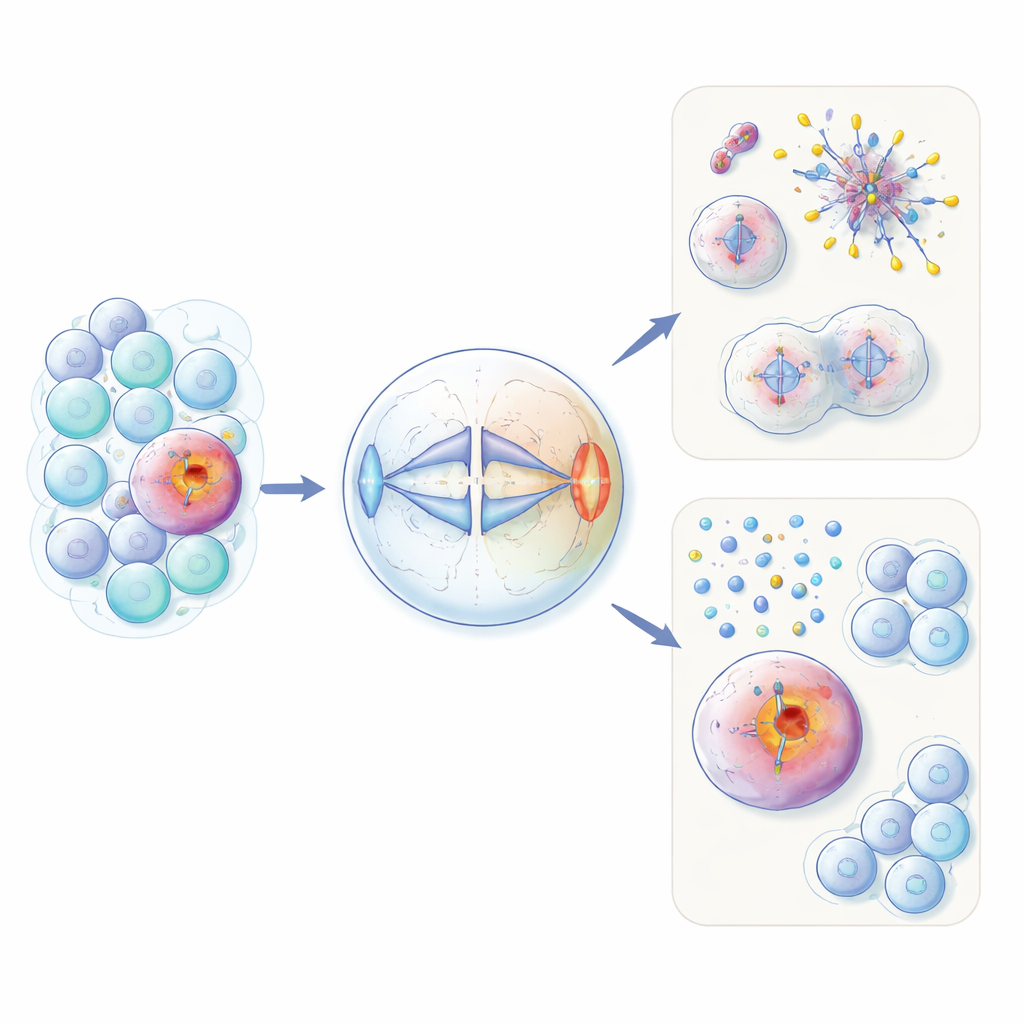
חלבון פוריות שגוי במקומו בתאי סרטן
HORMAD1 מופיע בדרך כלל רק בתאי נבט, שם נוצרים הביציות והזרעים. שם הוא מסייע בניהול שחלוף ה-DNA ובבקרת איכות במהלך סוג מיוחד של חלוקות בשם מיוזה. המחברים מראים שבכ־60% ממקרי סרטן השד משולש-שלילי — ובתתי קבוצות של סוגי גידולים נוספים — החלבון הזה נדלק בצורה לא מתאימה. באמצעות תאים שאינם סרטניים מהונדסים וקווי תאי סרטן, הם מצאו כי ביטוי עודף של HORMAD1 מופרע מהפרדה שווה של הכרומוזומים במהלך חלוקת התא הרגילה. תאים שמבטאים HORMAD1 פיתחו יותר כרומוזומים מאוחרים (lagging chromosomes), כרומוזומים עודפים או חסרים (אנתפלואידיה), ו"מקרו-גרעינים" קטנים המכילים DNA — כל סימנים של כאוס גנומי הנצפה בסרטנים אגרסיביים.
כיצד בדיקות הבטיחות של חלוקת התא פועלות בדרך-כלל
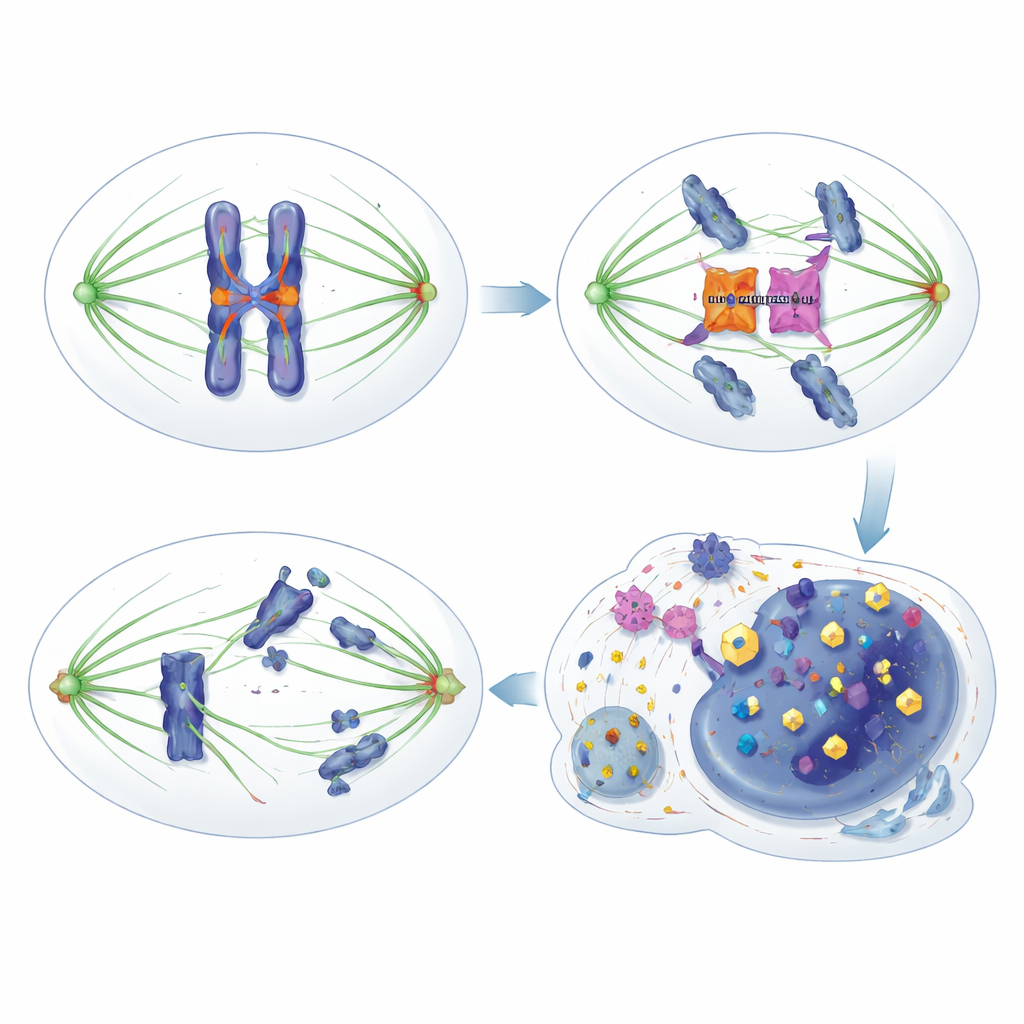
כדי להתחלק נכון, התא בונה כישור של סיבי מיקרוטובולים שמתחברים לכל כרומוזום. מערכת השגחה המכונה נקודת הביקורת להרכבת הכישור פועלת כמו בלם רגיש למתח: אם כרומוזום כלשהו אינו מחובר כראוי, הבלם חוסם את ההתקדמות ומונע הפרדה עד שהשגיאות תוקנו. כמה אנזימים שנקראים קינאזות מיטוטיות, כולל MPS1, Aurora B ו-BUB1, מסייעים לחוש חיבורים לקויים ולקדם "תיקון שגיאות" כדי שכל תא בת יקבל את מערך הכרומוזומים הנכון. שיבוש של מערכת זו יכול גם לזרז התפתחות סרטן וגם ליצור חולשות ספציפיות שניתן למקד בתרופות.
HORMAD1 מחליש את הבלם בשקט
החוקרים גילו ש-HORMAD1 מערער את הבלם הזה באופן עדין אך משמעותי. במקום להפריע למרכיבי נקודת הביקורת הקלאסיים כמו חלבון ה-HORMA MAD2L1, HORMAD1 נקשר ישירות לקינאזת Aurora B. בדרך כלל Aurora B משתפת פעולה עם חלבון נוסף, INCENP, כדי להיות פעילה במלואה ולזרז שינויים חלבוניים במרכזוני הכרומוזומים וקינטוכורים — אתרים חיוניים על הכרומוזומים בהם מתחברים סיבי הכישור. כשה-HORMAD1 נוכח בתאי גידול מתחלקים, הוא מתחרה עם INCENP על ההיקשרות ל-Aurora B, מקטין את שיתוף הפעולה ביניהם ומחליש את פעילות Aurora B. כתוצאה מכך, אותות פוספורילציה טיפוסיים של Aurora B על מספר מטרות נחלשים, תיקון השגיאות פחות יעיל, ונקודת הביקורת נעשית "דולפת": תאים יוצאים מהמִיטוֹז מוקדם מדי, אפילו כשחיבורים לקויים נשארים, מה שמוביל להפרדה שגויה של כרומוזומים וחוסר יציבות גנומית.
מחולשה להזדמנות טיפולית
מכיוון ש-HORMAD1 משתק חלקית את Aurora B ושמירת הגבולות הקשורות, תאי הסרטן נשארים ברי-קיום במידה מסוימת אך תלויים מאוד בפונקציה שנותרה של קינאזות מיטוטיות כדי לשרוד חלוקות חוזרות ולקויות. הצוות בחן זאת באמצעות חשיפת תאים חיוביים ל-HORMAD1 ותאים שליליים ל-HORMAD1 למעכבים ניסיוניים של MPS1, Aurora B ו-BUB1. במגוון מודלים, הביטוי של HORMAD1 הפך את התאים לרגישים יותר משמעותית לתרופות אלה, והקטין במידה דרמטית את יכולתם להתרבות או ליצור מושבות. דיכוי גנטי של BUB1 היה קטלני במיוחד רק בנוכחות HORMAD1, חשיפת תלות סלקטיבית חזקה. במודלים של עכברים עם גידולים משולש-שליליים שמקורם בחולים, אלה עם רמות גבוהות של HORMAD1 הצטמצמו או גדלו לאט יותר כאשר טופלו בניסוח ננו-חלקיקים של מעכב Aurora B, בעוד גידולים שליליים ל-HORMAD1 עמדו ברובם בעמידות לאותו טיפול.
מה זה אומר עבור החולים
עבור צופה שאינו מומחה, HORMAD1 פועל כסכין בעל שתי חודרים בסרטן: הוא דוחף תאי גידול לכאוס כרומוזומלי גדול יותר, דבר שיכול להניע את המחלה, אך בכך גם הופך אותם לתלויים ומתמוטטים להגן עליהם על ידי מספר קטן של מנגנוני שמירה שנותרו. המחקר מראה שהחלבון הזה של הפוריות מחליש נקודת ביקורת מרכזית על ידי הסטת Aurora B, ומשאיר גידולים חיוביים ל-HORMAD1 פגיעים במיוחד לתרופות שמכוונות ל-Aurora B, MPS1 או BUB1. מאחר ש-HORMAD1 נעדר ברוב רקמות הגוף התקינות אך נוכח בתת-קבוצה ברורה של גידולים, הוא יכול לשמש כסמן ביולוגי לזיהוי חולים שסביר שייהנו ממטיפולים אלה במעכבי קינאזות מיטוטיות בהתפתחות, ובכך לפתוח אפשרויות טיפול ממוקדות חדשות לסרטנים שקשים לטיפול כמו סרטן השד המשולש-שלילי.
ציטוט: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
מילות מפתח: HORMAD1, סרטן השד משולש-שלילי, חוסר יציבות כרומוזומלית, קינאזת Aurora B, מעכבים של נקודת הביקורת המיטוטית