Clear Sky Science · he
פולימרים פרוטאומימטיים הטרוביפונקציונליים להידרדרות ממוקדת של MYC ו-KRAS
כלים חדשים להפלת החלבונים הקשים ביותר של הסרטון
רבים מהחלבונים המסוכנים שמניעים סרטן, כמו MYC ו-KRAS, תויגו במשך זמן רב כ"לא ניתנים לתרופה" מכיוון שמולקולות תרופתיות מתקשות להיאחז בהם. המחקר חושף סוג חדש של חומר רך וסינתטי — פולימרי HYDRAC — שיכול לתפוס חלבונים חלקלקים אלה ולשלוח אותם למערכת הסילוק של התא. לקוראים, העבודה מציעה הצצה לאופן שבו כימיה וננוטכנולוגיה עשויות לפתוח אפשרויות טיפול עבור סרטן שהתנגד לטיפולים מסורתיים.
מעגן גמיש במקום כדור יחיד
מרבית התרופות הממוקדות בסרטן הן מולקולות קטנות שמתאימות לכיסים על פני שטח החלבון, בדומה למפתח במנעול. אך חלבונים כגון MYC נוטים להיות רכים וללא כיסים מתאימים, ו-KRAS לעתים מקרבל בדרכים שמנטרלות תרופות קלאסיות. המחברים תכננו במקום זאת פולימרים ארוכים בדמות שרשרות של יחידות חוזרות. לאורך השרשרות הם צירפו שני סוגי מרכיבים: מקטעים קצרים הקשורים לקיבוע חלבונים שמזהים מטרה כמו MYC או RAS, ומקטעי "דגרון" שמגייסים את מכונת הסילוק של התא. מכיוון שהעתקים רבים של כל מרכיב מעטרים את אותה שרשרת, מולקולת HYDRAC בודדת יכולה להתפשט ולגעת במספר חלבונים ואנזימים בו־זמנית — דבר שקשה להשיג עם מולקולת תרופה קשיחה ויחידה.
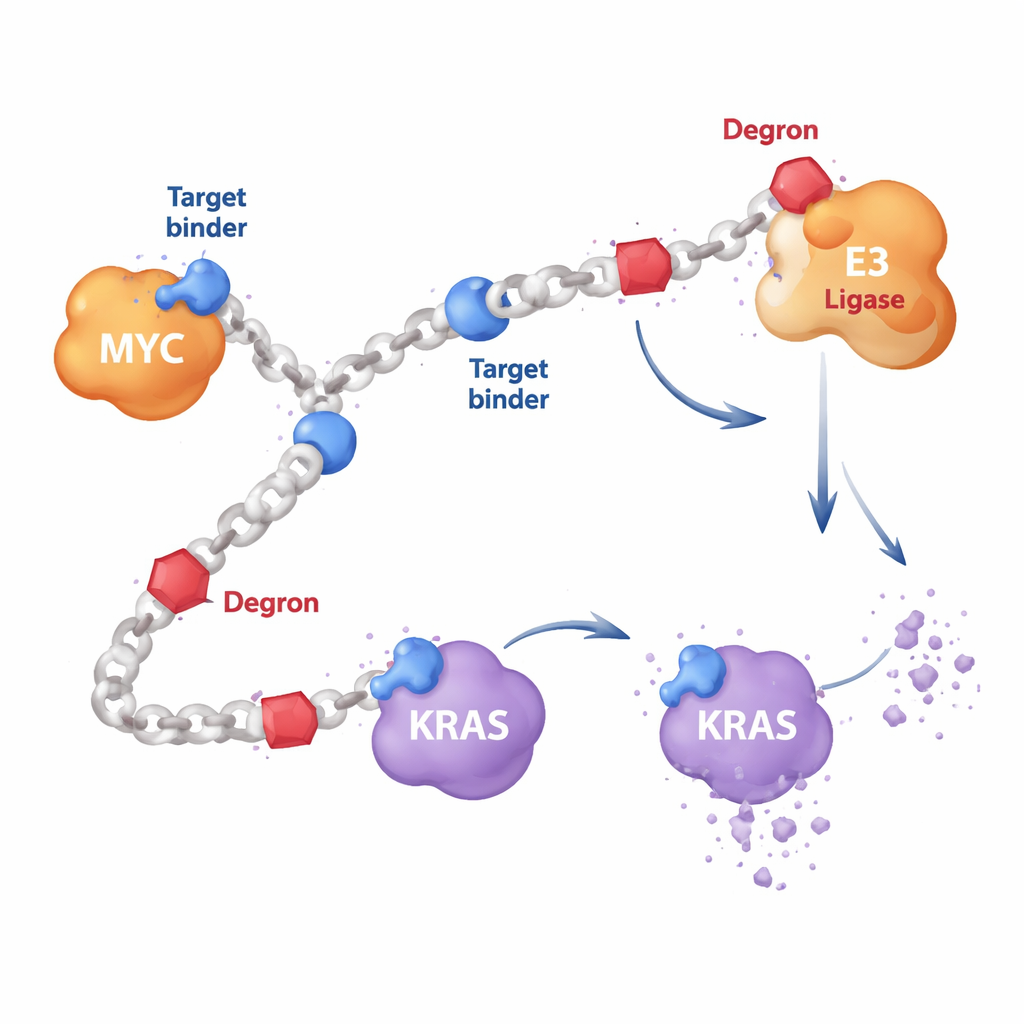
ללמד תאים ללעוס את MYC
כניסוי ראשון, החוקרים התמקדו ב-MYC, מתג על מרכזי שמניע גדילה במגוון סרטן אך התמודד עם התנגדות ישירה שנים רבות. הם בנו פולימרי HYDRAC שהציגו פפטיד ידוע הקושר MYC לצד מוטיף דגרון פשוט שמסמן חלבונים להשמדה על ידי הפרוטאוזום של התא, המגרסה העיקרית של חלבונים. בניסויים בצינור מבחנה, פולימרים אלה התקפלו לצורות קומפקטיות הדומות לחלבונים וקשרו חזק ל-MYC אך לא לחלבונים לא קשורים. בתאים סרטניים, ה-HYDRACs חדרו בקלות, שיבשו תכניות גנטיות הנשלטות על ידי MYC והפעילו מוות תאי — השפעות שתלויות בנוכחות שני מרכיבי המטרה והדגרון על אותה שרשרת פולימרית.
מתרבית תאים לכווץ גידולים
בתוך תאים, טיפול ב-HYDRAC גרם לירידה חדה ברמות החלבון MYC מבלי לצמצם את רמות ה-RNA של MYC, מה שמעיד על השמדה אמיתית ולא כיבוי פשוט של הביטוי. חסימת הפרוטאוזום או אנזימים מרכזיים שמפעילים מסלולי דגרדציה מסוימים הצילה את רמות ה-MYC, והראתה שהפולימרים פועלים על ידי הפניית מערכות הסילוק של התא. ניתוח פרוטאומי בכל קנה מידה חשף שמעט מאוד חלבונים אחרים הושפעו, מה שמעיד על בחירה מרשימה. במודלים עכבריים של גידולים המונעים על ידי MYC, HYDRACs מסומנים בפלואורסציה הצטברו באופן מובהק בגידולים לאחר הזרקה ונשארו שם למשך ימים. מתן חוזר האט את גדילת הגידול ללא ירידה משמעותית במשקל או פגיעה ברקמות גלויה, ודגימות גידול הראו פחות תאים מחלקים ויותר סימנים של מוות תאי מתוכנת.
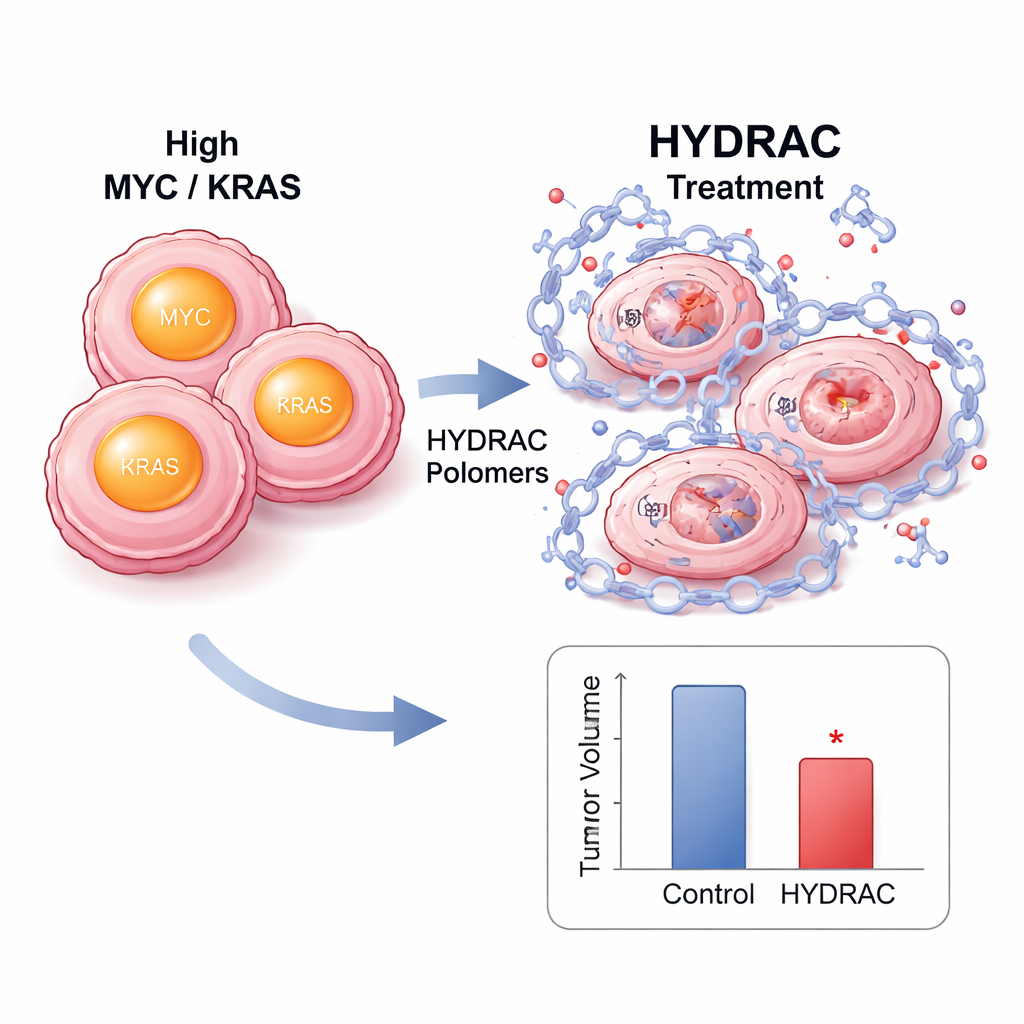
פלטפורמה מודולרית לרב־מטרות
אחת החוזקות של שיטת HYDRAC היא שצידי השרשרת ניתנים להחלפה כמו חלקים ניתנים להחלפה. הצוות החליף את הדגרון המקורי ברכיבי גיוס אחרים שמפנים לאנזימים תאיים שונים, כולל כאלה שמוכרים בזכות הקשר לתרופת התלידומיד. כל גרסה הפחיתה את MYC רק כאשר האנזים המיועד היה נוכח ותפקודי, מה שאישר שניתן לכוון את הפולימרים לשימוש בדרכי סליקה תאיות שונות. כדי לבדוק הכללה, החוקרים בנו אחר כך HYDRACs שמטרתם RAS באמצעות פפטיד שמכיר חלבוני RAS. מבנים אלה הרסו בהצלחה KRAS מוטנטי בשתי שורות תאים סרטניות שונות, מרמזים על פוטנציאל "פאן-KRAS" שאינו תלוי במוטציה ספציפית — צעד חשוב בסרטן שבו משתלבים וריאנטים רבים של KRAS.
מדוע זה חשוב לטיפול בסרטן בעתיד
העבודה מציגה את HYDRACs ככיתה חדשה של חומרים תכנתיים שלא רק חוסמים חלבונים בעייתיים — הם מסייעים לתאים למחוק אותם. על ידי שילוב רבות של יחידות מטרה ודגרדציה על פולימר גמיש, HYDRACs עוקפים את מגבלות העיצוב של תרופות מולקולות קטנות וקבוצות PROTAC, שלרוב יכולות לשאת רק יחידה אחת מכל סוג. למרות שעדיין נדרש הרבה לפני שהחומרים הללו יגיעו לקליניקה, התוצאות במודלים המונעים על ידי MYC ו-KRAS מצביעות על כך שחלבוני סרטן שנחשבו "לא ניתנים לטיפול" עשויים להיות פגיעים כאשר הרפואה נראית יותר כמו מברשת מולקולרית מותאמת ולא כדור קטן יחיד.
ציטוט: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
מילות מפתח: הידרדרות חלבונים ממוקדת, MYC, KRAS, תרפיות פולימריות, ננו-רפואה בסרטן