Clear Sky Science · he
נוף אפיגנומי משולב של מוח חולי האלצהיימר חושף הפרעות מולקולריות באוליגודנדרוציטים הקשורות לטאו
מדוע המחקר המוחי הזה חשוב
מחלת האלצהיימר מוכרת בעיקר באובדן הזיכרון ובהצטברותם של שני חלבונים מזיקים במוח: אמילואיד וטאו. עם זאת, אנשים עם אלצהיימר יכולים להציג דפוסי נזק שונים מאד, אפילו כאשר יש להם את אותו אבחון. המחקר שואל שאלה מרכזית: אילו מתגים בתוך תאי המוח מסייעים לקבוע כמה מהחלבונים המזיקים האלה מצטברים, וכיצד הם משפיעים על סוגי תאים שונים? באמצעות בחינת תגים כימיים על ה-DNA במאות מוחות, החוקרים חושפים קשר מפתיע בין טאו לבין התאים שאחראים על תפקוד “החיווט” של המוח.
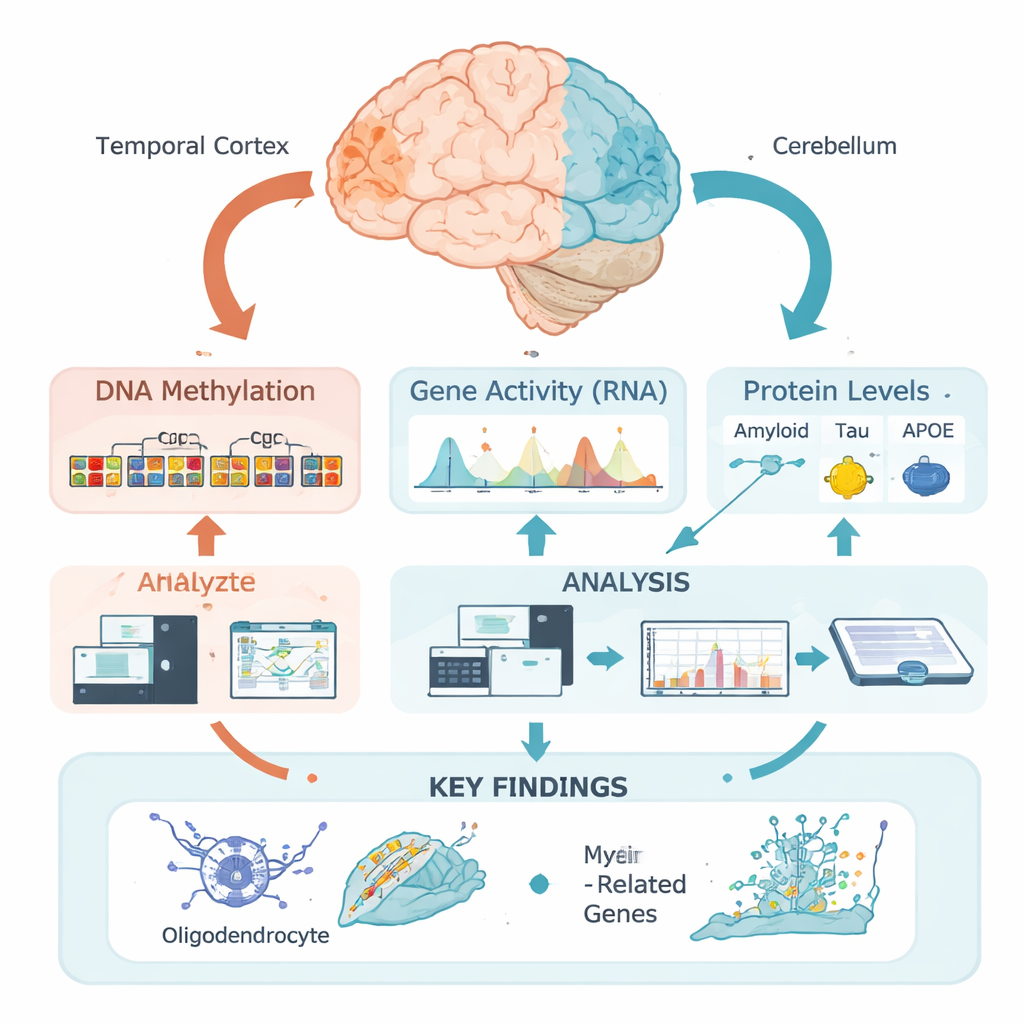
תגים כימיים על ה-DNA כמתגים סמויים
ה-DNA שלנו נושא את ההוראות הבסיסיות לבניית ותפקוד תאי המוח, אך אותן הוראות מנוהלות על ידי סימנים אפיגנטיים—תגים כימיים שיכולים להדליק או לכבות גנים סמוכים בלי לשנות את הקוד הגנטי. אחד התגים החשובים ביותר הוא מתילציה של DNA, שבה קבוצות כימיות קטנות נצמדות לאתרים ספציפיים ב-DNA. במקום לבחון אתרים בודדים באופן מנותק, הצוות השתמש בגישה חדשה "אזורית": הם קיבצו אתרים סמוכים רבים לאזורים פונקציונליים בהתאם לאריזה של ה-DNA בקורטקס הטמפורלי, אזור שנפגע במידה רבה באלצהיימר, ובצרבלום, שהוא יחסית מוגן. כך יכלו לשאול היכן, בהקשר ביולוגי, דפוסי המתילציה משתנים בקשר לתכונות המחלה.
חיבור סימני ה-DNA לחלבוני האלצהיימר
החוקרים ניתחו רקמות מוח מ-472 אנשים שלמחלת האלצהיימר אושרה לאחר המוות. עבור כל דגימת קורטקס טמפורלי מדדו רמות מפורטות של אמילואיד, טאו ו-APOE בצורות ביוכימיות שונות, וכן ציונים מיקרוסקופיים קלאסיים של משקעי אמילואיד וסבכי טאו. לאחר מכן ביצעו מחקרי אסוציאציה אפיגנומיים רחבי-סקלה, תוך בדיקה האם רמות מתילציה אזוריות עוקבות אחרי מדידות אלה. באופן מדהים, כמעט כל הקשרים החזקים שהם מצאו היו קשורים לא לטאו אלא לטאו — ובעיקר לטאו הממסרי הכולל ולצורה ממברנית ומפוספרת (ממולקת כימית) שנחשבת רעילה במיוחד.
אות חזק בתאי ה"חיווט" של המוח
רבים מהאזורים ב-DNA שקשורים לטאו נמצאו בחלקים "פעילים" של הגנום שמשפיעים על גנים סמוכים. על ידי שילוב נתוני מתילציה עם מדידות פעילות גנים מאותם מוחות, הצוות הראה שאזורים אלה לעתים קרובות שולטים בגנים המיועדים לאוליגודנדרוציטים—התאים העוטפים סיבי עצב במיאלין המבודד, ומאפשרים לאותות חשמליים לנוע במהירות ובאמינות. גנים מרכזיים הקשורים למיאלין כגון MBP, MAG ו-MYRF, יחד עם גן סיכון לאלצהיימר BIN1 וגֵן מועמד חדש בשם LDB3, הופיעו בקבוצה זו. רמות גבוהות של טאו ממוספר רעיל נטו להלכת יד עם מתילציה מוגברת באזורים אלה וביטוי נמוך של גני האוליגודנדרוציטים והמיאלין המקושרים אליהם, בעוד מאגר הטאו הממסרי הכולל הפחות מזיק הראה את הדפוס ההפוך.
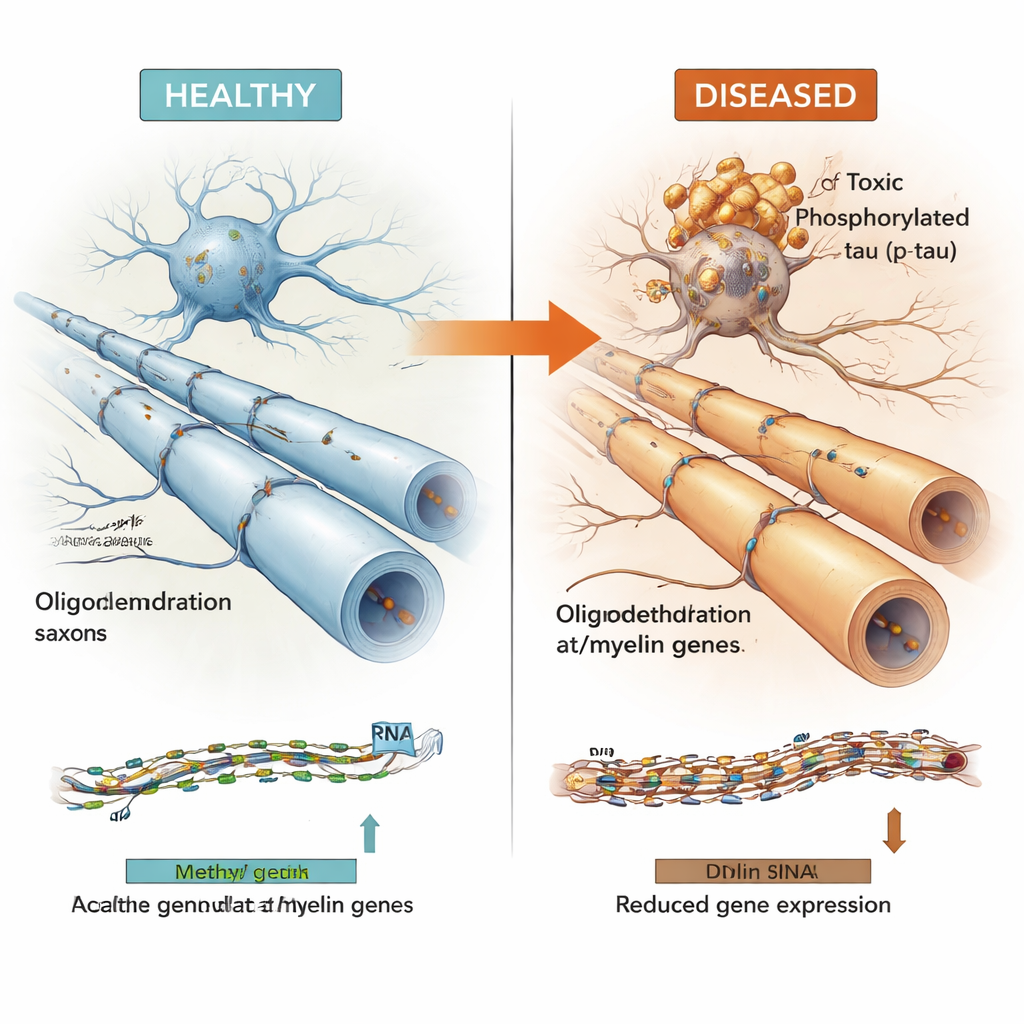
דפוס שניתן לראותו במחלות מוח שונות
כדי לבדוק האם הממצאים היו יציבים וכלליים, המחברים בחנו מערכי נתונים גדולים ועצמאיים מאוספים מוחיים אחרים של אלצהיימר, וממוחות שנפגעו ב"טאוופתיות" ראשוניות כמו דלדול גרעיני מתקדם (progressive supranuclear palsy) ומחלת פיק. אף על פי שקוהורטים אלה נמדדו בטכנולוגיות שונות ולעתים באזורים מוחיים שונים, רבים מאותם אזורי DNA וגני אוליגודנדרוציטים הראו התנהגות עקבית: רמות המתילציה שלהם היו מקושרות לעומס סבכי טאו, וביטוים היה מופחת במוחות חולים ובמחקרים חד-תאיים שהתמקדו במיוחד באוליגודנדרוציטים. חשוב לציין כי דפוסים אלו לא נראו מוסברים בפשטות על ידי גנטיקה או על ידי אובדן תאים כולל, מה שמעיד על שינוי אפיגנטי אמיתי בתפקוד האוליגודנדרוציטים.
מה משמעות הדבר להבנת האלצהיימר
במבט כולל, התוצאות תומכות במודל שבו עלייה ברמות טאו המזיק קשורה קשר הדוק לשינויים אפיגנטיים באוליגודנדרוציטים שמדכאים גנים הקשורים למיאלין, מה שעלול להחליש את ה"חיווט" של המוח ולתרום לירידה קוגניטיבית. עדיין לא ברור מה קורה קודם—הצטברות טאו או השיבוש של גני המיאלין—אבל הקשרים ההדוקים והחוזרים שנצפו באלפי דגימות ובכמה מחלות מצביעים על מנגנון משותף. על-ידי מיפוי מתגים אלה ב-DNA ושילובם ב"אטלס מולטי-אומיקי" ציבורי, עבודה זו מדגישה את האוליגודנדרוציטים ואת וויסותם האפיגנטי כיעדים מבטיחים לטיפולים עתידיים שמטרתם לייצב מעגלי מוח, במקום להתרכז אך ורק בנוירונים או בכתמי אמילואיד.
ציטוט: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
מילות מפתח: מחלת האלצהיימר, חלבון טאו, מתילציה של DNA, אוליגודנדרוציטים, מיאלין