Clear Sky Science · he
הבסיס המבני של איתות ותִקְנוּן בערוץ המופעל על‑ידי אבץ (ZAC) בבני אדם
כיצד מתכת במינון זעיר מסייעת לתאי עצב לתקשר
אבץ מוכר בעיקר כתוסף תזונה בטבליות מולטי‑ויטמין, אך בתוך הגוף המתכת הזו גם פועלת כשליח כימי מהיר במוח. המחקר המתואר כאן חושף, ברזולוציה אטומית, כיצד חלבון מעט ידוע שנקרא ערוץ המופעל על‑ידי אבץ (ZAC) מזהה אבץ מחוץ לתאים וממיר את האות הזה לתגובה חשמלית. הבנת השער המיוחד הזה בממברנת התא עשויה להבהיר כיצד אבץ מעצב פעילות מוחית ולהציע דרכים חדשות לכוונן אותות עצביים במצב תקין ובמחלות.
שער מיוחד לאיתותי אבץ
רבים מההודעות המהירות בין תאי עצב מועברות על‑ידי מולקולות מוכרות כגון סרוטונין או אצטילכולין, שפותחות ערוצים בצורת טבעת בממברנת התא. ZAC הוא קרוב רחוק של קולטנים אלה, אך במקום להגיב למולקולה אורגנית הוא נדלק על ידי יוני מתכת כמו אבץ, נחושת ופרוטונים. ZAC קיים ברקמות רבות בבני אדם, כולל במוח, אך חסר בבעלי חיים מקובלים במעבדה כגון עכברים וחולדות, מה שעיכב את הקידמה. עבודה זו משתמשת במיקרוסקופ אלקטרונים בקריוגניקה ברזולוציה גבוהה כדי לשמר כמה תמונות תלת‑ממדיות של ZAC האנושי: בצורתו המנוחה, כשהאבץ קשור, ועם שני נגדים שונים שמכבים את הערוץ. יחד, המבנים האלה מגלים כיצד האבץ מתעגן בחלק העליון של הערוץ, כיצד יונים עוברים דרכו ואיך החוסמים מהדקים את השער או משרים אותו במצב פתוח אך לא מוליך.
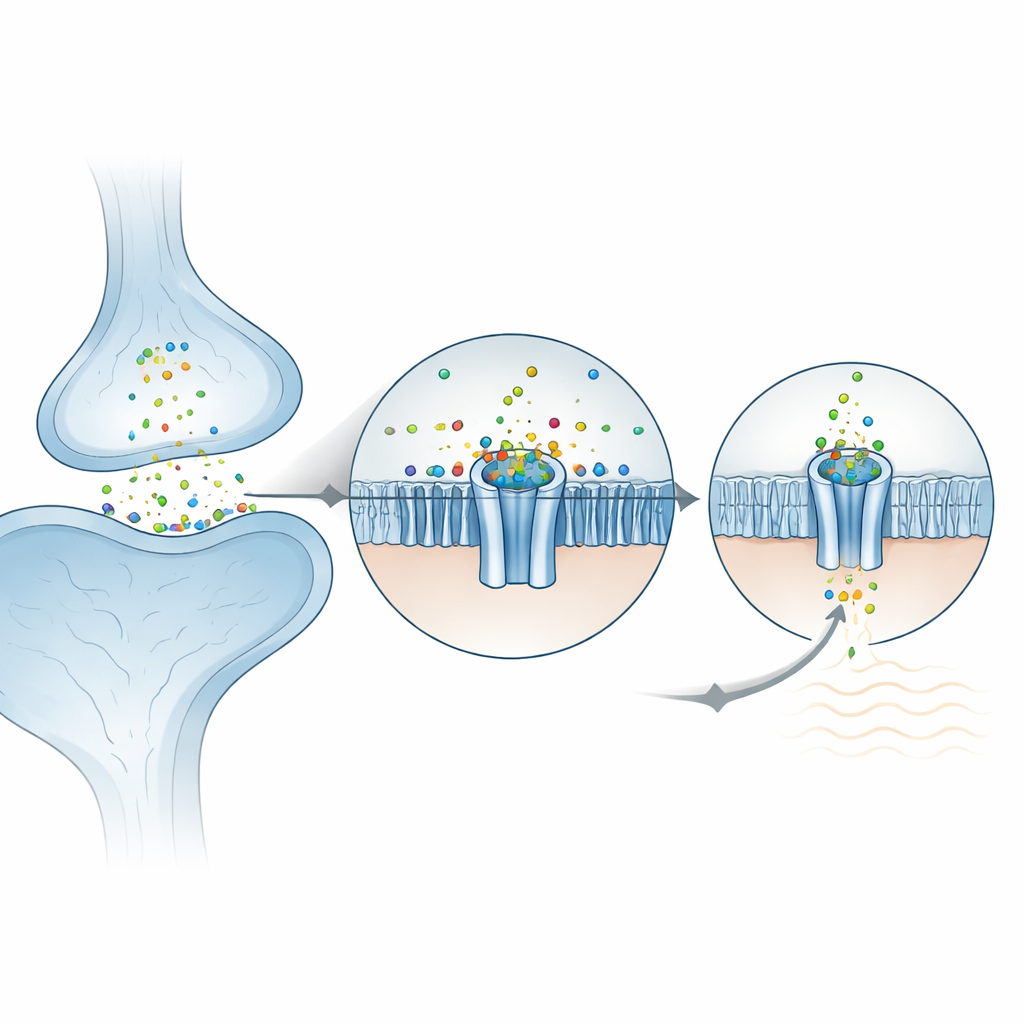
כיצד האבץ ננעץ בתוך הערוץ
בשטח החיצוני של התא, ZAC בנוי מחמישה תת‑יחידות זהות היוצרות סידור דמוי פרח. החוקרים מצאו שיוני אבץ שוקעים בחמישה כיסים שקולים, כל אחד ביניהם בין שתי תת‑יחידות סמוכות בתחום החיצוני. באופן מפתיע, האבץ אינו מוחזק על‑ידי חומצות אמינו ‘‘תופסות’’ רגילות שמקשרות מתכות (כמו היסטידין או ציסטאין). במקום זאת, הוא מיושן בעיקר על‑ידי שתי שרשראות צד ארומטיות טבעתיות שמייצבות את היונים החיוביים באמצעות אינטראקציות קטיון–π. כאשר שינו את שיירי המפתח הללו בביצי צפרדע ששימשו לרישומים חשמליים, הערוץ הפסיק להגיב לאבץ, מה שאשר את תפקידם המרכזי. הסביבה הסמוכה כבר מאורגנת מראש, מה שעוזר להסביר מדוע ל‑ZAC יש פעילות ספונטנית ניכרת גם ללא אבץ: החלבון יושב קרוב לנקודת המהפך בין סגור לפתוח, והאבץ פשוט מושך את המאזן.
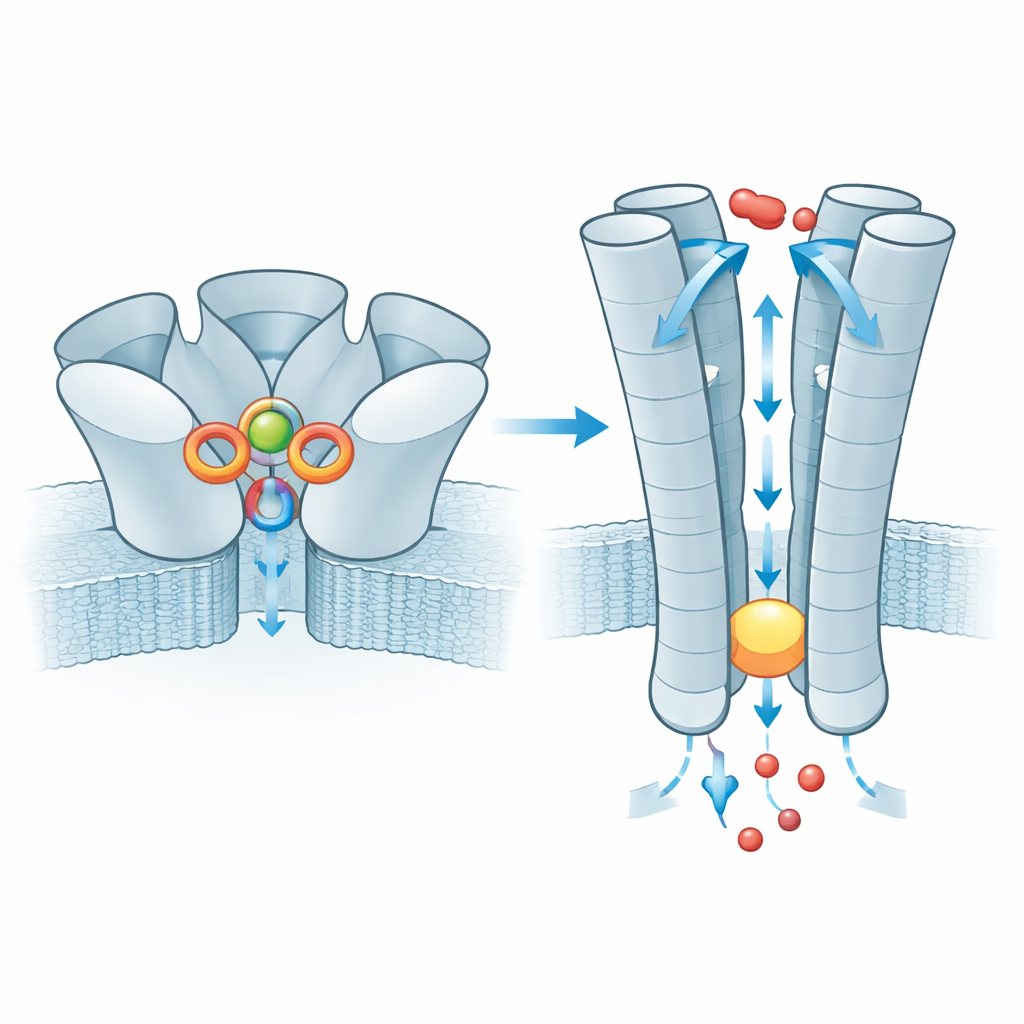
נתיב היונים ובני אדם עם וריאנט גנתי שכיח
לאחר שאבץ נקשר, האפקט מועבר לחלק החוצה ממברנה של ZAC, שם חמש אלפנות פנימיות יוצרות את הנקב. במצב המנוחה הצינור הזה מצטמצם בטבעת של שיירי לֵאוּצין, שיוצרת פקק הידרופובי שחוסם תנועת יונים. כשהאבץ קשור, הפקק מתרחב במידה המאפשרת ליונים קטנים חיוביים כגון נתרן ואשלגן לחלוף, בעוד שהשורה המטענת בתוך הנקב מסייעת בסלקציה של יונים אלה. הצוות בדק גם וריאנט אנושי נפוץ של ZAC שבו חומצה אמינית אחת (תריאונין) מוחלפת באלנין בקטע קצר מעל הפקק. שינוי קטן זה מחליש רשת אינטראקציות בין תת‑יחידות שכנות שבדרך כלל מסייעת להעביר את קשירת האבץ אל השער, ומדידות חשמליות מראות שערוצים הבנויים מהווריאנט הזה מוליכים זרמים קטנים בהרבה. לפיכך הווריאנט פועל כמרכז המרה פחות יעיל של האות, אף שהשפעתו הפיזיולוגית בבני אדם נותרת לא ברורה.
כיצד שני תרופות משתקות את הערוץ
מעבר לאבץ, המחקר בוחן גם כיצד שני אנטגוניסטים, TTFB ו‑d‑טובוקורארין (d‑TC), מכבים את ZAC. TTFB הוא מולקולה זעירה מעוצבת שנעוצה עמוק באזור הממברנה, חודרת בין שתי האלפנות היוצרות את הנקב ממש מעל השער. שם היא מתקשרת לכיס הידרופובי צמוד ולשיירים פולריים בקרבת מקום, מה שמחזיק את האלפנות כך שלא יוכלו לזוז למצב פתוח מוליך מלא. d‑TC, תרופה ותיקה שבעבר שומשה כמשחרר שרירים, פועלת באופן רחב יותר. מולקולת d‑TC אחת נקשרת לאותו כיס חיצוני שלרוב מאכלס אבץ, מדמה את המטען החיובי של האבץ אך חוסמת קשירה תקינה של אבץ אמיתי. מולקולת d‑TC נוספת יושבת בפתיחת הנקב עצמה, ומסתירה פיזית את המנהרה. יחד, הקשירות האלה לוכדות את ZAC במצב חסר‑חישה, לא מוליך, בעוד צורת החלבון נשארת יחסית פתוחה.
מה משמעות הממצאים לגבי אבץ ובריאות
עבודה מבנית זו מראה בפרטי מולקולרים ברורים כי ZAC הוא חיישן אבץ אמיתי, המשתמש בעריסה ארומטית בלתי שגרתית כדי לזהות את המתכת באותו סוג אתר שבו בני המשפחה האחרים מקשרים מוליכי עצב. היא גם מזהה רשתות אינטראקציה ספציפיות המכוונות עד כמה הערוץ נפתח ונסגר, וממפה שני אתרי קשירת תרופות מובחנים שיכולים או לשים יתד בשער או לשתק את הנקב. עבור קהל לא‑מומחה, המסר המרכזי הוא שאבץ אינו רק חומר תזונתי סטטי אלא אות פעיל, ו‑ZAC הוא אחד המקלטים המוקדשים שלו. ככל שמדענים חוקרים את תפקידי ZAC בגוף האדם ובמחלות נוירולוגיות המקושרות לחוסר איזון אבץ, שרטוטים ברמת האטום אלה מספקים מפת דרכים לעיצוב מולקולות מדויקות יותר למתן השפעה על הערוץ ובפוטנציאל לתקן איתותי אבץ מופרעים.
ציטוט: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
מילות מפתח: איתות אבץ, ערוצי יונים המופעלים על‑ידי ליגנד, נוירו‑מדע, מבנה cryo‑EM, שינוי ערוץ