Clear Sky Science · he
תפקיד מצעדי השומנים בממסלול האונקוגני המתווך על ידי FGFR2c באמצעות מעורבות תעלת TRPA1 בתאי אדנו-קרצינומה של צינור הלבלב
מדוע איים קטנים בממברנת התא חשובים
סרטן הלבלב הוא אחד הסרטנים הקטלניים ביותר, בין השאר משום שתאיו מיוחדים ביכולתם להתנתק מן הגידול המקורי ולחדור רקמות סמוכות. מחקר זה בוחן "איים" זעירים בעור החיצוני של תאי הסרטן, עשויים כולסטרול ושומנים, ושואל שאלה פשוטה בעלת השלכות גדולות: האם האיים האלה מסייעים להפעיל אות גדילה שהופכת את סרטן הלבלב לאגרסיבי יותר, והאם פגיעה בהם יכולה להאט את התהליך?
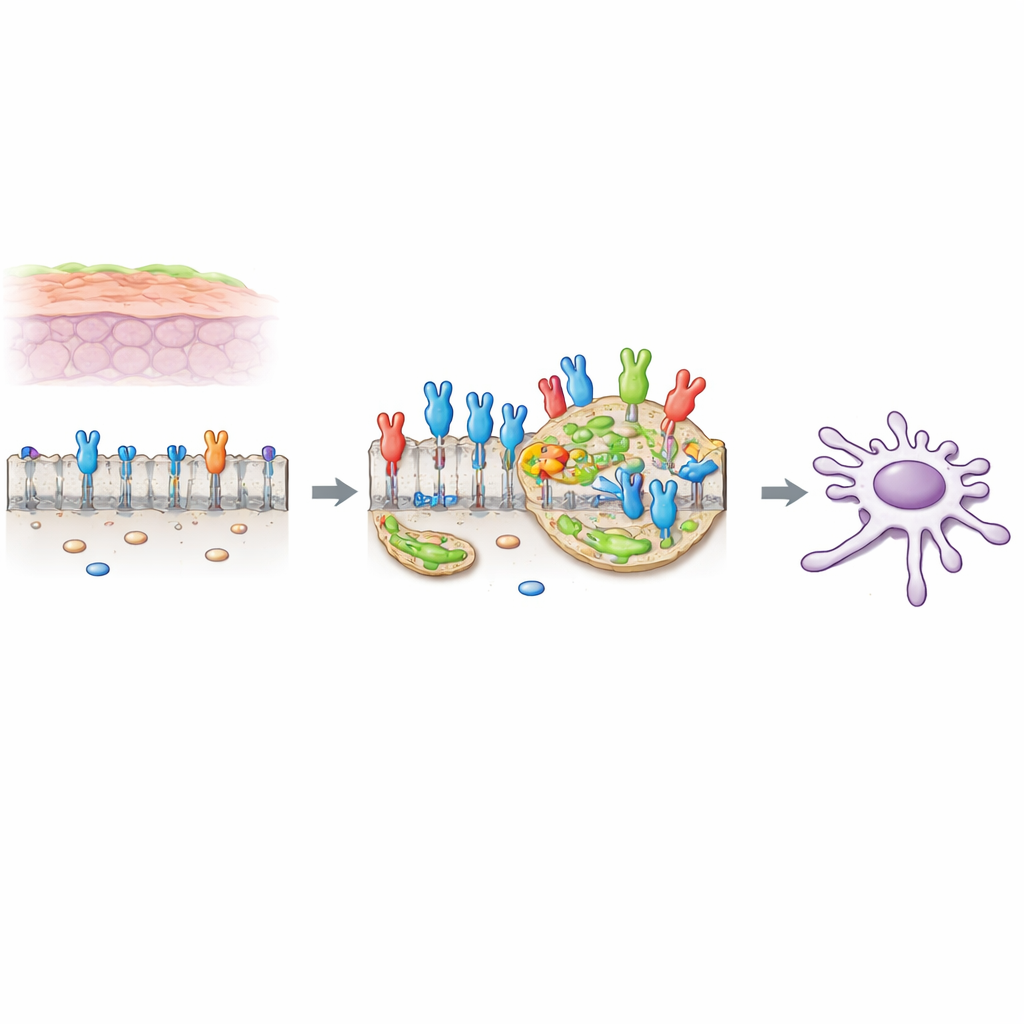
מתג מקדם-סרטן על פני התא
תאים רבים נושאים מתגים על פני השטח שמגיבים לאותות גדילה. אחד המתגים האלה, בשם FGFR2c, הוא וריאנט שנמצא בדרך כלל בתאים גמישים וניידים יותר, אך הוא הופך לשמור-יתר בתאי אדנו-קרצינומה של צינור הלבלב (PDAC). כאשר מתג זה נדלק על ידי מולקולה מתאמת בסביבה, הוא מניע שינויים הידועים כהעברה אפיתליאלית–מזנכימלית (EMT), שעושים את התאים פחות דבקים ויותר מסוגלים לנוע ולחדור. עבודות קודמות של המחברים הראו שבתאי PDAC, FGFR2c מפעיל שרשרת של שליחים פנימיים הכוללת את החלבון PKCε וכמה מסלולי גדילה קלאסיים, ומגביר שרידות, תנועה וחדירה של התאים.
איים עשירים-כולסטרול כמגברים של אות
הממברנה החיצונית של התא אינה אחידה. היא מכילה טלאים קטנים עשירי כולסטרול הנקראים מצעדי שומנים (lipid rafts), המשמשים כזירות מיקרו שבהן מולקולות איתות יכולות להתכנס ולהתקשר ביעילות רבה יותר. החוקרים מצאו שכאשר FGFR2c מוּפעַל על ידי האות החיצוני שלו, יותר קולטנים נעים לתוך מצעדי השומנים הללו. באמצעות סימונים פלואורסצנטיים ויזור ביוכימי, הראו שה-FGFR2c המופעל מתרכז בכתמים אלה, בעוד שהתפלגותו מחוץ למצעדים משתנה מחלקה לחלקה מנוקד, בהתאמה לאשכולות קולטנים על האיים הללו.
פירוק האיים מחליש תכונות סרטניות
כדי לבדוק האם האיים השומניים חיוניים להשפעות המקדמות-סרטן של FGFR2c, הקבוצה השתמשה בתרכובת (מתיל-β-ציקלודקסטרין) שמסירה באופן סלקטיבי כולסטרול מהממברנה ומייצבת פחות את מצעדי השומנים מבלי להרוג את התאים. בתאי PDAC עשירים ב-FGFR2c, פגיעה במצעדים הפחיתה בחוזקה את הפעלת מולקולות איתות מרכזיות בהמשכה של הקולטן והחלישה את תכנית ה-EMT: גנים וחלבונים הקשורים למצב נייד וחדיר ירדו, בעוד שהתכונות האפיתליאליות שוחזרו בחלקן. אותו טיפול גם הוריד רמות של חלבונים הקשורים לחדירה כגון MCL-1, SRC ואנזימים מפרקי מטריצה, והקטין את יכולת תאי הסרטן לנוע ולחדור ג'ל המדמה את הרקמה הסובבת. בתאים עם מעט FGFR2c נרשמה כמעט אי-תגובה, מה שמדגיש עד כמה שותפות הקולטן–מצעד מרכזית בגידולים אלה.
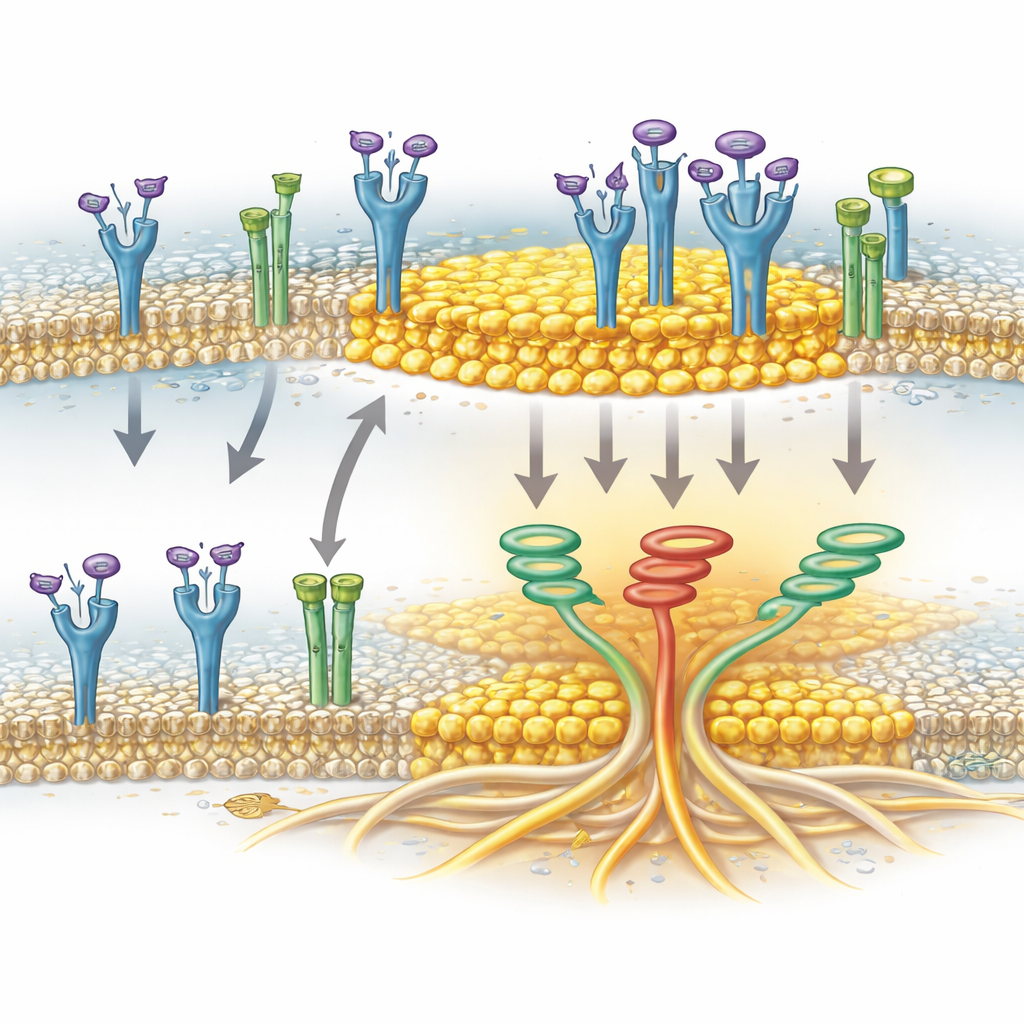
תעלת יונים כעוזרת לאשכולות
המחקר מזהה גם עוזרת מפתיעה: TRPA1, חלבון תעלה המוכר בעיקר כחושן לגירויים ולמתח חמצוני בעצבים. בתאי סרטן הלבלב, TRPA1 נוכח בממברנה ויכול לשכון במצעדי השומנים. המחברים הראו ש-TRPA1 מקושר פיזית ל-FGFR2c כאשר הקולטן מופעל, ושקישור זה חל בזמן העשרת ה-FGFR2c בשברי המצעדים. כאשר רמות TRPA1 הוכרעו, ה-FGFR2c המופעל כבר לא הצטבר ביעילות באזורים של מצעדים, אפילו כאשר המצעדים עצמם נותרו שלמים. זה מעיד ש-TRPA1 אינו רק נוסע פסיבי אלא מסייע באופן פעיל בליווי או בייצוב FGFR2c בתוך הפלטפורמות העשירות-כולסטרול הללו, שם הקולטן יכול להפעיל ביתר עוצמה את רשת האיתות המעודדת חדירה.
מה המשמעות לכך עבור טיפולים עתידיים
במבט הכולל, העבודה מציירת תמונה שבה FGFR2c, TRPA1 ומצעדי השומנים יוצרים יחידה שיתופית המעצימה את ההתנהגות החודרת של תאי סרטן הלבלב. FGFR2c מספק את אות הגידול, מצעדי השומנים מספקים את הבמה הפיזית שבה מתכנסים קומפלקסי האיתות, ו-TRPA1 עוזר להביא את הקולטן לבמה זו. עבור הקורא הכללי, המסקנה העיקרית היא שלא רק מולקולות הגידול עצמן, אלא גם נופי הממברנה הקטנים שהם תופסים, יכולים לקבוע כמה מסוכן יהיה הגידול. באמצעות ייעוד FGFR2c, TRPA1 או היציבות של האיים העשירים-כולסטרול — בנפרד או בשילוב — טיפולים עתידיים עשויים להיחלש את המכניזם החודר של תאי סרטן הלבלב באופן מדויק יותר ותלוי-גידול.
ציטוט: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
מילות מפתח: סרטן הלבלב, מצעדי שומנים, FGFR2c, תעלת TRPA1, חדירת תאים