Clear Sky Science · he
PRDM1 מגבילה את התקדמות סרטן שלפוחית השתן ומשפרת את הרגישות לכימותרפיה על ידי דיכוי ניתוק האוביקוויטין של CDC6 שמתווך על-ידי OTUD6A
מדוע המחקר הזה חשוב לחולים
סרטן שלפוחית השתן נפוץ ונוטה להילקח בטיפולים כימותרפיים כמו גמציטאבין וציספלטין. עם זאת, גידולים רבים אינם מגיבים היטב או מהירים בפיתוח עמידות, ומשאירים לחולים אפשרויות מצומצמות. מחקר זה חושף בלם פנימי בתאי השלפוחית — חלבון בשם PRDM1 — שמעכב את צמיחת הגידול ועוזר לכימותרפיה לפעול טוב יותר. הבנת אופן הפעולה של הבלם הזה — ואיך הגידולים מכבים אותו — עשויה לפתוח דרכים לחיזוי תגובת הטיפול ולעיצוב טיפולים חכמים יותר.
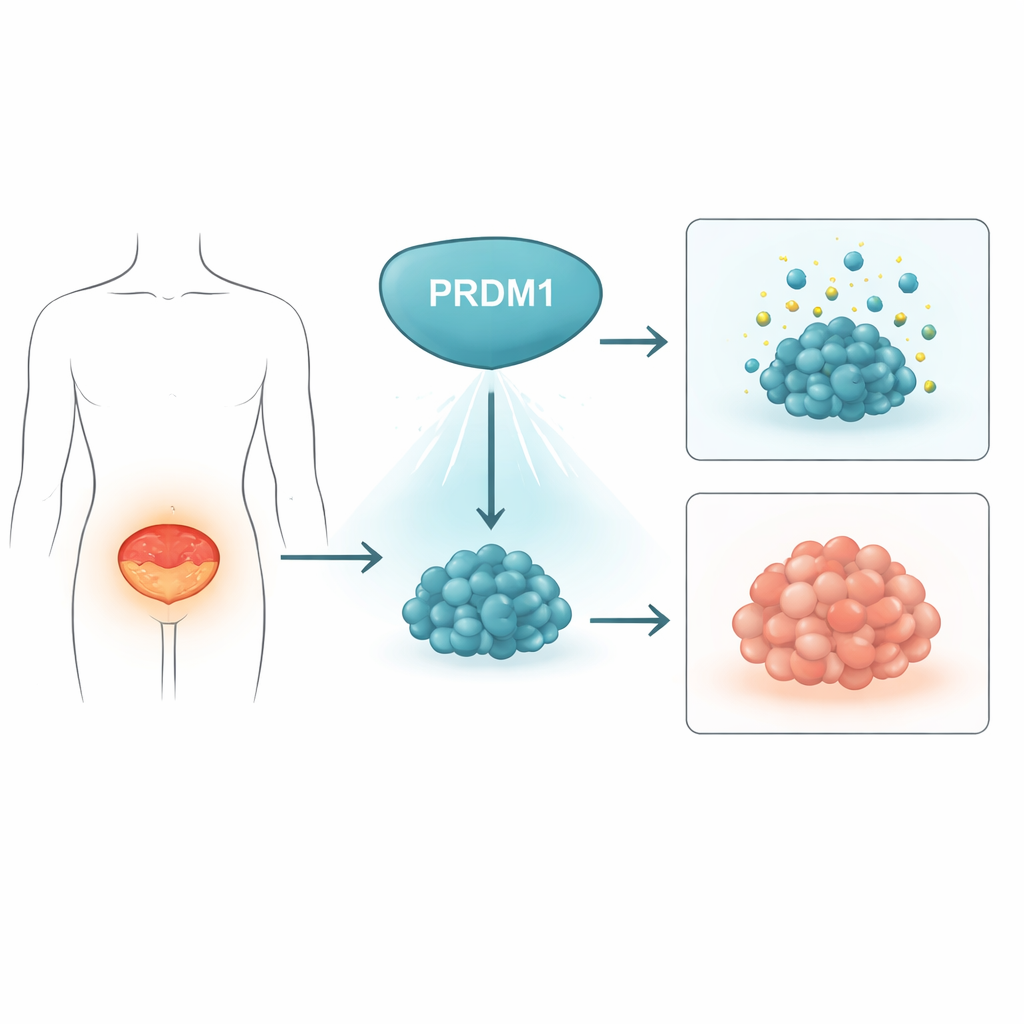
בלם טבעי על גידולי השלפוחית
חוקרי הצוות שאלו תחילה האם PRDM1, גן הידוע בוויסות התפתחות תאי מערכת החיסון, עשוי להשפיע גם על סרטן השלפוחית. בבדיקה של 48 זוגות של גידולים אנושיים של שלפוחית והרקמה התקינה הסמוכה, הם מצאו שרמות החלבון PRDM1 היו באופן עקבי נמוכות יותר בגידולים לעומת הרירית התקינה. מאגרי נתונים ציבוריים גדולים הראו דפוס דומה ברמת ה-RNA. במודל עכבר שבו סרטן שלפוחית מושרה בהדרגה על-ידי חומר במי השתייה, רמות PRDM1 ירדו בהדרגה כשרקמה תקינה הפכה לסרטנית. יחד, הנתונים הללו מצביעים על כך שבדרך כלל PRDM1 פועל כבלם על היווצרות גידול והוא נכבה ככל שסרטנות השלפוחית מתפתחת.
האטת גדילת תאים וחלוקת התא
כדי לחקור מה PRDM1 עושה בפועל בתוך תאי סרטן השלפוחית, הקבוצה השתמשה בכלים גנטיים להנמכה או להגברה של הביטוי. כשהורידו את PRDM1 בקווי תאי סרטן שלפוחית, התאים התרבו מהר יותר, יצרו יותר מושבות וצמחו לגידולים גדולים יותר בעכברים. השמטה מוחלטת של PRDM1 בעזרת עריכת גנים CRISPR הביאה להשפעות דומות. לעומת זאת, אילוץ ביטוי גבוה של PRDM1 האט את הצמיחה בתאיות והוביל לגידולים קטנים משמעותית במודלים בעלי חיים, וכן לרמות נמוכות יותר של סמן חלוקת התא Ki-67. ניתוח מפורט של מחזור התא הראה כי עודף PRDM1 גרם לעיכוב כאשר תאים ניסו לעבור ממיטוזה לשלב הגדילה הבא, מה שמציין שהחלבון מסייע לשמור על פיקוח על חלוקת התא.
הגברת פגיעות הכימותרפיה
מאחר שהצלחת הכימותרפיה תלויה במידה רבה עד כמה התרופות גורמות לנזק ל-DNA ומעוררות מוות תאי, החוקרים בדקו האם PRDM1 משפיע על הרגישות לתרופות. תאים חסרי PRDM1 היו קשים יותר להריגה באמצעות גמציטאבין או ציספלטין, נדרשו מינונים גבוהים יותר להשגת אותו אפקט, בעוד שתאים עם ביטוי מוגבר של PRDM1 הפכו לרגישים יותר. תאי חסרי PRDM1 הראו פחות נזק ל-DNA ופחות תאים מתים לאחר הטיפול, בעוד שתאים עם ביטוי יתר של PRDM1 הציגו יותר שברי DNA ורמות גבוהות יותר של סמנים אפופטוטיים. המחקר בחן גם מסלול מרכזי של איתות נזק ל-DNA הידוע כנתיב ATR–Chk1, שעוזר לתאים לשרוד כימותרפיה. אובדן PRDM1 הגביר את איתות ההישרדות הזה, בעוד שהגברה של PRDM1 דיכאה אותו. במודלים של גידולים בעכברים, גידולים עם PRDM1 גבוה הגיבו טוב יותר לגמציטאבין, והשבת PRDM1 בתאים עמידים חלקית הופכת את העמידות.
חשיפת מסלול בקרה בשלושה שלבים
בהעמקה נוספת, החוקרים זיהו שרשרת מולקולרית שמקשרת את PRDM1 לצמיחה התאית ולתגובת התרופה. בעבודה קודמת הם הראו כי אנזים בשם OTUD6A מייצב חלבון אחר, CDC6, שמעורב בהתחלת שכפול ה-DNA ובהפעלת איתות נזק ה-DNA. כאן הם גילו ש-PRDM1 אינו משנה את ההודעה הגנטית של CDC6 אלא מקדם את פירוקו על-ידי מכונת הפינוי של החלבונים בתא. PRDM1 מוריד את רמות OTUD6A, מה שמוביל לעלייה בסימונים כימיים על CDC6 המסמנים אותו לפירוק. כאשר הורידו באופן ניסיוני את OTUD6A או את CDC6, אלה נגדו את היתרון בצמיחה ובעמידות לתרופות שנגרם על-ידי חוסר PRDM1. להפך, העלאת OTUD6A או CDC6 יכלה לבטל את היתרונות של PRDM1 גבוה. ניתוחים של דגימות מטופלים אשררו קשר זה: בגידולים נמצא בדרך כלל PRDM1 נמוך אך OTUD6A ו-CDC6 גבוהים, ורמות החלבונים הללו היו קשורות זו לזו בחוזקה.
מה המשמעויות לטיפולים עתידיים
בסך הכל, המחקר מספק מפת מסלול שבה PRDM1 מעכב את סרטן השלפוחית ומשפר את תגובת הכימותרפיה על ידי כיבוי OTUD6A, מה שמאפשר לתא לפרק את CDC6. בלי הבלם הזה CDC6 מצטבר, חלוקת התאים מואצת ותאי הגידול הופכים מיומנים יותר לשרוד תרופות שמזיקות ל-DNA. עבור חולים, הממצאים הללו מרמזים כי מדידת רמות PRDM1, OTUD6A ו-CDC6 בגידולים עשויה לעזור לחזות עד כמה הכימותרפיה תעבוד. בטווח הארוך, יתכן שניתן לפתח תרופות המשקמות את פעילות PRDM1 או חוסמות את OTUD6A או CDC6 כדי להחזיר רגישות לגידולים עמידים ולשפר את תוצאות הטיפול.
ציטוט: Cui, J., Chen, S., Liu, X. et al. PRDM1 restricts bladder cancer progression and enhances chemosensitivity by suppressing OTUD6A-mediated deubiquitination of CDC6. Cell Death Dis 17, 247 (2026). https://doi.org/10.1038/s41419-026-08498-3
מילות מפתח: סרטן שלפוחית השתן, עמידות לכימותרפיה, PRDM1, CDC6, OTUD6A