Clear Sky Science · he
דהידרו-אציל-CoA קצר־שרשרת מתחיל דה‑מתילציה ודליפה של mtDNA להנעת חיסון אנטי‑גידולי בסרטן המעי הגס
מדוע התאים שלנו לעתים מסתירים את הסרטן ממערכת החיסון
סרטן המעי הגס הוא אחד הגידולים הקטלניים בעולם, חלקית מפני שמערכת ההגנה החיסונית של הגוף לעתים קרובות אינה מזהה או תוקפת אותו. המחקר הזה חושף קשר בלתי צפוי בין האופן שבו תאי סרטן שורפים שומנים, איך התחנות הכוח הקטנות שלהם (המיטוכונדריות) מטפלות ב‑DNA שלהן, והאם המערכת החיסונית מתעוררת לנוכחות הגידול. באמצעות מעקב אחרי שרשרת האירועים הזו, החוקרים גם מצביעים על חומר טבעי ותיק, היפריצין, כדרך אפשרית להחזיר את התקיפה החיסונית בסרטן המעי הגס.
"שומר" מיטוכונדריאלי חסר בגידולי המעי
הצוות החל בחיפוש במאגרי נתונים גדולים של בני אדם ועכברים כדי למצוא גנים מטבוליים שמשתנים בעקביות בסרטן המעי הגס. אנזים אחד עלה על פני השטח: דהידרוגנאז אציל‑CoA קצר־שרשרת, או ACADS, שעוזר במצב תקין למיטוכונדריות לפרק חומצות שומן קצרות. בדגימות מטופלים ובכמה מודלים עכבריים, רמות ה‑ACADS היו נמוכות משמעותית ברקמת הגידול לעומת המעי הבריא הסמוך. כאשר המדענים הפחיתו ACADS בתאי סרטן מעי עכבריים, הגידולים גדלו מהר יותר ובאופן תוקפני יותר; הגדלת ה‑ACADS האטה את גדילת הגידול. בעכברים מהונדסים שחסרו ACADS באופן ספציפי ברירית המעי התפתחו יותר וגידולים גדולים יותר במודל כימי של סרטן המקושר לדלקת המעי, נתמך הרעיון ש‑ACADS פועל כמדכא גידולים במעי.
כיצד הגידולים מכבים אותות אזעקה חיסוניים
השפעות הגדילה האלה לא ניתנו להסבר רק בקצב חלוקת התאים במעי בתרבית, ששונה במעט. במקום זאת, אובדן ACADS קידם גדילת גידול רק בחיות עם מערכת חיסון שלמה, מה שמצביע על שינוי בסביבת הגידול. ניתוח יחיד‑תאי של סרטן המעי האנושי הראה כי גידולים עם ACADS נמוך היו מוקפים ביותר תאי גידול ותאים מדכאים של מערכת החיסון — כגון תאים מדכאי מוצא מיולוגי, מקрофאגים מסוימים ותאי T רגולטוריים — ופחות תאי T מועילים ותאי הרג טבעיים. דפוס זה מצביע על "שכונה אימונוסופרסיבית" שמסתירה את הגידול מהתקפה. 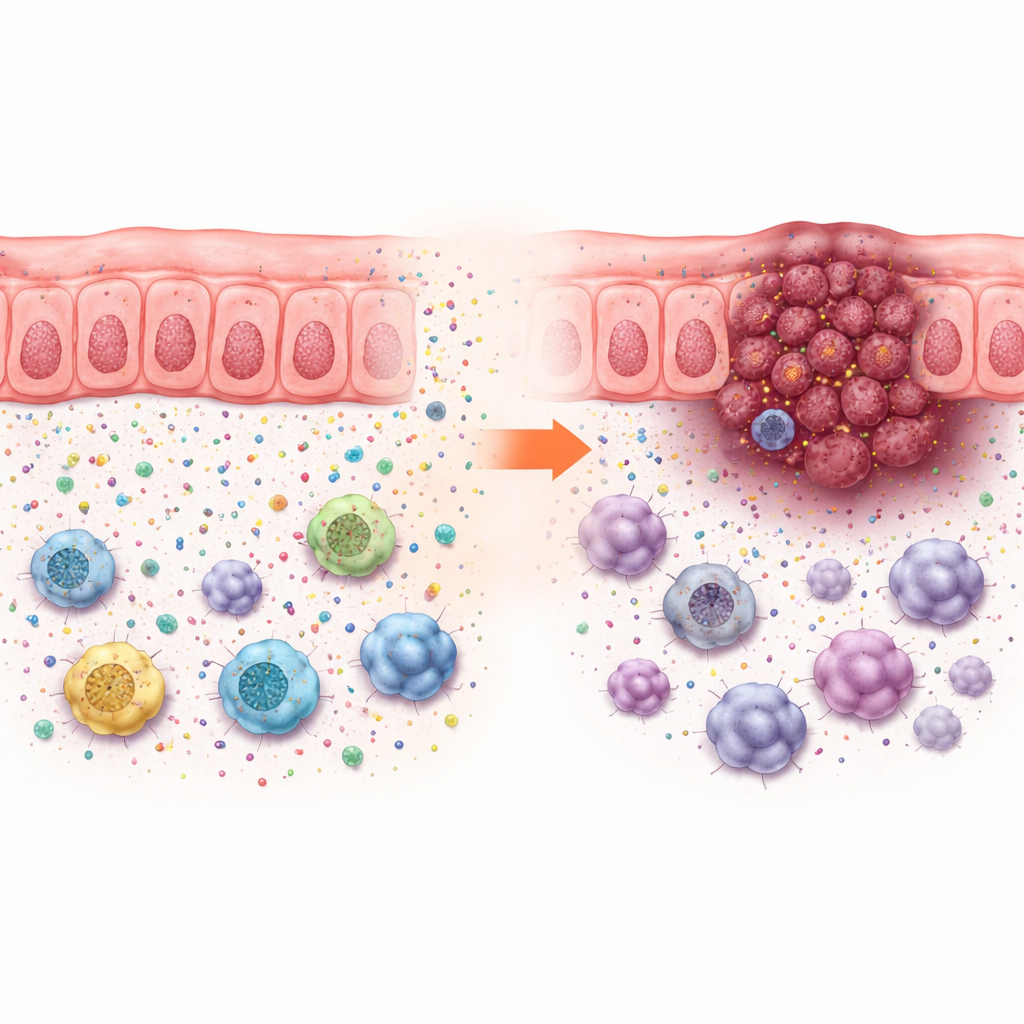
דליפת DNA מיטוכונדריאלי כטריגר הסמוי
מה מחבר בין אנזים שורף שומנים לחיישן DNA חיסוני? התשובה טמונה ב‑DNA המיטוכונדריאלי (mtDNA). בתנאי לחץ, חתיכות של mtDNA יכולות לדלוף מהמיטוכונדריות לנוזל התוך‑תאי, שם cGAS מזהה אותן כאות סכנה. החוקרים הראו שתאי סרטן חסרי ACADS הכילו פחות mtDNA במחזור זה, אף שה‑mtDNA הכולל לא השתנה. חסימת הדליפה של mtDNA בתאים עם רמות גבוהות של ACADS כיבתה את cGAS–STING, ואישרה כי הרסיסים האלה שברחו הם האזעקה הקריטית. באופן מפתיע, גורמי לחץ מיטוכונדריאלי קלאסיים כמו סוגי חמצון פעילים (ROS), גלי סידן ושינויים גדולים בצורת המיטוכונדריות לא הסבירו לחלוטין את ההבדל. במקום זאת, המחקר מצביע על ה"שערים" בממברנה המיטוכונדריאלית ובעיקר על הסימנים הכימיים על ה‑mtDNA עצמו. 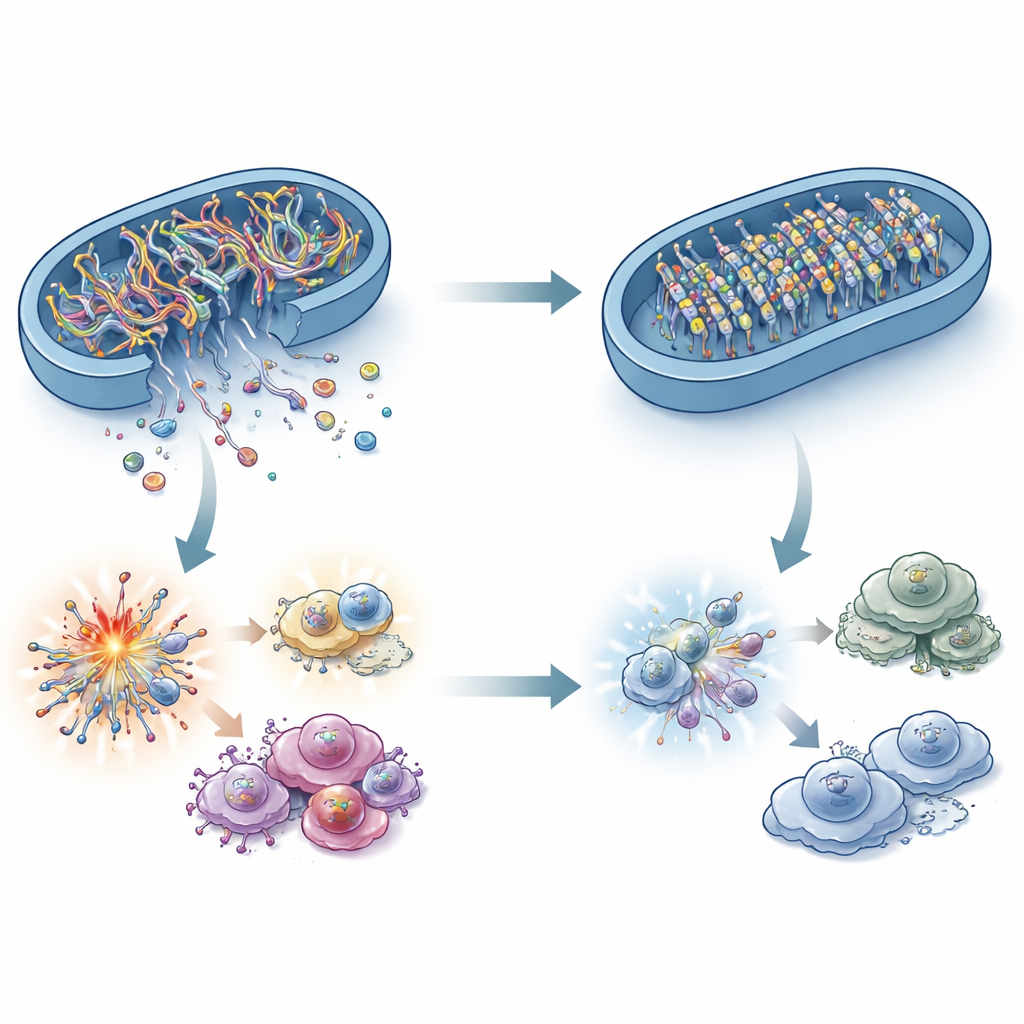
שותף ממתיל‑DNA שנועל את האזעקה מבפנים
באמצעות סריקות אינטראקציות חלבון־חלבון נמצא כי ACADS מקושר לצורתו המיטוכונדריאלית של אנזים מתילציית ה‑DNA DNMT1. כש‑ACADS ירד, אותו DNMT1 מיטוכונדריאלי הצטבר, והוסיף קבוצות מתיל ל‑mtDNA. סימנים אלה מקנים ל‑mtDNA יציבות מוגברת ופחות נטייה לשבירה ולדליפה. העמסת תאים ב‑DNMT1 מיטוכונדריאלי הקטינה את בריחת ה‑mtDNA, דיכאה איתות cGAS–STING והאיצה את גדילת הגידול, בעוד שחסימת DNMT1 באמצעות הדאקיטאבין השיבה את דליפת ה‑mtDNA והאטה גידולים חסרי ACADS. דגימות מטופלים השתקפו בממצאים אלה: ACADS נמוך היה מקושר ל‑DNMT1 מיטוכונדריאלי גבוה, איתות STING חלש יותר, פחות תאי אפקטור T, יותר תאי חיסון מדכאים ותשובות צפויות גרועות יותר לאימונותרפיה מבוססת‑checkpoint.
החייאת ההגנות החיסוניות באמצעות תרכובת ותיקה
כדי לבדוק אם אפשר לנצל את המסלול לטיפול, החוקרים השתמשו בסריקה ממוחשבת לחיפוש מולקולות שמקשרות ל‑ACADS. הם זיהו את ההיפריצין, פיגמנט טבעי שנבדק בעבר כטיפול מואר לכמה לימפומות עוריות. בתאי סרטן מעי, ההיפריצין הגדיל רמות ACADS, הוריד את ה‑DNMT1 המיטוכונדריאלי, הגביר דליפת mtDNA ופעיל מחדש את איתות cGAS–STING — שינויים שתלויים בנוכחות ACADS. במודלים עכבריים של גידולים ובתרביות קצרות טווח של גידולים אנושיים, טיפול בהיפריצין הקטין גידולים או הזיז את מורכבות התאים החיסוניים לכיוון פעיל יותר, עשיר בתאי T. למרות שנדרש עוד עבודה לפני שימוש קליני, ממצאים אלה מרמזים כי הפעלה תרופתית מחדש של ACADS עשויה לסייע להמיר גידול "קר" ומדוכא חיסונית לאחד שמגיב טוב יותר לאימונותרפיה.
מה משמעות הדבר עבור מטופלים וטיפולים עתידיים
במלים פשוטות, עבודה זו מראה שחלק מהמקרים של סרטן המעי הגס צומחים חלקית מפני שהם משתיקים אנזים מיטוכונדריאלי שבאופן רגיל מסייע לדלוף קטעי DNA זעירים לתוך תא, שם הם משמשים כאיתותים לקריאה למערכת החיסון. בכך שלשיתוף פעולה של דה‑מתילציה של DNA המיטוכונדריאלי מסגרת את ה‑mtDNA במקום, גידולים חסרי ACADS משאירים את האיתותים האלה מוסתרים ומתחמקים מזיהוי חיסוני. שיקום פעילות ACADS, למשל באמצעות תרופות דמויות היפריצין, יכול לפתוח מחדש את מערכת האזעקה המיטוכונדריאלית הזאת, לחזק חיסון אנטי‑גידולי ולשפר תגובות לאימונותרפיות קיימות. ACADS, DNMT1 מיטוכונדריאלי ופעילות מסלול STING עשויים לכן לשמש כסמנים וביעדים שימושיים במאמצים לפיתוח טיפולים יעילים יותר לסרטן המעי הגס.
ציטוט: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
מילות מפתח: סרטן המעי הגס, חיסון כנגד גידול, DNA מיטוכונדריאלי, מטבוליזם שומנים, מסלול cGAS‑STING