Clear Sky Science · he
מטרה: fused in sarcoma (FUS) — אסטרטגיית אנטיסנס חדשה לטיפול בפיברוזיס ריאתי אידיופטי
מדוע צלקות בריאות חשובות
פיברוזיס ריאתי אידיופטי (IPF) היא מחלה ריאתית מתקדמת שבה נימיות אוויר עדינות הופכות בהדרגה לרקמת צלקת קשיחה, מה שמקשה על כל שאיפה. התרופות הקיימות כיום יכולות להאט את התקדמות הצלקתיות אך אינן עוצרות או הופכות אותה. המחקר בוחן מטרה חדשה בשם FUS, חלבון המסייע לתאים לטפל במסרים הגנטיים שלהם, ובודק האם כיבויו בעזרת גדיל מעוצב של חומר דמוי DNA יכול להרגיע את תהליך הצלקתיות ולעודד תיקון של ריאות פגועות.
מנהל תנועה תאית שנותר על המסלול
FUS הוא חלבון שבדרך כלל שוכן בגרעין התא, שם הוא מסייע לנהל כיצד RNA — העתק הפעיל של הגנים שלנו — מעובד ומנוצל. במחלות מוחיות כגון ALS החלבון יכול להתנהג בצורה לקויה, לעזוב את הגרעין, להצטבר באזורים החיצוניים של התא ולהפריע לתפקוד התקין. החוקרים תהו האם התנהגות דומה עשויה לנהוג את הצלקתיות ב‑IPF. הם בחנו פיברובלסטים ריאתיים — תאי רקמת החיבור שמניחים את חומר הצלקת — ממטופלים עם IPF ומיתורמים בריאים. בתאים של חולי IPF נצפו רמות גבוהות יותר של FUS בסך הכל ובמיוחד כמות גדולה יותר של FUS בציטופלסמה בהשוואה לתאים בריאים. באמצעות מיקרוסקופ אלקטרונים ברזולוציה גבוהה אישרו שהחלבון מצוי בכמות חריגה מחוץ לגרעין, מרמז שאופן שליטתו על ה‑RNA עלול להיות מעוות בריאות פיברוטיות. 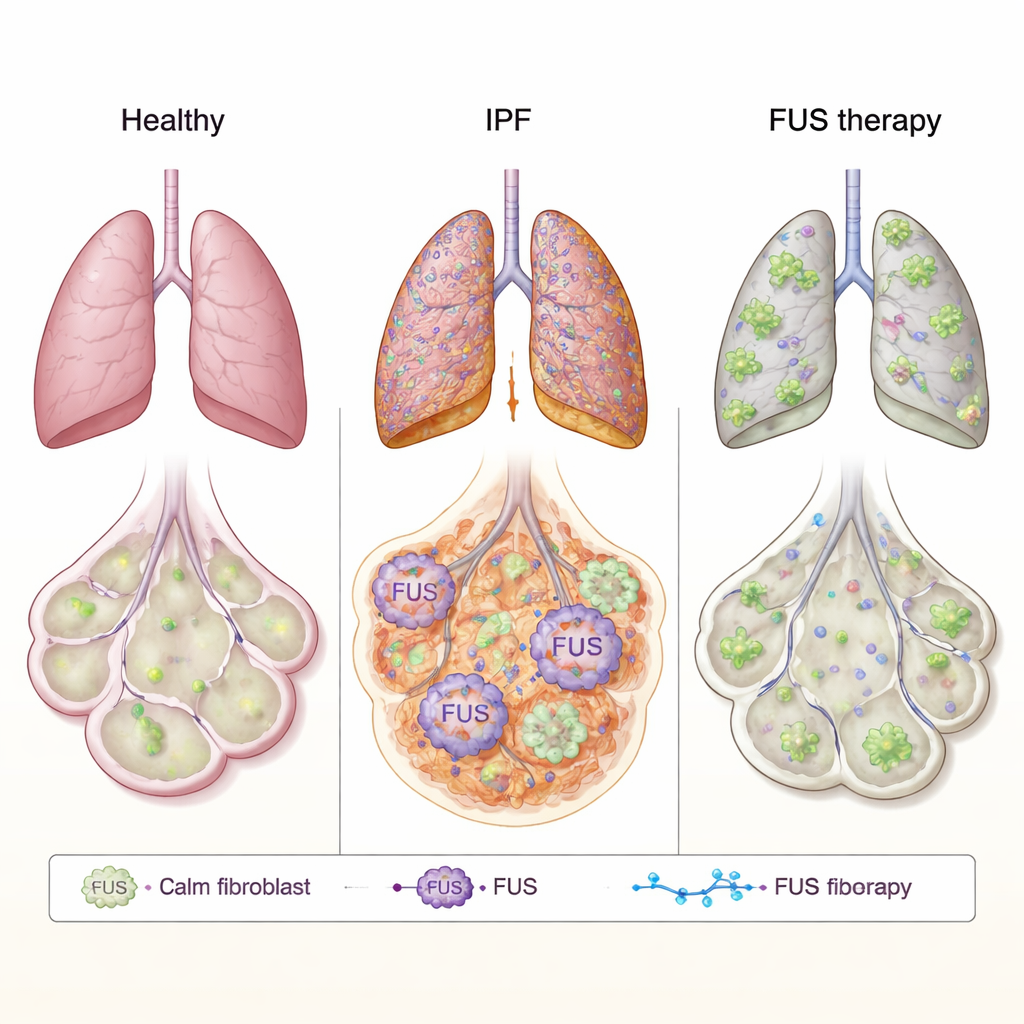
כיצד FUS מדליק תאי צלקת
כדי לבדוק מה החלבון המתנהג באופן לקוי עושה בפועל, החוקרים הגבירו את רמות FUS בפיברובלסטים בריאים והורידו אותן בפיברובלסטים של IPF. עודף FUS דחף תאים בריאים להתחלק מהר יותר, בעוד שהפחתת FUS בתאי IPF האטה את הגידול והתנועה שלהם — שני התנהגויות מרכזיות ביצירת הצלקת. הצוות השתמש אחר כך בטכניקה שמקפיאה קשרים בין חלבון ל‑RNA וקוראת אילו RNAs קשורים ל‑FUS. בפיברובלסטים של IPF נמצא כי FUS נקשר בהרבה מסרים גנטיים המעודדים פיברוזיס, כולל אלה המקודדים לקולגן, גורמי גדילה כמו TGF‑β, ואותות דלקתיים. במילים אחרות, FUS פעל כצומת המחברת רשת שלמה של מסרים פרו‑צלקתיים.
שתיקת האות בעזרת תרופה מדויקת
המחקר בחן אוליגונוקלאוטיד אנטיסנס בשם ION363 — גדיל קצר, מעובד כימית, שעוצב לקשור את ה‑RNA של FUS ולגרום להשמדתו. כאשר פיברובלסטים של IPF טופלו ב‑ION363, רמות FUS ירדו, התאים האטו את התרבותם וההגירה שלהם, וגנים מרכזיים לבניית צלקת שקטו. חשוב לציין שהתוצאה לא נבעה מהרג תאים או הכפפתם להזדקנות; במקום זאת נראה שהטיפול איפס את ההתנהגות שלהם. כאשר אותו טיפול הופעל על פרוסות דקיקות של רקמת ריאה מ‑IPF שהוחזקו בחיים במעבדה, קבוצות גדולות של גנים הקשורים למטריצה החוץ‑תאית, דלקת ורירית אפיתלית לא תקינה דוכאו, בעוד שגנים הקשורים לייצור תמיסת פנים (סורפקטנט) ותפקוד אלוואולרי הועלו. הטיפול גם הפחית צביעת קולגן והגביר סמנים של תאי שטח ריאתיים תפקודיים, דבר שמעיד על תמורה מצלקת לכיוון תיקון.
עזרה לשיקום נימיות האוויר הפגועות
מכיוון שתאי השכבה הפנימית המיקרוסקופית של הנימיות, המכונים תאי אלוואולר מסוג II, חיוניים לתיקון הריאה, החוקרים בנו "אלוואולוספירים" תלת‑ממדיים מתאי מטופלים כדי לדמות יחידות ריאה מיניאטוריות. בתרביות ממטופלי IPF מבנים אלה בדרך כלל שורדים באופן לקוי. בטיפול ב‑ION363 נוצרו יותר אלוואולוספירים, הם גדלו יותר והציגו פעילות ליזוזומלית מוגברת — סימן לאקטיביות חידוש. צביעות מפורטות חשפו יותר תאים הנושאים סמני בגרות של תאי חילוף גז, מה שמעיד כי שתיקת FUS לא רק הרגיעה פיברובלסטים אלא גם עודדה את האפיתל הפגוע לבנות משטח בריא יותר. 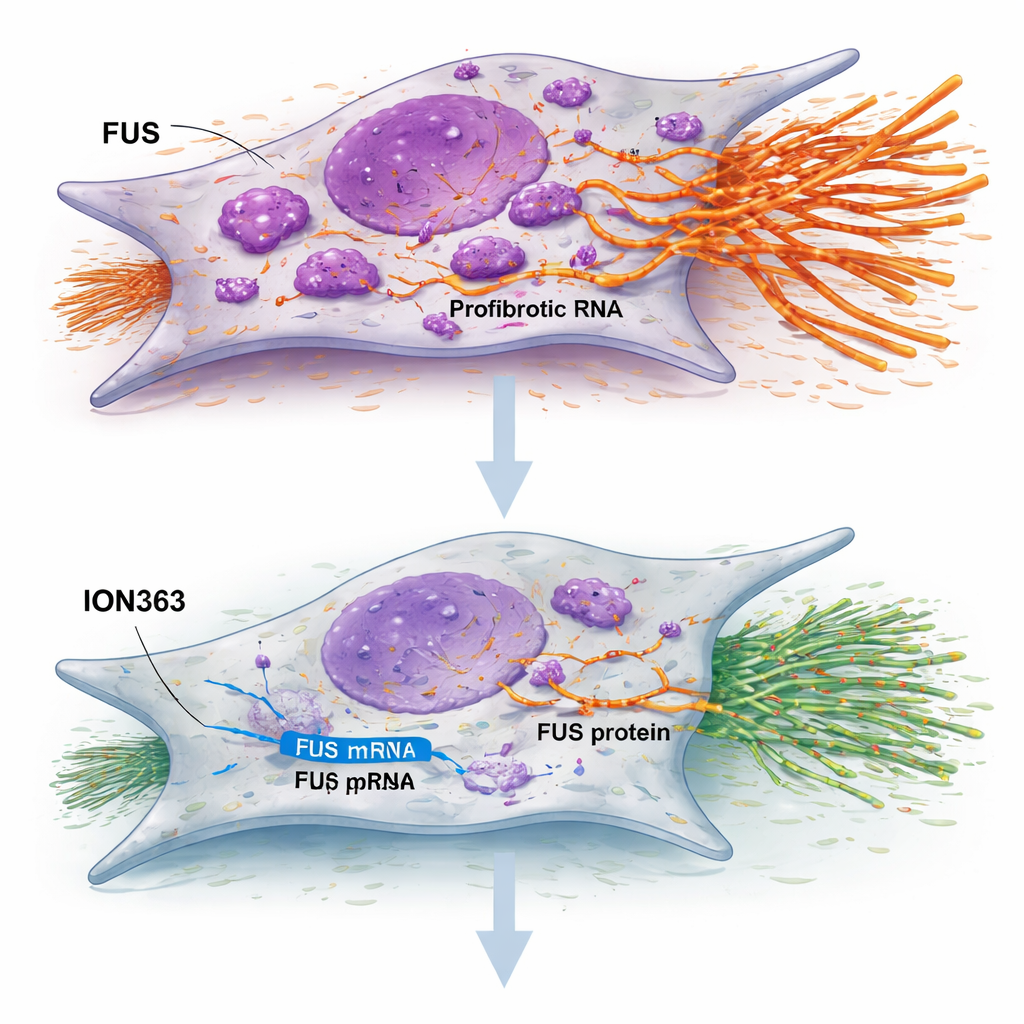
מה זה יכול למשמעות עבור חולים
לסיכום, העבודה מציירת את FUS כמפתח מרכזי ב‑IPF שמקשר בין פיברובלסטים פעילי‑יתר היוצרים צלקת לבין כשל בתיקון הנימיות העדינות. על ידי השתקת FUS בעזרת תרופת אנטיסנס ממוקדת, החוקרים הצליחו להקטין תכניות גנטיות פרו‑פיברוטיות, להקל על הצטברות קולגן ולעודד רגנרציה במודלים ריאתיים שמקורם בחולים. למרות שהגישה עדיין נמצאת בשלב מעבדה ותדרוש בדיקות קפדניות במודלים חייתיים וניסויים קליניים, היא מציעה כי בעתיד ייתכן שניתן יהיה לטפל ב‑IPF לא רק על‑ידי האטת הצלקתיות, אלא גם על‑ידי איזון ישיר של התכניות התאית השולטות בפגיעה ובתיקון הריאה.
ציטוט: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
מילות מפתח: פיברוזיס ריאתי אידיופטי, אוליגונוקלאוטיד אנטיסנס, חלבון FUS, צלקתיות ריאה, תיקון אלוואולרי