Clear Sky Science · fr
Technologies de détection multimodale pour la biosurveillance de l’IAHP dans les systèmes de production avicole
Pourquoi la grippe aviaire dans les élevages concerne tout le monde
La grippe aviaire hautement pathogène, souvent appelée IAHP ou grippe aviaire, n’est plus seulement un problème pour les poulets des fermes lointaines. Les récentes vagues du virus H5N1 ont décimé plus de 168 millions d’oiseaux aux États-Unis, fait flambées les prix des œufs et se sont même propagées aux bovins laitiers et à des personnes. Cet article de synthèse explique comment de nouvelles technologies de détection « intelligentes » — écouter les sons des animaux, prélever l’air des bâtiments et réaliser des tests génétiques rapides sur place — pourraient repérer les foyers plus tôt, protéger l’approvisionnement alimentaire et réduire le risque qu’un virus dangereux adapte sa transmission pour se propager facilement entre humains.
La menace croissante dans les élevages et chez l’humain
Ces dernières années, une nouvelle branche du virus H5N1 (clade 2.3.4.4b) s’est largement propagée au sein de la volaille américaine et, plus récemment, des troupeaux laitiers. Chaque foyer oblige les éleveurs à abattre des cheptels entiers, entraînant des pertes dépassant 1,4 milliard de dollars et des chutes soudaines de l’offre en œufs et en viande. Parallèlement, plus de 70 infections humaines ont été enregistrées aux États-Unis, principalement chez des travailleurs à faibles revenus qui manipulent des animaux infectés et ont souvent un accès limité aux soins. Les cartes et données de surveillance montrent que les vagues de H5N1 chez les oiseaux se superposent souvent aux pics hivernaux habituels de la grippe saisonnière chez l’humain, créant un paysage de risque partagé à la frontière animal–humain. Cette superposition rend d’autant plus important le suivi de ce qui se passe dans les bâtiments et les pâturages, ainsi que dans les cliniques.
Comment ce virus fonctionne et pourquoi il se propage si facilement
Les virus de la grippe aviaire sont de petits particules enveloppées qui portent leur matériel génétique sur huit segments d’ARN séparés. Deux protéines de surface, l’hémagglutinine (H) et la neuraminidase (N), donnent des appellations familières comme H5N1 ou H3N2 et déterminent quelles espèces le virus peut infecter et la gravité de la maladie. Les souches faiblement pathogènes restent principalement dans l’appareil digestif et les voies respiratoires des oiseaux et provoquent souvent peu de signes visibles. En revanche, les souches hautement pathogènes comme le H5N1 actuel possèdent un « site de clivage » particulier sur la protéine H qui permet au virus de se multiplier dans tout l’organisme, entraînant une mort subite chez 90–100 % des oiseaux affectés. Le génome segmenté facilite également l’échange de segments entre virus issus d’hôtes différents, d’où l’inquiétude face aux infections inter-espèces chez les bovins, les chats ou la faune : chaque nouvel hôte est une occasion pour le virus d’évoluer.
Limites de la biosécurité et des tests actuels
Les entreprises avicoles appliquent déjà des règles strictes de biosécurité, notamment l’accès contrôlé, la désinfection et des inspections sanitaires visuelles. Pourtant, de gros foyers d’IAHP se déclarent même dans des exploitations respectant ces normes. Une raison est la rapidité : la surveillance traditionnelle repose sur la détection d’oiseaux malades, le prélèvement d’écouvillons et l’envoi vers un laboratoire distant pour PCR, un processus qui peut prendre deux à trois jours. Comme le H5N1 peut décimer un troupeau en près de 48 heures, ce délai laisse une fenêtre au virus pour balayer les bâtiments et se transmettre entre exploitations. Prélever suffisamment d’oiseaux dans des cheptels géants est aussi difficile, et les protocoles habituels testent rarement la poussière, l’eau ou les surfaces où le virus peut persister sans être remarqué. En conséquence, les infections précoces, les cas bénins et les faibles niveaux de contamination passent souvent entre les mailles du filet.
Écouter, renifler et voir : de nouvelles façons de détecter les foyers
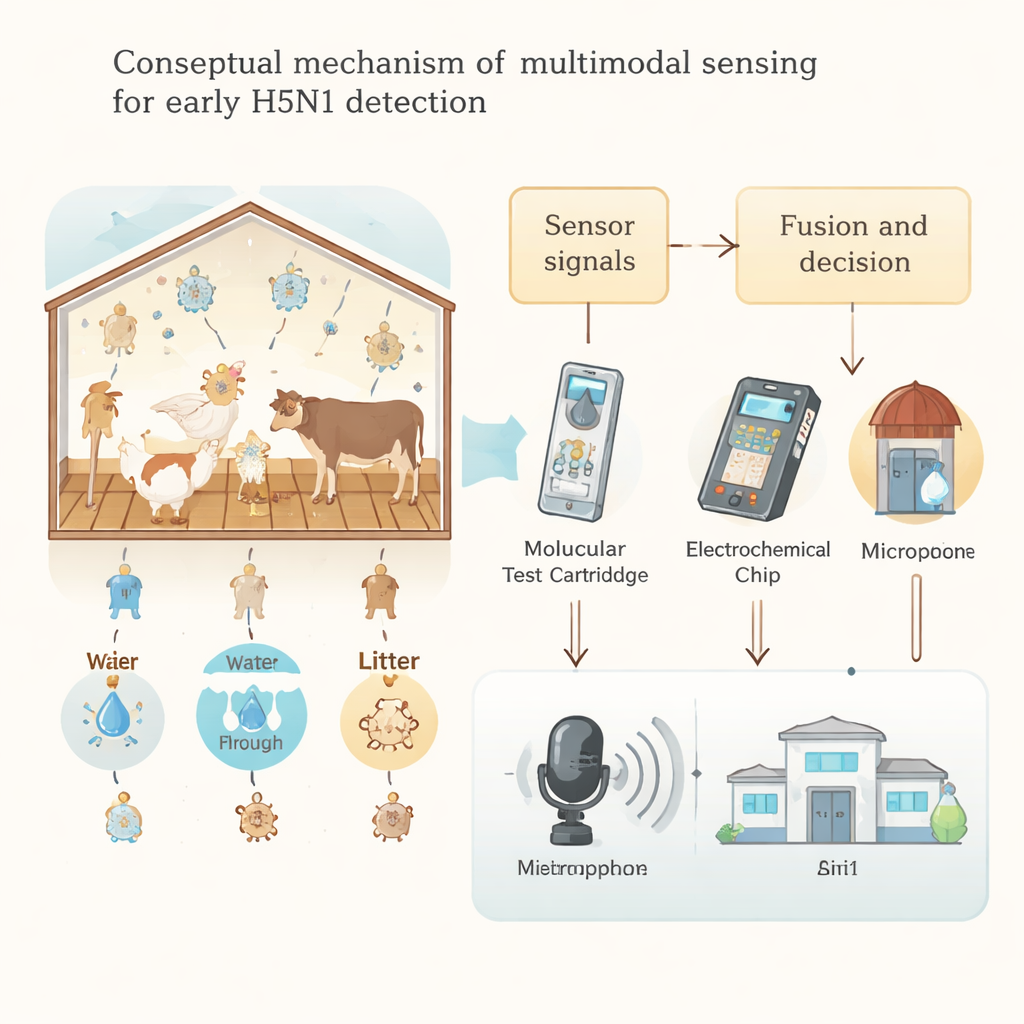
Les auteurs soutiennent que les fermes ont besoin d’une détection multimodale — plusieurs moyens complémentaires de surveiller les signes de problème. Du côté ciblé, on trouve des outils qui recherchent directement le virus ou ses composants : des méthodes portables d’amplification de l’ARN viral à température unique, des tests programmables à base de CRISPR donnant des résultats en moins d’une heure, et des biosenseurs électrochimiques et optiques compacts capables de détecter des protéines virales dans l’air, l’eau ou des écouvillons. Du côté non ciblé, on utilise des méthodes qui cherchent des signes généraux de maladie sans identifier l’agent responsable, comme les caméras thermiques détectant la fièvre, les lasers lisant des empreintes chimiques dans la poussière de l’abri et des systèmes de microphones apprenant les motifs sonores des cheptels sains et malades. Par exemple, des modèles d’apprentissage profond peuvent détecter des changements subtils dans les vocalisations de poules un à deux jours avant l’apparition de signes évidents, tandis que des méthodes avancées de diffusion lumineuse peuvent distinguer des molécules liées au virus dans des aérosols mêlés à la poussière ordinaire des bâtiments.
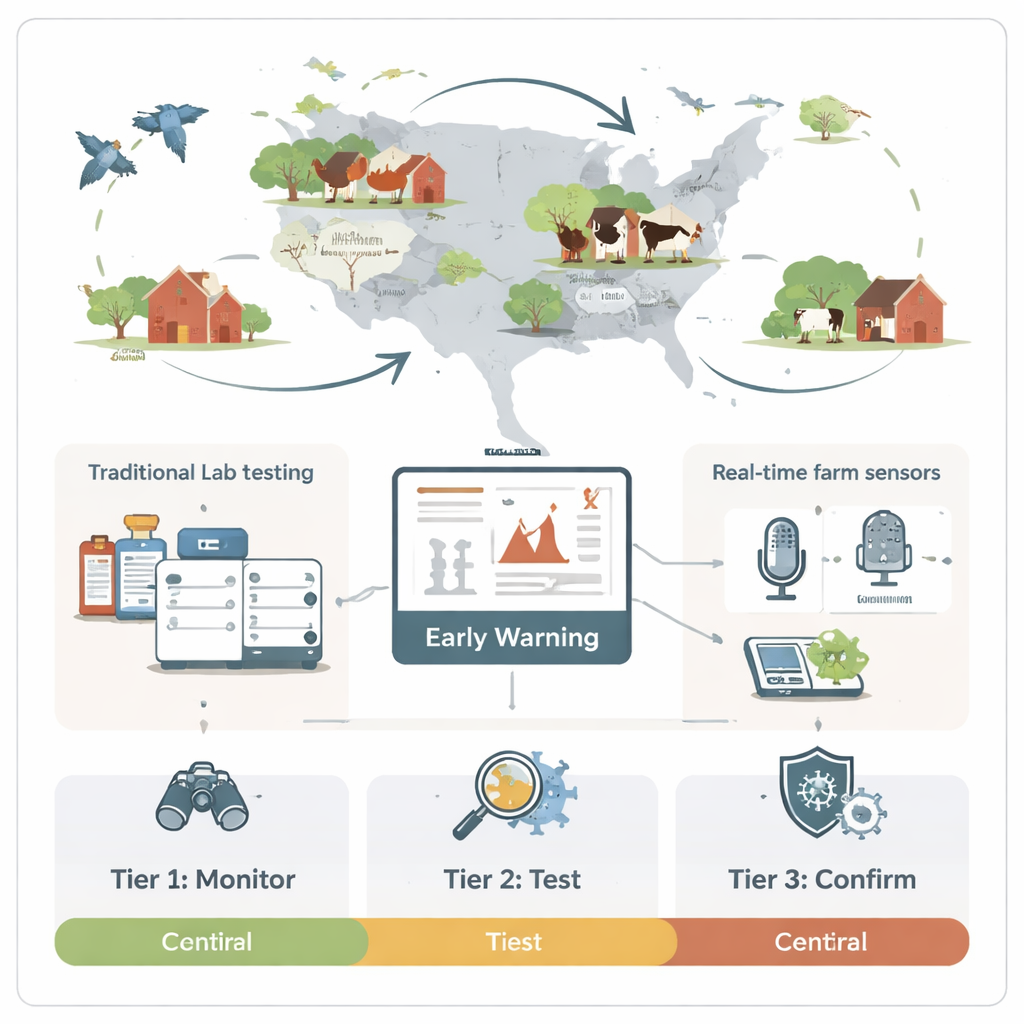
Construire un système d’alerte précoce en niveaux
Plutôt que d’utiliser tous les outils partout, la revue propose un système à trois niveaux. Au niveau 1, des capteurs peu coûteux fonctionnent en continu en arrière-plan, détectant des toux anormales, suivant les particules en suspension ou analysant la poussière pour repérer des signatures chimiques suspectes. Si ces alarmes larges dépassent un seuil, le niveau 2 s’enclenche : des tests moléculaires rapides sur place et des biosenseurs vérifient des échantillons ciblés comme des concentrés d’air ou des écouvillons, généralement en 30–60 minutes. Ce n’est qu’à la suite de ces dépistages rapides suggérant un danger réel que le niveau 3 démarre, avec des tests de confirmation en laboratoire tels que des panels PCR complets ou l’isolement viral qui prennent un jour ou plus. Cette approche progressive équilibre rapidité et fiabilité, réduisant la panique liée aux fausses alertes tout en gagnant un temps précieux par rapport à l’attente de la mort des oiseaux ou de la chute visible de la santé des travailleurs.
Ce que cela signifie pour la sécurité alimentaire et sanitaire
En termes simples, l’article conclut que combattre la grippe aviaire moderne exige que les fermes se comportent davantage comme des usines intelligentes que comme des hangars isolés. En combinant des oreilles (surveillance acoustique), des nez (capteurs chimiques et moléculaires) et des cerveaux (algorithmes de fusion de données) à travers les secteurs de la santé animale, environnementale et humaine, l’agriculture peut passer de la réaction aux catastrophes à l’anticipation. Une détection plus précoce signifie moins d’abattages massifs, des prix plus stables pour les œufs, la viande et le lait, et de moindres chances que le H5N1 acquière les bonnes mutations pour déclencher une pandémie humaine. Il reste des obstacles — coût des technologies, formation des travailleurs et difficulté de combiner des données bruitées provenant de capteurs très différents — mais la détection multimodale offre une voie réaliste vers des fermes plus sûres et une surveillance One Health renforcée pour tous.
Citation: Ali, M.A., Ataei Kachouei, M., Jacobs, L. et al. Multimodal sensing technologies for HPAI biosurveillance in poultry production systems. npj Biosensing 3, 11 (2026). https://doi.org/10.1038/s44328-025-00075-6
Mots-clés: grippe aviaire, biosenseurs, surveillance des exploitations, diagnostics CRISPR, surveillance acoustique