Clear Sky Science · fr
Perspectives unicellulaires sur l'hétérogénéité trophoblastique et la dysfonction adaptative dans le retard de croissance fœtale sélectif
Quand un jumeau prend du retard
Pour des parents attendant des jumeaux, il est profondément inquiétant qu’un des bébés cesse de grandir aussi bien que l’autre, alors qu’ils partagent le même utérus et le même placenta. Cette affection, appelée retard de croissance fœtale sélectif, met non seulement en danger la santé du jumeau plus petit avant la naissance, mais peut aussi influencer le développement à long terme. Cette étude utilise des analyses unicellulaires de pointe pour scruter le placenta partagé dans ces grossesses gémellaires, révélant comment de petites modifications dans des cellules placentaires spécifiques et dans les réponses immunitaires peuvent faire basculer l’équilibre entre une croissance saine et une carence dangereuse.
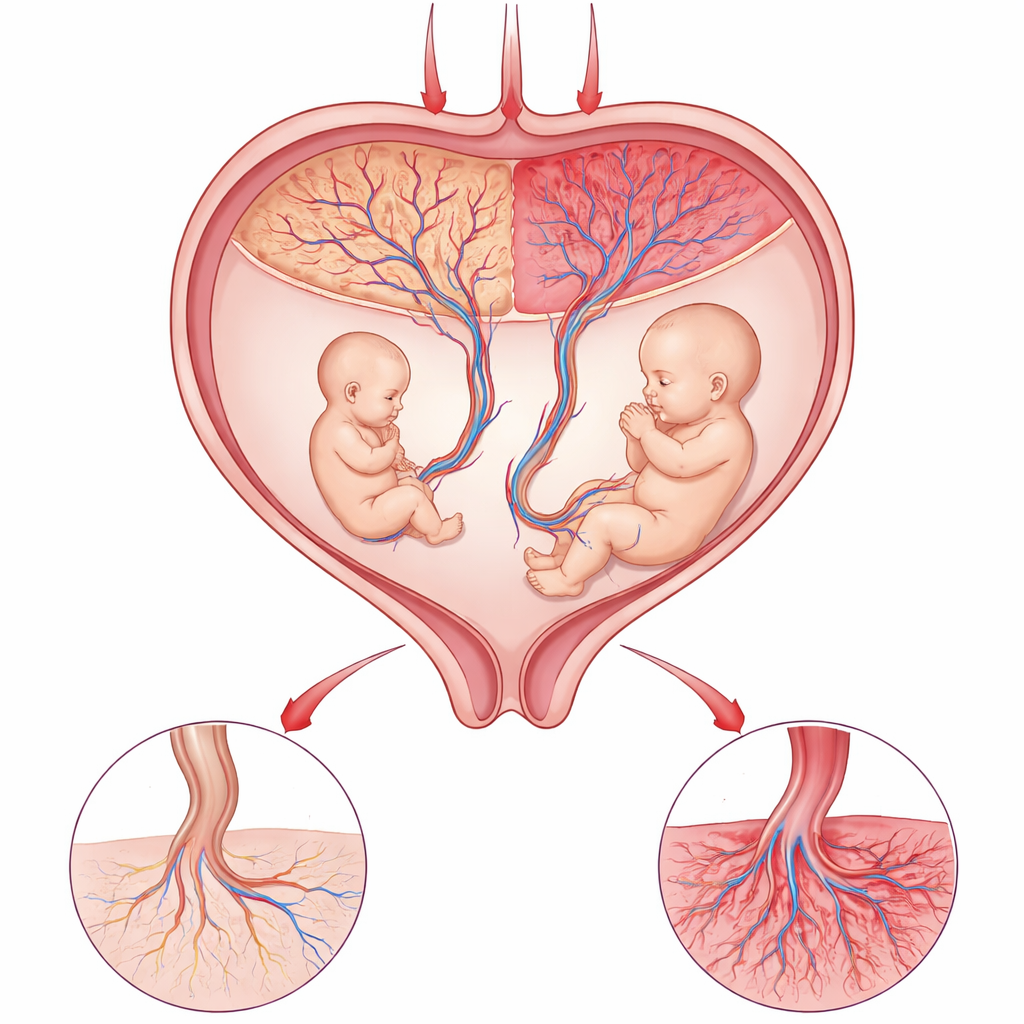
Le fragile jeu d’équilibre du placenta
Le placenta est la ligne de vie entre la mère et le bébé, apportant l’oxygène et les nutriments tout en éliminant les déchets. Dans certaines grossesses de jumeaux monozygotes, les deux bébés partagent un seul placenta mais occupent des territoires différents à l’intérieur de celui-ci. Lorsqu’un jumeau devient nettement plus petit que l’autre, les cliniciens savent qu’un dysfonctionnement local s’est produit dans cet organe partagé. Parce que les jumeaux ont la même mère et des gènes presque identiques, ils constituent une expérience naturelle puissante : toute différence majeure de croissance provient probablement du fonctionnement des parties respectives du placenta, plutôt que de différences propres aux bébés.
Approche à l’échelle cellulaire du placenta
Les chercheurs ont prélevé des échantillons placentaires de trois grossesses dans lesquelles un jumeau était significativement plus petit que l’autre. En utilisant le séquençage ARN unicellulaire — une méthode qui mesure l’activité de milliers de gènes dans des cellules individuelles — ils ont profilé plus de 175 000 cellules provenant des différentes régions du placenta. Cela leur a permis de classer les cellules en types distincts, incluant des cellules de soutien, des cellules vasculaires et plusieurs types de cellules immunitaires. Ils se sont concentrés sur un groupe clé appelé cytotrophoblastes villositaires, une couche de cellules qui tapisse les petites projections en forme de doigt où le sang maternel rencontre la circulation fœtale et qui renouvelle et répare en permanence la surface du placenta.
Deux états cellulaires clés : structure versus mode survie
Au sein de ces cytotrophoblastes villositaires, l’équipe a identifié deux états principaux avec des rôles très différents. Un groupe, marqué par une molécule appelée TP63, jouait le rôle de gardiens structurels : ils soutenaient la barrière mère‑bébé, maintenaient les jonctions entre cellules et contribuaient à l’organisation tissulaire. L’autre groupe, marqué par une enzyme appelée LDHA, était orienté vers une production d’énergie intense et la gestion du stress, activant des voies liées aux mitochondries, au stress oxydatif et à la qualité des protéines. Dans les territoires placentaires du jumeau plus petit, les cellules protectrices TP63 étaient raréfiées, tandis que les cellules stressées de type LDHA s’étendaient et présentaient un cycle cellulaire plus actif. Une analyse informatique des trajectoires suggérait que les cellules étaient poussées le long d’un chemin allant de fonctions structurelles saines vers un mode survie, avec moins de cellules atteignant l’état fusionné complet qui maintient normalement une surface d’échange lisse et efficace.
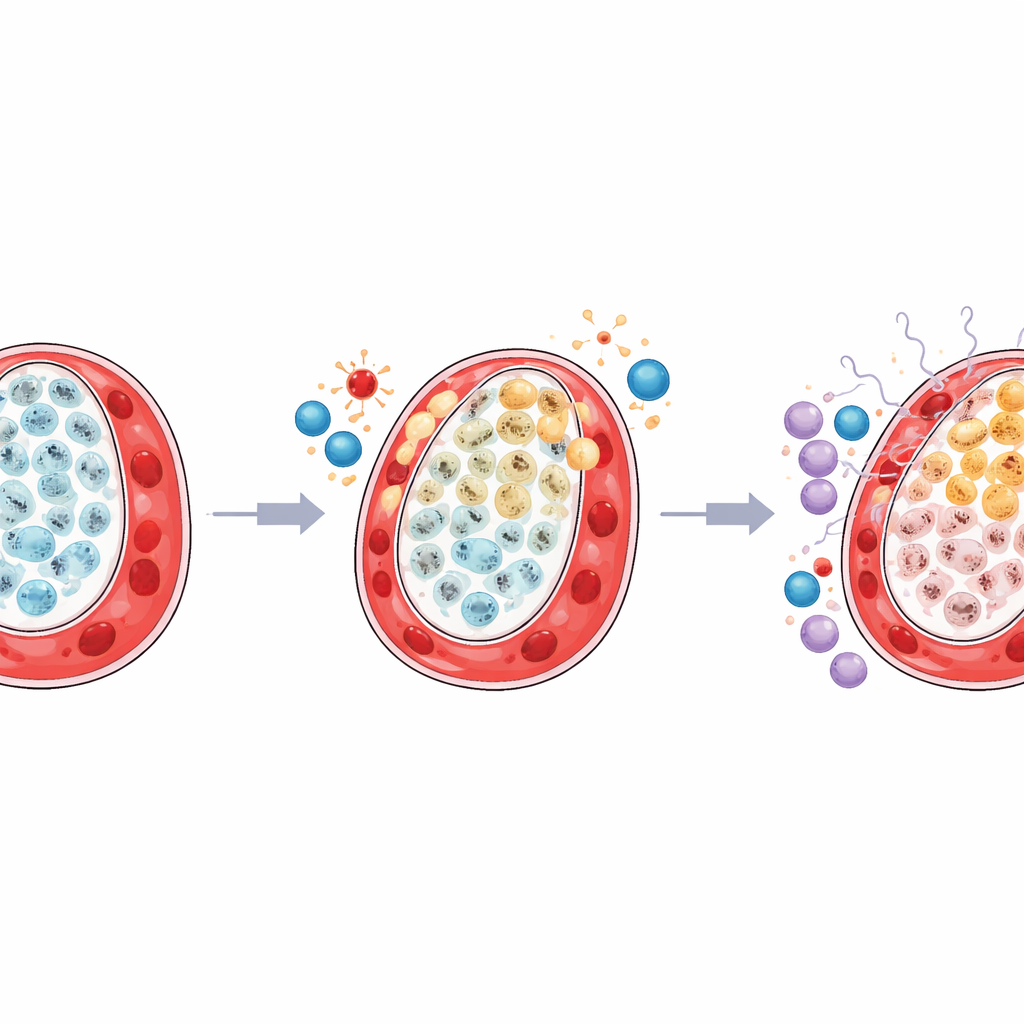
Un environnement inflammatoire autour des cellules stressées
L’étude a également montré que l’environnement immunitaire entourant le territoire placentaire du jumeau plus petit était remanié de manière délétère. Un type utile de macrophage résidant, connu sous le nom de cellules de Hofbauer, qui soutient habituellement la santé tissulaire et gère le métabolisme, était réduit en nombre. Parallèlement, certaines cellules tueuses naturelles, préparées aux réponses antivirales et inflammatoires, devenaient plus nombreuses et plus actives. Une cartographie détaillée des signaux échangés entre cellules a montré que les trophoblastes stressés de type LDHA interagissaient plus fortement avec les cellules immunitaires via des voies dominées par l’interféron et des molécules d’alerte apparentées. Pendant ce temps, la communication entre les cellules structurelles TP63 et les cellules stromales et vasculaires de soutien s’affaiblissait, suggérant une perte à la fois du soutien physique et d’une régulation immunitaire apaisante.
Une défaillance en trois volets qui limite la croissance fœtale
Pris ensemble, les résultats dessinent un tableau clair et accessible de ce qui tourne mal dans le placenta lorsqu’un jumeau prend du retard. Les cellules de soutien structurel qui maintiennent la surface d’échange compacte et ordonnée s’épuisent, les cellules stressées avides d’énergie prennent le relais, et le système immunitaire bascule vers un état plus inflammatoire. Ces trois éléments — perte de structure, surcharge métabolique et inflammation chronique — se renforcent mutuellement et sapent progressivement la capacité du placenta à fournir suffisamment d’oxygène et de nutriments au bébé plus petit. En identifiant précisément les types cellulaires et les voies de signalisation impliqués, cette étude fournit une feuille de route pour des tests et traitements futurs visant à détecter plus tôt les problèmes placentaires et, peut‑être, à ramener ces cellules vers un équilibre plus sain.
Citation: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Mots-clés: placenta, grossesse gémellaire, retard de croissance fœtale, séquençage ARN unicellulaire, cellules trophoblastiques