Clear Sky Science · fr
Analyse protéomique des vésicules extracellulaires issues des tissus révèle des changements moléculaires région‑spécifiques dans un modèle rongeur du syndrome de takotsubo
Quand le stress laisse une empreinte cardiaque temporaire
La plupart des gens associent une crise cardiaque à des lésions permanentes, mais il existe une affection intrigante où le cœur s’affaiblit soudainement puis se rétablit en grande partie en quelques jours ou semaines. On parle de syndrome de takotsubo, souvent déclenché par un stress émotionnel ou physique intense. L’étude résumée ici explore de minuscules « bulles » biologiques envoyées par les cellules cardiaques dans un modèle de rat de ce syndrome, révélant comment différentes régions du cœur réagissent chacune à leur manière à une brutale tempête d’hormones de stress.
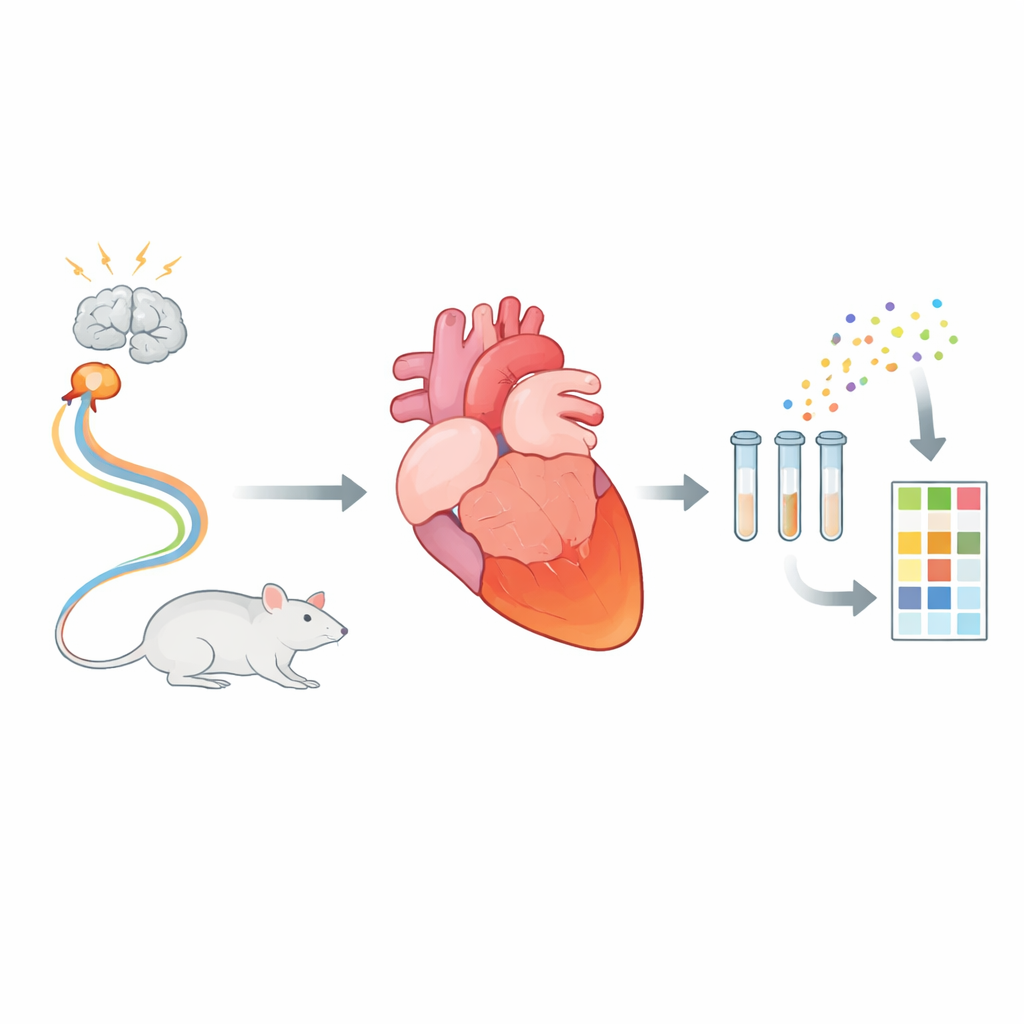
Une insuffisance cardiaque temporaire soulevant des questions durables
Le syndrome de takotsubo imite une crise cardiaque classique : les patients arrivent avec des douleurs thoraciques, des électrocardiogrammes alarmants et une fonction de pompage réduite. Pourtant, leurs artères coronaires ne sont pas obstruées, et les régions cardiaques affectées récupèrent généralement. Un motif caractéristique est que l’apex du ventricule gauche devient quasi immobile, tandis que la base continue de se contracter. Malgré une reconnaissance croissante, la « conversation » biologique entre cellules cardiaques stressées — comment elles signalent détresse, dommage et réparation — reste mal comprise. Les chercheurs ont utilisé un modèle de rat bien établi qui reproduit fidèlement les caractéristiques humaines du takotsubo après une dose contrôlée d’un médicament mimant le stress, en examinant le cœur 24 heures après, au début de la phase de récupération.
De minuscules bulles qui portent des messages cardiaques
Toutes les cellules du corps libèrent des paquets nanoscopiques appelés vésicules extracellulaires. Ces bulles entourées d’une membrane transportent des protéines, des lipides et du matériel génétique capables d’altérer le comportement de cellules voisines ou distantes. En cardiologie, ces vésicules peuvent aggraver les lésions en alimentant l’inflammation ou favoriser la réparation en soutenant la néovascularisation et la restauration tissulaire. Dans ce travail, les scientifiques ont isolé avec soin des vésicules directement depuis l’apex et la base des cœurs de rats, plutôt que depuis le sang. Par microscopie électronique, suivi de particules et marqueurs protéiques, ils ont confirmé obtenir des préparations propres de vésicules typiques, de l’ordre de 50 à 400 nanomètres. Fait important, seule la région apicale stressée dans les cœurs takotsubo produisait moins de vésicules, tandis que la base intacte et les cœurs normaux en libéraient des nombres similaires, suggérant une réponse au stress spécifique à la région.
Deux moitiés du cœur, deux récits moléculaires
L’équipe a ensuite appliqué la protéomique à haute résolution, une technique qui catalogue et quantifie des milliers de protéines simultanément. Au total, ils ont identifié un peu plus de 2 000 protéines à l’intérieur des vésicules. Dans les cœurs sains, les vésicules issues de l’apex et de la base se ressemblaient remarquablement, suggérant un profil de communication « de base » uniforme. Après le stress, cependant, les vésicules de la région apicale ont changé de façon spectaculaire, tandis que celles de la base ont à peine évolué. Des centaines de protéines étaient modifiées dans les vésicules apicales comparées à l’apex sain et à la base stressée. Beaucoup des protéines les plus augmentées étaient liées au système immunitaire et à l’inflammation, tandis que nombre des protéines diminuées soutenaient la fonction mitochondriale — les centrales énergétiques de la cellule. Des analyses réseau et de voies avancées ont pointé de façon cohérente vers un schéma organisé : un métabolisme énergétique diminué associé à une activité immunitaire et de remodelage tissulaire accrue dans le segment lésé.
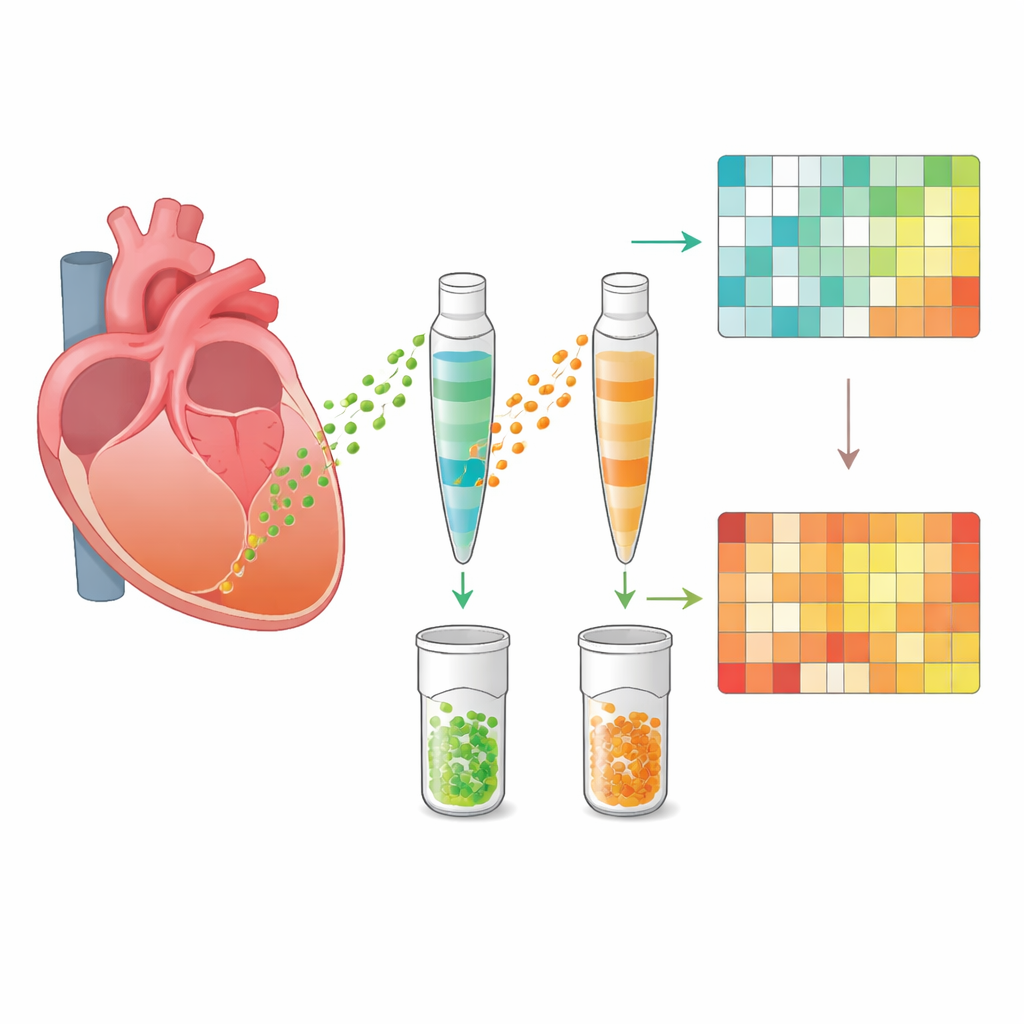
Inflammation, lipides et signaux de réparation
En examinant de plus près les réseaux protéiques interconnectés, les chercheurs ont observé que les protéines impliquées dans le traitement des lipides étaient étroitement liées à celles portant l’inflammation. Cela concorde avec des observations antérieures selon lesquelles des gouttelettes lipidiques et un œdème apparaissent rapidement après le stress, suivis par l’infiltration de cellules immunitaires puis des modifications cicatricielles. Les vésicules de l’apex affecté étaient enrichies en protéines associées à la coagulation sanguine, à l’angiogenèse et à la formation de collagène — caractéristiques à la fois de la réparation et de la cicatrisation. Parallèlement, elles contenaient des protéines appartenant à des voies de signalisation de survie clés, notamment les voies MAPK, qui aident les cellules à résister aux blessures et peuvent soutenir la capacité du cœur à retrouver sa force de contraction. Dans l’ensemble, le contenu des vésicules dessinait le portrait d’une région cardiaque en situation de pénurie énergétique, d’une inflammation active, d’un remodelage structurel et d’efforts de préservation.
Ce que cela signifie pour les patients et les soins futurs
Cette étude est la première à cartographier en détail le contenu protéique des vésicules libérées depuis différentes régions du cœur dans le syndrome de takotsubo. Pour le non‑spécialiste, le message central est que la pointe assommée du cœur n’attend pas passivement de récupérer ; elle est animée d’une intense activité moléculaire, émettant de minuscules paquets signalant stress énergétique, inflammation, réparation tissulaire et survie. Ces vésicules pourraient un jour servir de marqueurs sanguins sensibles pour diagnostiquer le takotsubo, le distinguer d’un infarctus ou identifier les patients à risque de récupération plus lente. Elles pourraient aussi mettre en lumière de nouvelles cibles thérapeutiques — des voies à moduler pour réduire l’inflammation nuisible ou favoriser une réparation saine. Bien que le travail ait été réalisé chez des rats mâles à un seul point temporel et reste exploratoire, il ouvre une nouvelle fenêtre sur la façon dont le cœur stressé communique avec lui‑même pendant cette forme mystérieuse, généralement réversible, d’insuffisance cardiaque.
Citation: Zulfaj, E., Nejat, A., Kalani, M. et al. Proteomic analysis of tissue-derived extracellular vesicles shows region-specific molecular changes in a rat model of takotsubo syndrome. Sci Rep 16, 8731 (2026). https://doi.org/10.1038/s41598-026-42812-5
Mots-clés: syndrome de takotsubo, vésicules extracellulaires, stress cardiaque, protéomique, inflammation cardiaque