Clear Sky Science · fr
Effet potentiel bénéfique gonadique de la sitagliptine contre la dysfonction testiculaire induite par le paclitaxel via la médiation de la voie de signalisation PERK/CHOP/NLRP3/Sestrin2
Pourquoi cette étude importe pour les patients atteints de cancer
La chimiothérapie sauve des vies mais peut discrètement endommager la fertilité, en particulier chez les hommes. Un médicament anticancéreux largement utilisé, le paclitaxel, est connu pour nuire aux testicules et diminuer la qualité du sperme. Cette étude réalisée chez le rat pose une question pratique à portée humaine claire : une pilule antidiabétique déjà approuvée, la sitagliptine, pourrait‑elle être réutilisée pour protéger le système reproducteur masculin des effets secondaires du paclitaxel sans interférer avec son rôle anticancéreux ?
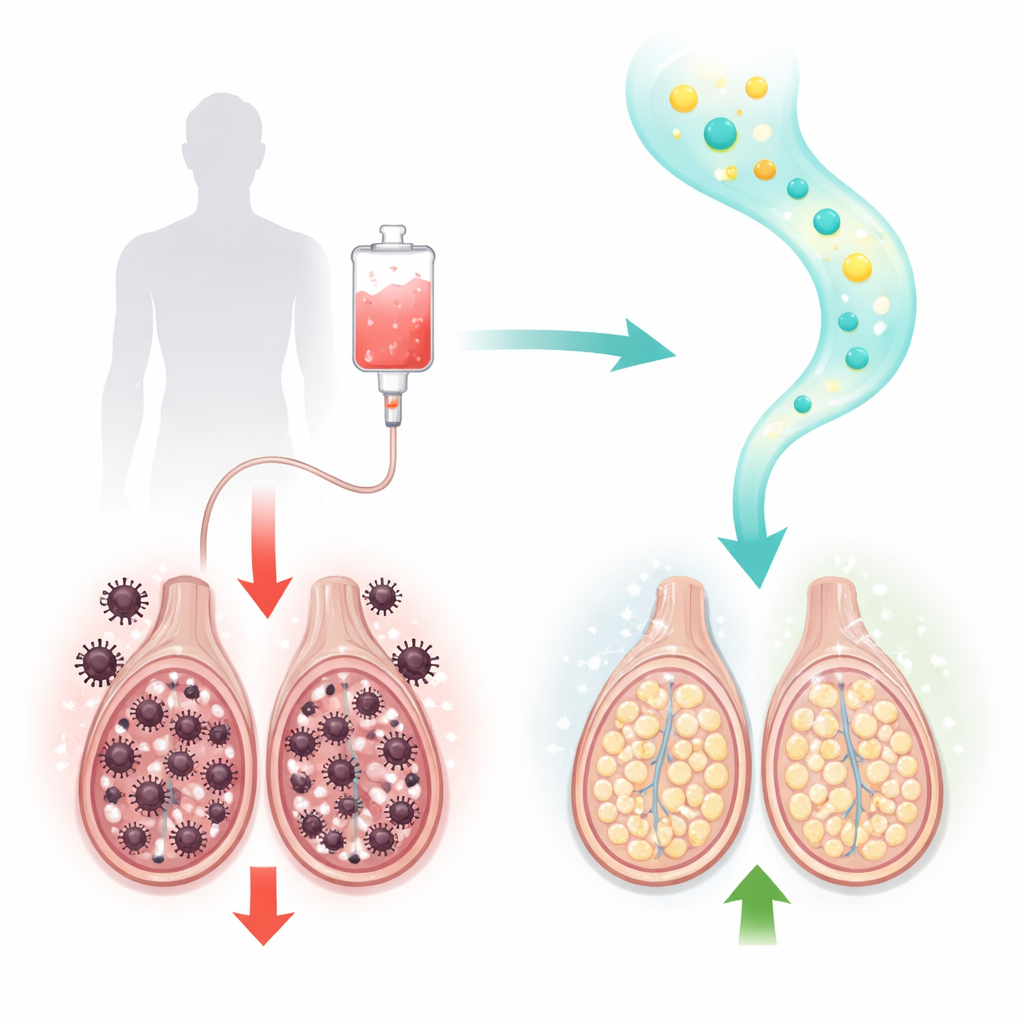
Un médicament anticancer courant au coût caché
Le paclitaxel est un traitement de référence pour les cancers du sein, de l’ovaire, du poumon et d’autres tumeurs solides. Il agit en bloquant la machinerie de division cellulaire des cellules cancéreuses à prolifération rapide. Malheureusement, les cellules en division des organes sains sont aussi vulnérables. Chez le rat mâle, le traitement par paclitaxel a entraîné des signes classiques de lésion testiculaire : le nombre, la mobilité et la viabilité des spermatozoïdes ont fortement chuté, tandis que la fréquence de spermatozoïdes malformés a augmenté. Au microscope, les chercheurs ont observé des tubes séminifères endommagés (lieu de fabrication des spermatozoïdes) et des cellules de Leydig produisant des hormones lésées, ainsi qu’un amaigrissement des couches tissulaires. Les analyses sanguines ont confirmé une nette baisse de la testostérone et d’une enzyme clé nécessaire à sa synthèse, la 17β‑hydroxystéroïde déshydrogénase.
Un médicament contre le diabète comme protecteur inattendu
La sitagliptine est largement prescrite pour contrôler la glycémie chez les personnes atteintes de diabète de type 2. Des travaux antérieurs suggéraient qu’au‑delà de ses effets métaboliques, la sitagliptine peut atténuer le stress oxydatif nocif, l’inflammation et la mort cellulaire dans des organes tels que le foie, le rein et le cerveau. S’appuyant sur cela, les chercheurs ont réparti des rats mâles en quatre groupes : témoins non traités, groupe traité uniquement au paclitaxel, et deux groupes ayant reçu le paclitaxel plus une dose faible ou élevée de sitagliptine pendant deux semaines. Ils ont ensuite comparé la qualité du sperme, les niveaux hormonaux, la structure tissulaire et un ensemble de « systèmes d’alerte » moléculaires à l’intérieur des testicules qui détectent le stress et déclenchent l’inflammation et l’autodestruction cellulaire.
Comment la sitagliptine a calmé le stress cellulaire et l’inflammation
Le paclitaxel a poussé les testicules dans un état de stress oxydatif et endoplasmique : les niveaux de produits toxiques (mesurés par le malondialdéhyde) ont augmenté, tandis que les défenses naturelles telles que le glutathion réduit et l’enzyme catalase ont diminué. Au cœur des cellules, l’usine de repliement des protéines — le réticulum endoplasmique — a activé une voie de danger appelée PERK–CHOP, signalant qu’un stress prolongé fait basculer les cellules vers la mort. Parallèlement, un complexe protéique inflammatoire (NLRP3) est devenu très actif, augmentant des médiateurs inflammatoires comme l’interleukine‑1β et activant une cascade de protéines de mort cellulaire, y compris le cytochrome c et la caspase‑3. La sitagliptine a inversé une grande partie de ces effets. Les deux doses ont réduit les dommages oxydatifs et restauré les défenses antioxydantes. Elles ont nettement diminué l’activation de la voie de stress PERK–CHOP et freiné l’inflammation et l’apoptose pilotées par NLRP3. Une protéine protectrice appelée Sestrin2, qui aide à éliminer les molécules réactives et a été associée à un sperme plus sain, a été augmentée par la sitagliptine au niveau génique et protéique.
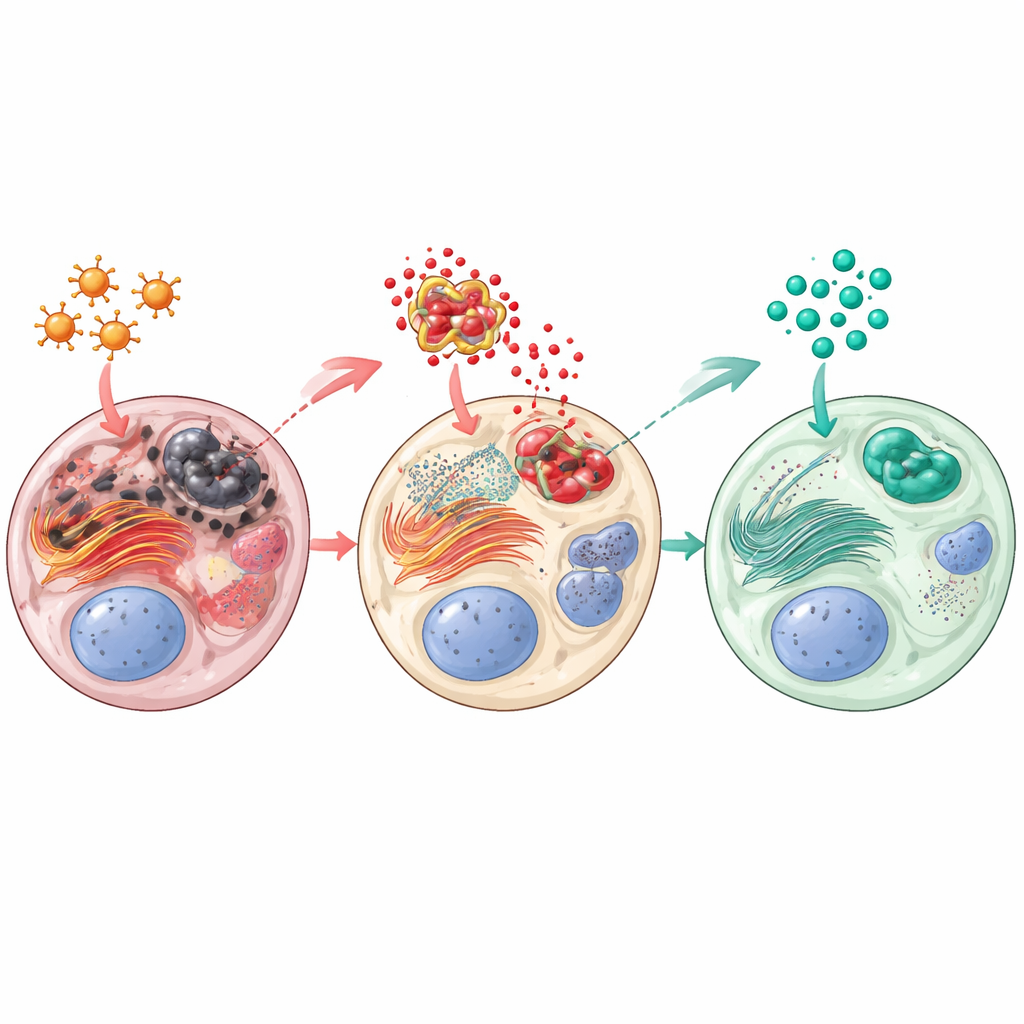
Un sperme meilleur, des tissus plus sains, des hormones renforcées
Les améliorations biochimiques se sont traduites par des bénéfices fonctionnels tangibles. Les rats recevant de la sitagliptine après le paclitaxel présentaient des numérations spermatiques plus élevées, une meilleure motilité et moins de spermatozoïdes anormaux que les animaux traités uniquement au paclitaxel, la dose élevée de sitagliptine se rapprochant le plus de la normale. La testostérone et la 17β‑hydroxystéroïde déshydrogénase ont rebondi, suggérant une récupération de la production stéroïdienne par les cellules de Leydig. Au microscope optique et électronique, les testicules traités par sitagliptine montraient des tubes séminifères plus ordonnés, plus de cellules de Leydig, des couches cellulaires plus épaisses et plus saines, et moins de distorsions structurelles. Globalement, le médicament a contribué à préserver l’architecture et la fonction nécessaires à la production continue de spermatozoïdes.
Ce que cela pourrait signifier pour les hommes sous chimiothérapie
Ces travaux sur l’animal suggèrent que la sitagliptine peut atténuer de manière significative les dommages testiculaires induits par le paclitaxel en calmant un réseau de signaux nocifs — stress oxydatif, stress du repliement des protéines, inflammation et mort cellulaire programmée — principalement en augmentant la Sestrin2 et en diminuant l’axe PERK/CHOP/NLRP3. Étant donné que la sitagliptine est déjà utilisée en clinique pour le diabète, elle se distingue comme un candidat réaliste à tester comme adjonction protectrice de la fertilité chez les hommes recevant du paclitaxel, en particulier chez ceux qui sont aussi diabétiques. Les auteurs soulignent que des études chez l’homme sont encore nécessaires, mais leurs résultats ouvrent une perspective encourageante : une pilule familière pourrait un jour aider les patients atteints de cancer à préserver non seulement leur vie mais aussi leurs chances de procréation.
Citation: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Mots-clés: paclitaxel, sitagliptine, fertilité masculine, stress oxydatif, toxicité testiculaire