Clear Sky Science · fr
Une co-culture exploratoire in vitro de neurones entériques et de cellules musculaires lisses démontre la contribution neuronale à la formation de la couche musculaire
Pourquoi il est important de cultiver de nouveaux muscles intestinaux
Pour les personnes nées avec, ou qui perdent, de larges portions de l’intestin grêle, la vie quotidienne peut dépendre d’une alimentation intraveineuse parce que le segment restant ne peut pas absorber suffisamment de nutriments. Les greffes sont risquées et échouent souvent avec le temps. Cette étude explore une idée très différente : les scientifiques peuvent-ils faire pousser en laboratoire des portions fonctionnelles de muscle intestinal, dotées de leur propre « cerveau intestinal » pour coordonner le mouvement ? Si oui, cela pourrait un jour aider à fabriquer des segments intestinaux de remplacement pour les patients atteints du syndrome de l’intestin court.
Le cerveau caché dans l’intestin
La paroi intestinale est plus qu’un simple tube. Elle contient des couches de muscle lisse qui comprimment rythmiquement les aliments, guidées par un réseau dense de nerfs appelé système nerveux entérique, parfois surnommé le « cerveau dans l’intestin ». Lorsque ces nerfs sont absents ou endommagés, comme dans la maladie de Hirschsprung ou après une chirurgie majeure, la couche musculaire seule ne peut pas propulser correctement les aliments. Les auteurs ont estimé que tout tissu de remplacement cultivé en laboratoire doit donc inclure à la fois des cellules musculaires et des cellules nerveuses entériques, et non pas seulement l’un ou l’autre, et se sont attelés à construire un modèle épuré ne contenant que ces deux acteurs essentiels.
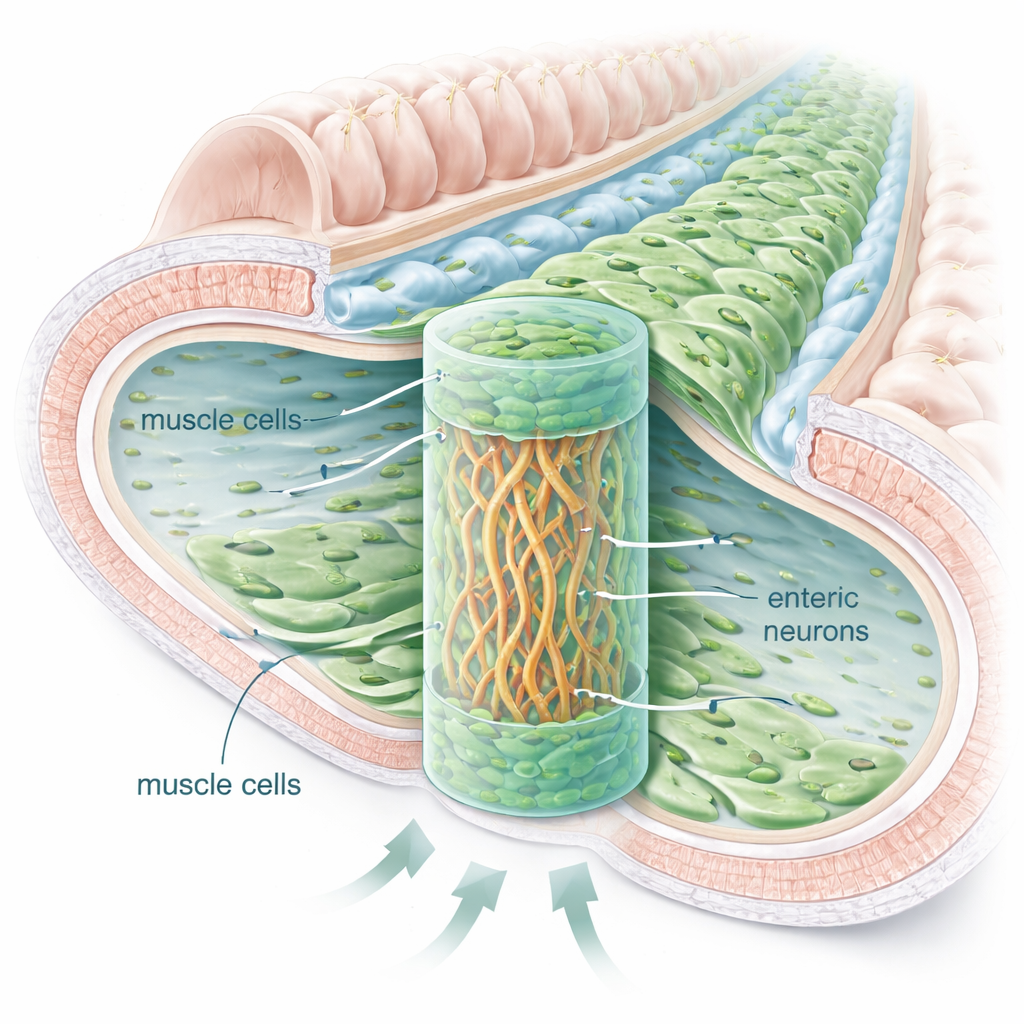
Construire une mini-paroi intestinale dans un gel
L’équipe a isolé des cellules nerveuses entériques chez de jeunes rats et les a combinées avec des cellules musculaires lisses intestinales d’origine commerciale dans un échafaudage souple de type gel fabriqué à partir d’acide hyaluronique. Ils ont testé différents milieux nutritifs liquides jusqu’à en trouver un qui soutienne les deux types cellulaires, puis ont expérimenté diverses organisations tridimensionnelles. La configuration la plus réussie ressemblait à un sandwich : une bande dense de cellules nerveuses au milieu du gel, encadrée au-dessus et en dessous par des cellules musculaires lisses. Dans ce montage, les deux types cellulaires ont survécu pendant des semaines à des mois et ont formé des structures en couches rappelant la paroi intestinale naturelle.
De cellules dispersées à des fibres organisées et mobiles
La microscopie a révélé que la présence de cellules nerveuses entériques changeait profondément le comportement des cellules musculaires. Seules dans le gel, les cellules musculaires lisses restaient rondes, exprimaient faiblement leurs protéines contractiles et ne s’alignaient pas en fibres. Quand des cellules nerveuses étaient présentes à proximité ou en contact direct, les cellules musculaires s’allongeaient, s’alignaient entre elles et formaient de longs faisceaux similaires aux couches musculaires natives. Les chercheurs ont observé des réseaux de fibres nerveuses se faufilant entre les faisceaux musculaires, ainsi que des cellules gliales qui soutiennent normalement les neurones. Grâce à des marqueurs fluorescents et à la microscopie électronique, ils ont identifié des structures ressemblant à des synapses — de minuscules points de contact où les nerfs communiquent avec les cellules musculaires.
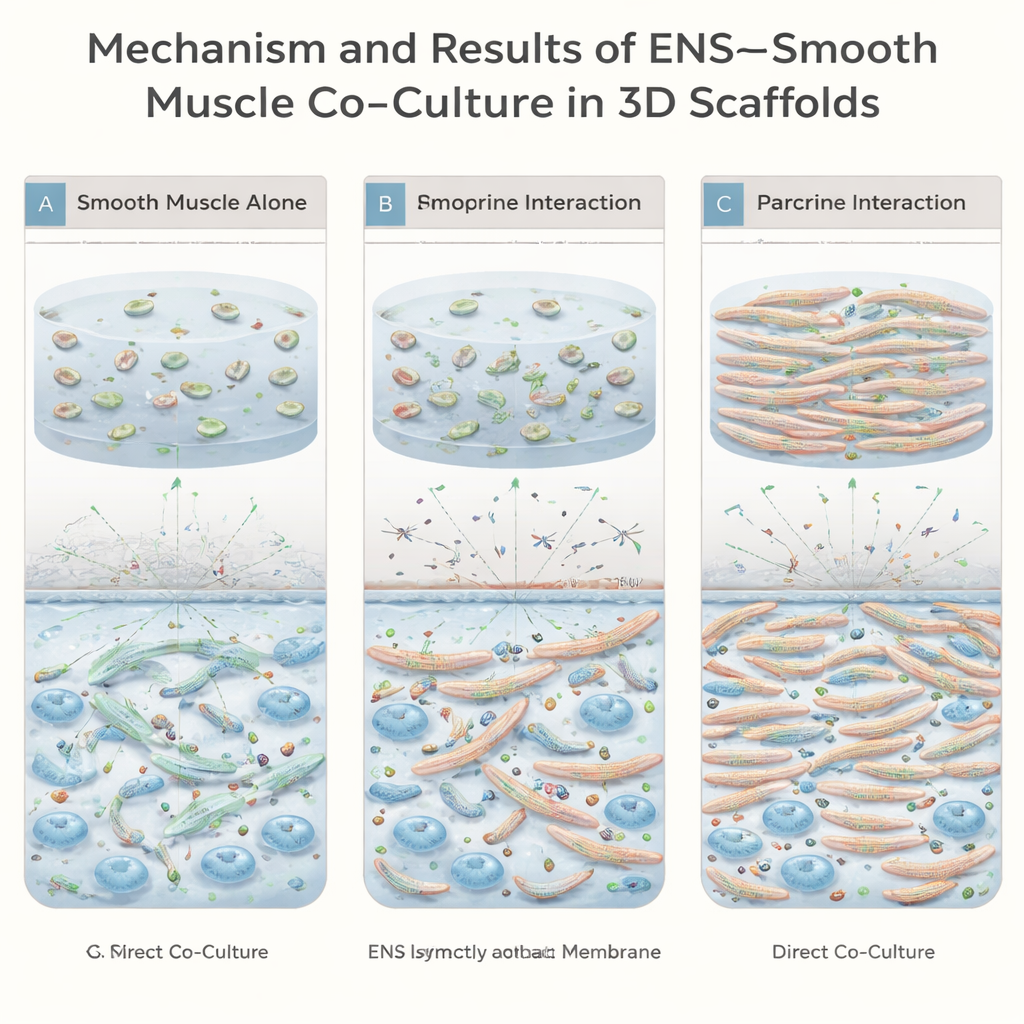
Ces fibres cultivées en laboratoire se contractent-elles réellement ?
À partir d’environ trois semaines de culture, les constructions contenant à la fois des cellules musculaires et des neurones entériques ont commencé à montrer des contractions spontanées visibles au microscope optique. Des faisceaux musculaires fins et épais se raccourcissaient et se relâchaient de façon répétée, suggérant que le tissu conçu pouvait se mouvoir activement plutôt que de rester passif dans le gel. La co-culture directe, où nerfs et muscles se touchaient au sein du même échafaudage, produisait les fibres les plus robustes et bien alignées ainsi que les réseaux nerveux les plus denses. En comparaison, lorsque les deux types cellulaires étaient séparés par une membrane ne laissant passer que des signaux solubles, des fibres musculaires se formaient mais étaient moins nombreuses, plus faibles et moins organisées.
Ce que cela signifie pour la réparation intestinale future
Ce travail ne prouve pas encore que les contractions sont entièrement contrôlées par les cellules nerveuses, et il ne recrée pas non plus la paroi intestinale complète avec son épithélium et ses cellules immunitaires. Néanmoins, il fournit une preuve de concept claire : les cellules nerveuses entériques peuvent aider à guider les cellules musculaires lisses pour qu’elles s’organisent en faisceaux alignés et innervés qui se comportent davantage comme du muscle intestinal vivant. Pour les patients atteints du syndrome de l’intestin court, de telles couches musculaires simplifiées mais fonctionnelles sont une étape cruciale vers la construction de segments intestinaux de remplacement. Des études futures combinant ces constructions neuromusculaires avec la muqueuse intestinale et des tests plus poussés du contrôle nerveux du mouvement pourraient rapprocher l’intestin conçu par ingénierie tissulaire de la réalité clinique.
Citation: Khasanov, R., Tapia-Laliena, M.Á., Schulte, S. et al. An exploratory in vitro co-culture of enteric neurons and smooth muscle cells demonstrates neuronal contribution to muscle layer formation. Sci Rep 16, 7732 (2026). https://doi.org/10.1038/s41598-026-39409-3
Mots-clés: syndrome de l’intestin court, ingénierie tissulaire intestinale, système nerveux entérique, muscle lisse, co-culture 3D