Clear Sky Science · fr
La perturbation de l’homéostasie des neutrophiles est associée à des altérations fonctionnelles des mitochondries chez des patients COVID‑19 en état critique
Pourquoi cela compte pour les patients COVID‑19
La plupart des gens savent maintenant que le COVID‑19 dépasse l’infection pulmonaire, mais la façon dont le virus détourne les défenses de l’organisme reste en grande partie à élucider. Cette étude examine de près les neutrophiles, un type courant de globules blancs, chez des patients en soins intensifs atteints d’une forme grave de COVID‑19. En analysant la façon dont ces cellules vivent, meurent et utilisent leurs « centrales » internes (les mitochondries), les chercheurs mettent en évidence un profil de neutrophiles persistants et hyperactifs qui pourrait contribuer à l’inflammation chronique, aux lésions vasculaires et aux atteintes d’organes observées dans les formes sévères.
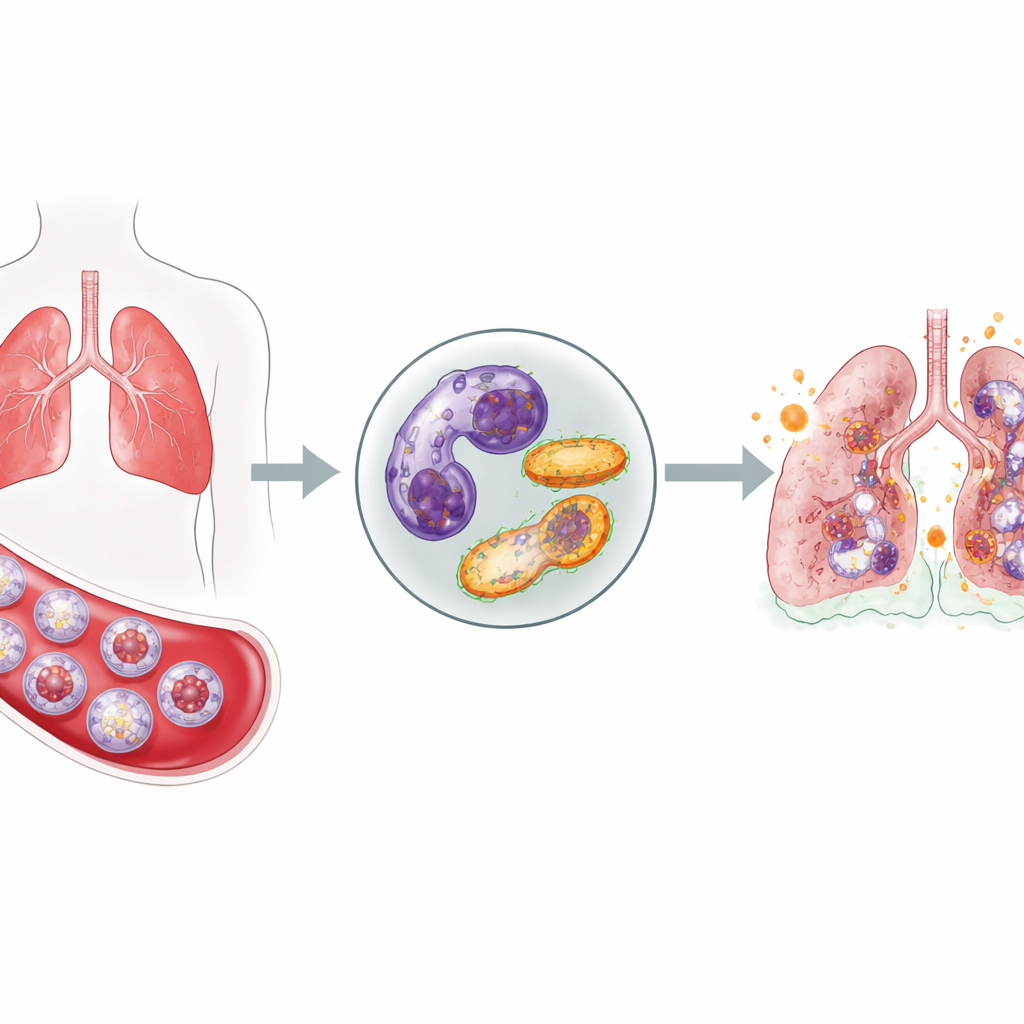
Des cellules de première ligne qui ne se calment pas
Les neutrophiles sont parmi les premiers intervenants de l’organisme lors d’une infection : ils affluent dans le sang, migrent dans les tissus et libèrent des molécules toxiques pour tuer les microbes. Normalement, après leur action, ils s’autodétruisent discrètement et sont éliminés, ce qui évite qu’ils n’endommagent les tissus sains. Chez les patients COVID‑19 en état critique, l’équipe a observé un tableau très différent. Par rapport à des volontaires sains, ces patients présentaient une poussée de neutrophiles dans le sang et, surtout, une proportion importante d’entre eux étaient des cellules immatures expulsées prématurément de la moelle osseuse. Parallèlement, plusieurs tests ont montré qu’un plus faible nombre de neutrophiles déclenchait leur mort programmée, ce qui suggère que ces cellules agressives persistent plus longtemps qu’à l’accoutumée.
Signaux génétiques subtils mais schéma clair de survie
Les chercheurs ont également examiné de petites molécules régulatrices appelées microARN dans les neutrophiles de survivants et de non‑survivants des soins intensifs. Certaines de ces molécules étaient altérées d’une manière qui, sur le papier, pointe vers des voies perturbées contrôlant la mort cellulaire et l’équilibre calcique. Cependant, lorsqu’ils ont mesuré des marqueurs directs de la mort cellulaire, ils n’ont pas observé de différences majeures entre survivants et non‑survivants — les deux groupes présentaient une réduction similaire de l’autodestruction des neutrophiles par rapport aux témoins sains. Cela signifie que les profils de microARN constituent plutôt des pistes pour des travaux futurs que des indicateurs fermes du pronostic, et souligne que l’incapacité générale des neutrophiles à s’éteindre est une caractéristique commune des formes sévères de COVID‑19.
Variations du calcium et centrales surchargées
Pour comprendre pourquoi les neutrophiles ne mouraient pas à temps, l’équipe s’est concentrée sur deux systèmes étroitement liés à l’intérieur des cellules : les signaux calciques et les mitochondries. Les ions calcium agissent comme de petits interrupteurs pour de nombreuses décisions cellulaires, y compris la programmation de la mort. Les chercheurs ont constaté que les neutrophiles des patients en état critique présentaient moins de calcium libre intracellulaire, ainsi que des niveaux réduits de protéines clés qui aident normalement à transporter le calcium vers les mitochondries et à ouvrir une soupape de sécurité pouvant déclencher la mort cellulaire. Parallèlement, les mitochondries elles‑mêmes étaient anormalement « chargées », avec un gradient électrique membranaire plus élevé et une consommation d’oxygène accrue, en particulier via une voie respiratoire majeure. Plutôt que de s’éteindre, ces mitochondries hyperactives produisaient davantage de molécules réactives de l’oxygène, susceptibles d’endommager les tissus environnants et d’alimenter l’inflammation.
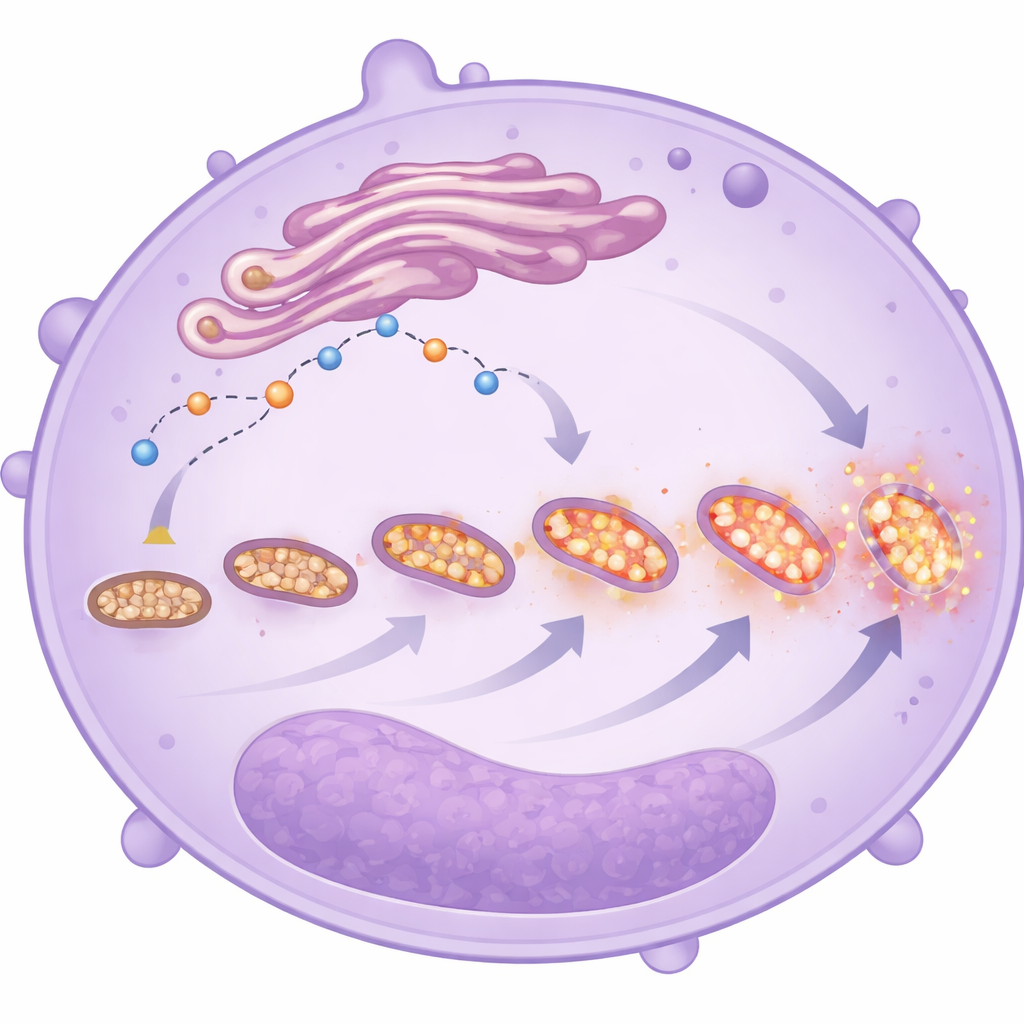
Mitochondries stressées et fragmentées
Les images au microscope électronique et les sondes fluorescentes ont permis d’examiner plus finement la forme et le comportement de ces mitochondries. Chez les neutrophiles des patients les plus gravement atteints, les mitochondries étaient plus nombreuses mais plus petites et plus fragmentées — des signes fréquents de stress. Ces cellules présentaient également des niveaux accrus d’espèces réactives de l’oxygène mitochondriales, indépendamment de l’issue clinique du patient. Avec l’altération de la gestion du calcium et le retard de la mort cellulaire, ces observations dessinent le portrait de neutrophiles ayant modifié leur stratégie énergétique : plutôt que de s’appuyer principalement sur la glycolyse, ils misent davantage sur le métabolisme mitochondrial, en particulier dans les cellules immatures. Ce basculement peut renforcer leur capacité à migrer, à persister et à libérer des molécules dommageables dans les poumons et d’autres organes, même si l’étude ne peut pas prouver qu’ils sont la cause directe d’un pronostic plus défavorable.
Ce que cela pourrait signifier pour les soins futurs
En termes simples, l’étude suggère que dans le COVID‑19 critique, les neutrophiles deviennent trop nombreux, trop immatures et trop difficiles à éteindre. Leurs signaux calciques internes et leurs mitochondries sont reprogrammés de façon à les maintenir en vie et très actifs, produisant des poussées de composés oxygénés nocifs. Bien que le travail soit observationnel et n’établisse pas de lien de cause à effet, il met en lumière plusieurs « boutons de contrôle » potentiels dans ces cellules — tels que les régulateurs du calcium et les points de contrôle mitochondriaux — qui pourraient un jour permettre de ramener en douceur les neutrophiles vers un comportement normal. Si des recherches ultérieures confirment ces idées, des traitements visant à restaurer l’arrêt approprié des neutrophiles ou à calmer leurs mitochondries surchargées pourraient aider à réduire les dommages collatéraux causés par ces cellules essentielles lors du COVID‑19 sévère et éventuellement dans d’autres pathologies critiques.
Citation: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Mots-clés: COVID-19, neutrophiles, mitochondries, inflammation, maladie critique