Clear Sky Science · fr
Synthèse et évaluation biologique de complexes de base de Schiff ibuprofène/o‑vanilline avec activités anti‑inflammatoires, antiprolifératives et anti‑SARS‑COV‑19
Pourquoi améliorer un antidouleur bien connu est important
L’ibuprofène est l’un des analgésiques et antipyrétiques les plus utilisés au monde, mais un usage prolongé peut irriter l’estomac et il n’a jamais été conçu pour combattre les infections, le cancer ou de nouveaux virus. Dans cette étude, des chimistes réingénientent l’ibuprofène en le fixant à une molécule naturelle au parfum vanillé puis en y attachant différents métaux. Le résultat est une famille de nouveaux composés qui agissent non seulement comme antalgiques, mais aussi comme antibiotiques potentiels, agents anticancéreux, anti‑inflammatoires et même inhibiteurs d’une enzyme clé du SARS‑CoV‑2, tout en fournissant des pistes sur la façon de concevoir des médicaments plus intelligents à partir de médicaments du quotidien.
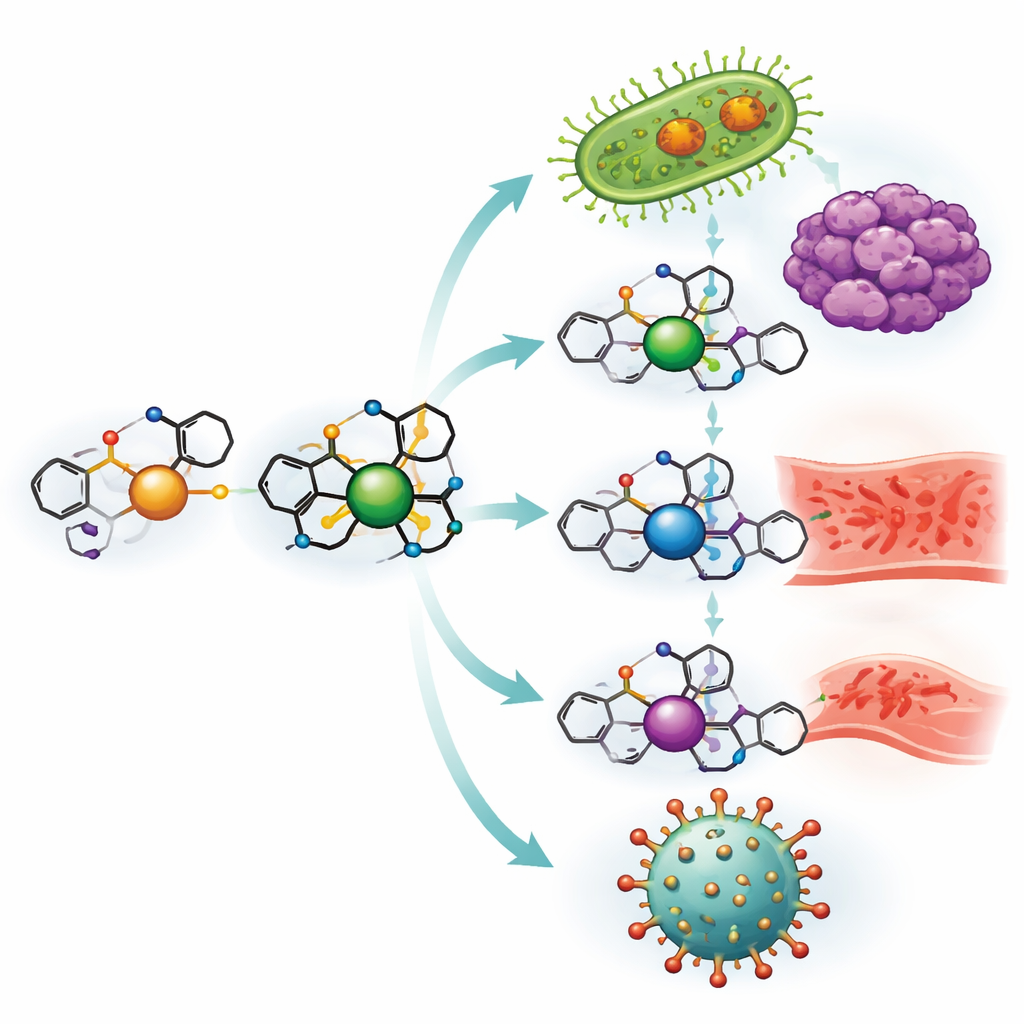
Construire de nouvelles molécules de type médicament à partir de l’ibuprofène
L’équipe a commencé par transformer l’ibuprofène en un bloc de construction plus polyvalent puis l’a lié à l’o‑vanilline, un proche cousin chimique du composé aromatique de la vanille. Ensemble, ils forment une ligand de type « base de Schiff » — essentiellement une pince sur mesure capable d’agripper des ions métalliques. Ce ligand a ensuite été combiné séparément avec des sels de cuivre, nickel, zinc et vanadium pour produire quatre complexes métalliques distincts. Des tests de laboratoire rigoureux, incluant des mesures du comportement à la fonte, de l’absorption de la lumière, des propriétés magnétiques et de la structure cristalline, ont confirmé comment le ligand enserre chaque métal et la stabilité des complexes obtenus, même à haute température et sur une large plage d’acidité.
Comment les complexes interagissent avec les cellules et l’ADN
Comme l’efficacité d’un médicament dépend souvent de sa rencontre avec des cibles biologiques, les chercheurs ont étudié la manière dont ces nouveaux complexes interagissent avec l’ADN et des cellules vivantes. Dans des expériences in vitro, le complexe de cuivre en particulier se liait fortement aux brins d’ADN et était capable de les endommager ou de les « cliver », un comportement souvent observé chez des agents anticancéreux et antibactériens puissants. Testés contre des lignées cellulaires cancéreuses humaines provenant de tumeurs du sein, du côlon et du foie, les quatre complexes se sont révélés plus toxiques pour les cellules cancéreuses que le ligand à base d’ibuprofène seul, le complexe de cuivre approchant la puissance du médicament chimiothérapeutique vinblastine à doses similaires.
Combattre germes, champignons et inflammation
Les mêmes composés ont été mis au défi contre des microbes pathogènes courants, y compris des bactéries Gram‑positives et Gram‑négatives et deux champignons problématiques. Là encore, les complexes métalliques ont surpassé le ligand libre, et le cuivre s’est distingué en inhibant fortement à la fois bactéries et champignons. Les auteurs interprètent ces résultats via la théorie de la chélation : une fois le métal retenu par le ligand, sa charge est en partie masquée et l’ensemble du complexe devient plus lipophile, lui permettant de pénétrer les membranes microbiennes et de perturber des enzymes vitales. Dans un test simple d’inflammation basé sur une protéine d’œuf endommagée par la chaleur, les nouveaux complexes ont également réduit la dénaturation protéique plus efficacement que l’ibuprofène lui‑même, suggérant qu’ils pourraient calmer les processus inflammatoires à des doses plus faibles.
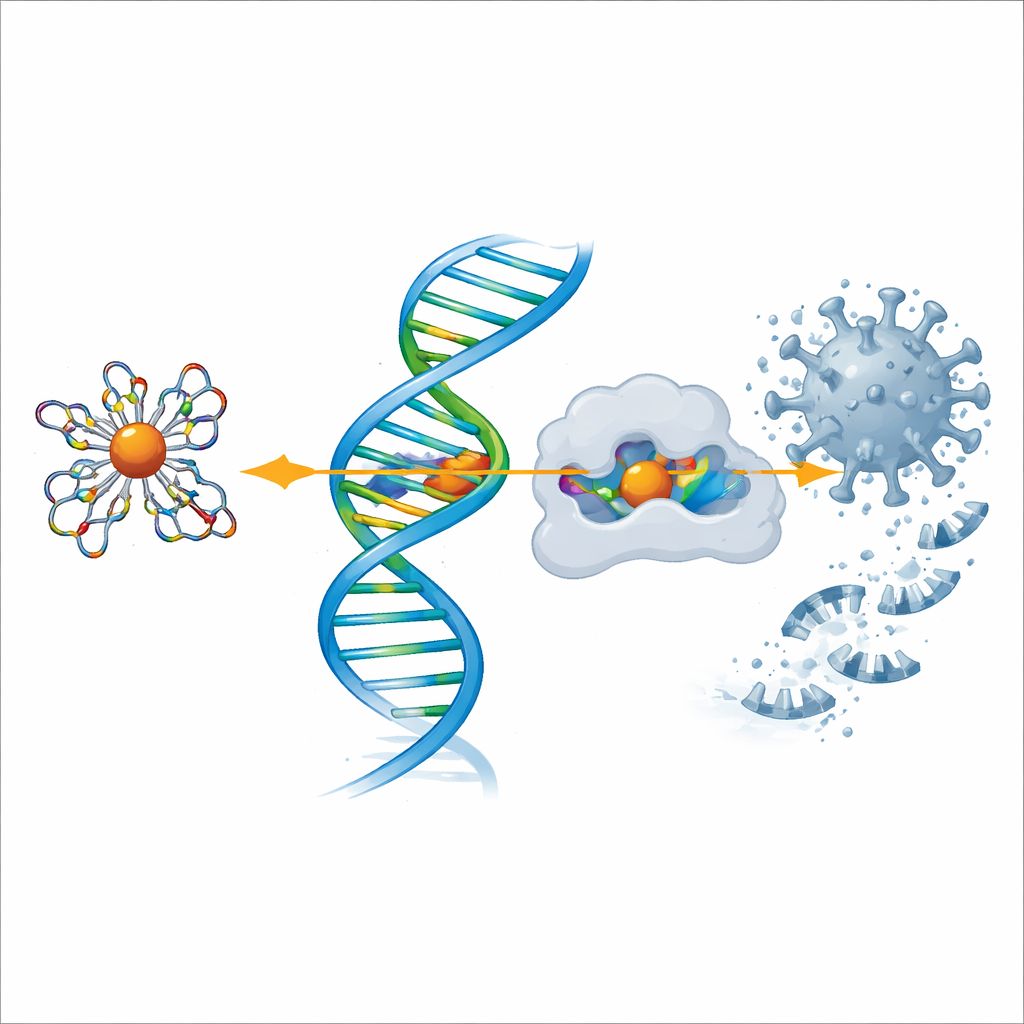
Examiner l’action contre le COVID‑19 et les enzymes de la douleur
Pour explorer un potentiel antiviral, l’équipe a utilisé la modélisation informatique pour effectuer un docking du ligand et de chaque complexe métallique dans les structures tridimensionnelles de deux protéines clés : la protéase principale du SARS‑CoV‑2, que le virus utilise pour cliver ses polyprotéines, et la cyclooxygénase‑2 (COX‑2), une enzyme impliquée dans la douleur et l’inflammation. Les simulations ont montré que les complexes, en particulier ceux du cuivre et du zinc, s’inséraient parfaitement dans les poches actives de ces protéines et formaient de multiples interactions stabilisantes. Plus l’énergie de liaison calculée était négative, plus la liaison prédite était forte, et une fois encore le complexe de cuivre s’est démarqué, suivi de près par le zinc et le nickel, ce qui corrobore les résultats expérimentaux sur les activités anti‑inflammatoires et antimicrobiennes.
Ce que cela pourrait signifier pour les médicaments de demain
Dans l’ensemble, ce travail montre qu’un médicament en vente libre familier peut être transformé en un outil chimique polyvalent en le fusionnant avec un partenaire organique soigneusement choisi et l’ion métallique approprié. Parmi les quatre métaux testés, le cuivre a produit le candidat le plus prometteur, avec des activités antibactériennes, antifongiques, anticancéreuses, anti‑inflammatoires et des effets anti‑SARS‑CoV‑2 prédits par modélisation, tandis que le nickel et le zinc offraient des effets un peu plus modérés mais néanmoins notables. Bien que ces résultats en soient encore au stade des études de laboratoire et de la modélisation informatique, ils indiquent une stratégie selon laquelle des médicaments du quotidien peuvent être « améliorés » en complexes métalliques ciblés susceptibles d’agir à des doses plus faibles et sur un spectre de maladies plus large que les médicaments originaux.
Citation: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Mots-clés: Dérivés de l’ibuprofène, Complexes médicamenteux métalliques, Agents anticancéreux, Thérapie antimicrobienne, Protéase du COVID‑19