Clear Sky Science · fr
Functionalisation asymétrique catalytique des esters boroniques de bicyclo[1.1.0]butane rendue possible par une migration 1,2 de l’oxygène
Pourquoi les petits cycles carrés comptent
Les chimistes aiment assembler de nouveaux médicaments et matériaux en emboîtant de petites pièces moléculaires, un peu comme des briques Lego. Les cycles à quatre atomes de carbone appelés cyclobutanes sont particulièrement prisés parce qu’ils concentrent beaucoup d’énergie et de géométrie dans un espace réduit, ce qui peut modifier le comportement d’un médicament dans l’organisme. Cet article décrit une nouvelle façon de fabriquer ces anneaux dans une forme très contrôlée et « unilatérale » (chirale), en utilisant une réaction astucieuse qui oblige un groupe porteur d’oxygène à sauter d’un atome à l’autre. Ce travail ouvre la voie à la conception de molécules plus complexes et plus précises pour la pharmaceutique et les matériaux avancés.
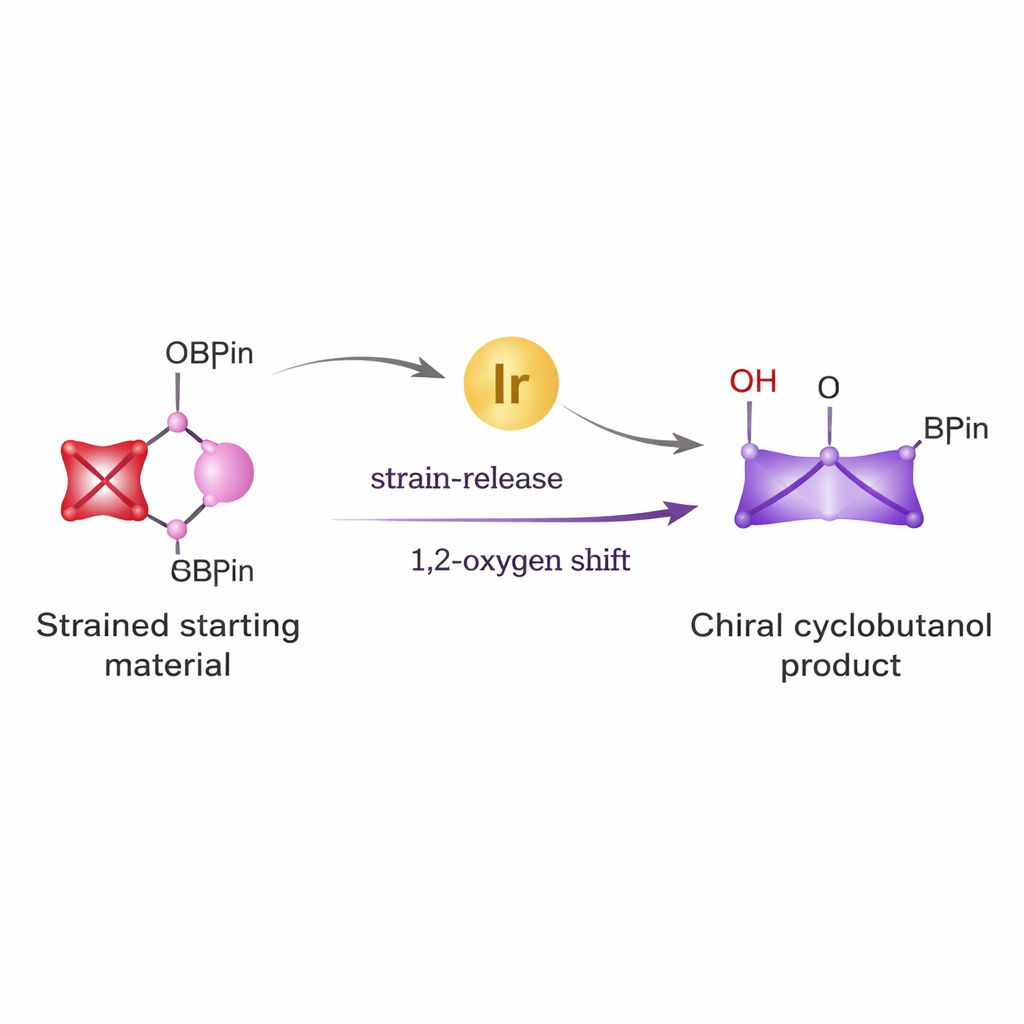
Des blocs de construction simples vers des anneaux puissants
Les cyclobutanes apparaissent dans divers agents antiviraux, candidats anticancéreux et autres molécules bioactives. Pourtant, les construire avec l’arrangement tridimensionnel exact requis en médecine a été difficile. Les méthodes traditionnelles exigent souvent des réactifs agressifs et donnent des mélanges de produits images miroir difficiles à séparer. Les auteurs ont cherché à résoudre ce problème en combinant deux idées puissantes : la réactivité inhabituelle d’un petit cycle très contraint, le bicyclo[1.1.0]butane, et la polyvalence des esters boroniques, une famille de réactifs bien connue et largement utilisée en chimie de couplage pour former des liaisons carbone–carbone.
Transformer un inconvénient en nouvelle voie réactionnelle
Dans les réactions de couplage catalysées par un métal classiques, les esters boroniques forment un complexe intermédiaire avec un alkoxyde (une base à base d’oxygène). Ce complexe suit presque toujours une voie bien établie appelée transmetallation, qui conduit directement à de nouvelles liaisons carbone–carbone ou carbone–halogène. Cette voie « par défaut » a limité l’exploration d’autres possibilités, comme le déplacement du groupe oxygéné lui‑même. L’équipe a réalisé que si elle partait d’un ester boronique de bicyclo[1.1.0]butane soumis à la contrainte du cycle, cette tension intrinsèque pourrait surpasser la voie habituelle. En associant ce système contraint à un catalyseur à l’iridium et à un ligand chiral soigneusement choisi, ils ont cherché à inciter la migration de l’oxygène de manière contrôlée, pendant que le cycle s’ouvrait puis se refermait en cyclobutane.
Une danse en étapes guidée par la contrainte
Les expérimentations ont confirmé que cette stratégie fonctionne. En utilisant des alkoxydes de lithium issus d’une grande variété d’alcools — y compris des sucres, des terpènes, des stéroïdes et de simples alcools aliphatiques — les auteurs ont converti des esters boroniques de bicyclo[1.1.0]butane en cyclobutanols cis avec des rendements élevés et un excellent contrôle de la chiralité. Le catalyseur à l’iridium forme d’abord un complexe allyl réactif à partir d’un carbonate allylique partenaire. Ce complexe attaque ensuite le système contraint du bicyclo[1.1.0]butane, formant une nouvelle liaison carbone–carbone au fur et à mesure que le petit cycle s’ouvre. Crucialement, au lieu de suivre immédiatement la transmetallation habituelle, l’intermédiaire contenant du bore subit une rotation subtile de la liaison carbone–bore, positionnant le groupe oxygéné attaché de sorte qu’il puisse se transférer proprement vers l’atome de carbone voisin. Cette migration 1,2 de l’oxygène verrouille l’arrangement cis souhaité sur le nouveau cycle cyclobutane.
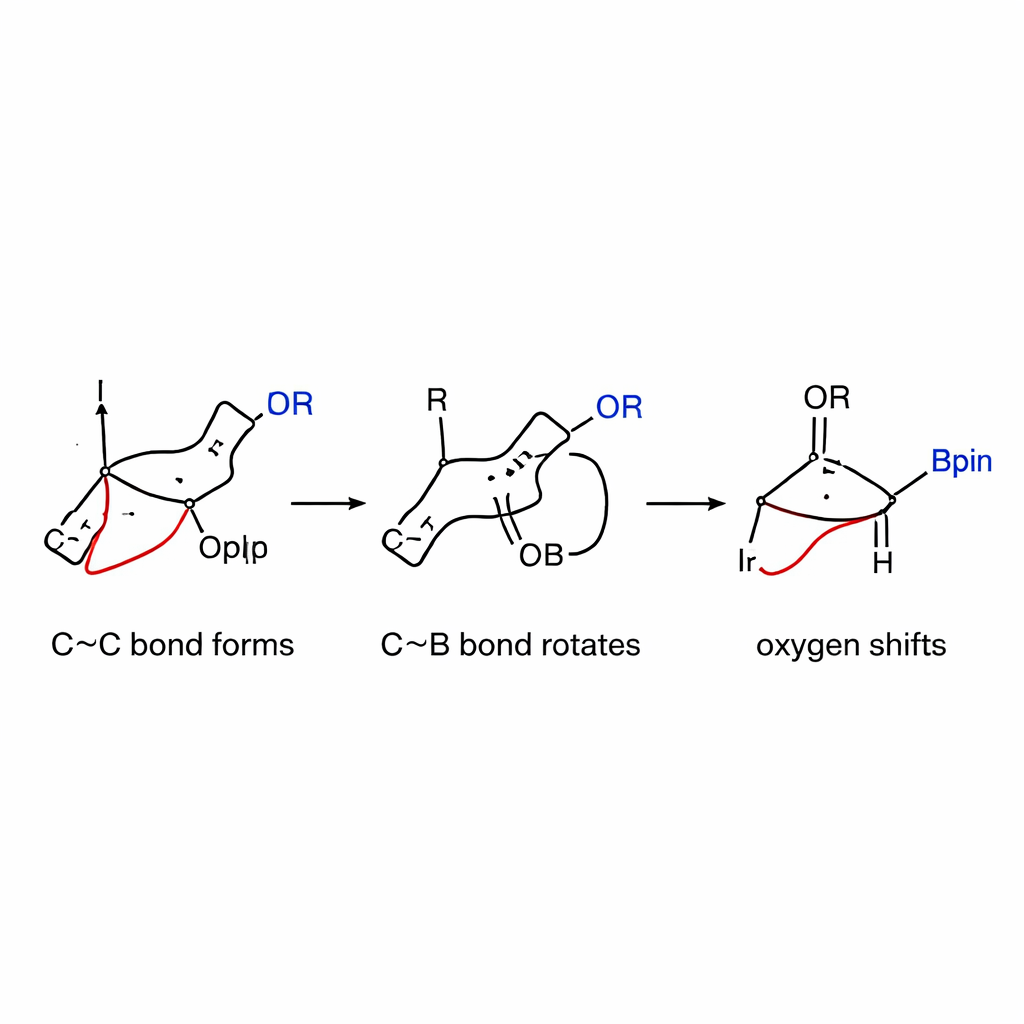
Explorer le mécanisme en détail
Pour comprendre pourquoi la réaction est si sélective, les auteurs ont combiné des mesures cinétiques avec des simulations informatiques détaillées. Ils ont constaté que l’étape lente et limitante est la formation initiale de la liaison carbone–carbone entre l’espèce iridium–allyl et le complexe boronaté contraint, et non l’activation préalable du carbonate allylique. Des tests électroniques ont montré que les partenaires allyliques qui stabilisent la charge positive réagissent plus vite, ce qui corrobore un mécanisme impliquant un intermédiaire partiellement chargé. Les calculs ont en outre révélé que la rotation autour de la liaison carbone–bore — auparavant considérée comme difficile — présente une barrière énergétique étonnamment basse dans ce système, grâce à la contrainte emmagasinée du cycle. Une fois la rotation alignant le groupe oxygéné, la migration 1,2 se déroule en douceur et favorise la formation du produit cis plutôt que de la forme trans plus courante.
De nouveaux outils pour façonner les médicaments de demain
Au‑delà de la confirmation d’un point mécanistique, la réaction fournit des produits polyvalents. Les cyclobutanols conservent une unité ester boronique, qui peut être transformée en de nombreux autres groupes fonctionnels grâce à la chimie établie. Les auteurs ont illustré de nombreuses modifications « de fin de séquence », telles que l’hydrogénation, l’oxydation, la métathèse d’oléfines et d’autres couplages, tout en préservant la forme tridimensionnelle précise de l’anneau. En termes simples, ce travail transforme une voie secondaire autrefois problématique — la migration d’oxygène dans les complexes boronates — en un puissant outil synthétique. En exploitant la contrainte des cycles et un catalyseur à l’iridium finement ajusté, les chercheurs offrent aux chimistes une méthode fiable pour construire des cyclobutanes chiraux complexes qui pourraient jouer un rôle clé dans les médicaments de nouvelle génération et les matériaux moléculaires avancés.
Citation: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Mots-clés: cyclobutane, chimie des organoboranes, catalyse asymétrique, bicyclobutane, migration d’oxygène