Clear Sky Science · fr
La régulation transcriptionnelle de la capsule pneumococcique peut dicter des infections spécifiques à un sérotype
Pourquoi de petites modifications chez un germe peuvent vous concerner
Streptococcus pneumoniae est une bactérie courante qui colonise discrètement les fosses nasales de nombreuses personnes mais peut aussi provoquer des pneumonies mortelles, des septicémies et des méningites. Les vaccins ciblent son enveloppe sucrée externe, appelée capsule, et ont sauvé d’innombrables vies. Cette étude pose une nouvelle question : au-delà de modifier la composition de cette capsule, le microbe peut-il changer la quantité de capsule qu’il produit — en n’utilisant que quelques ajustements d’ADN — pour échapper à nos défenses immunitaires et aux vaccins ? Les auteurs montrent que la réponse est oui.
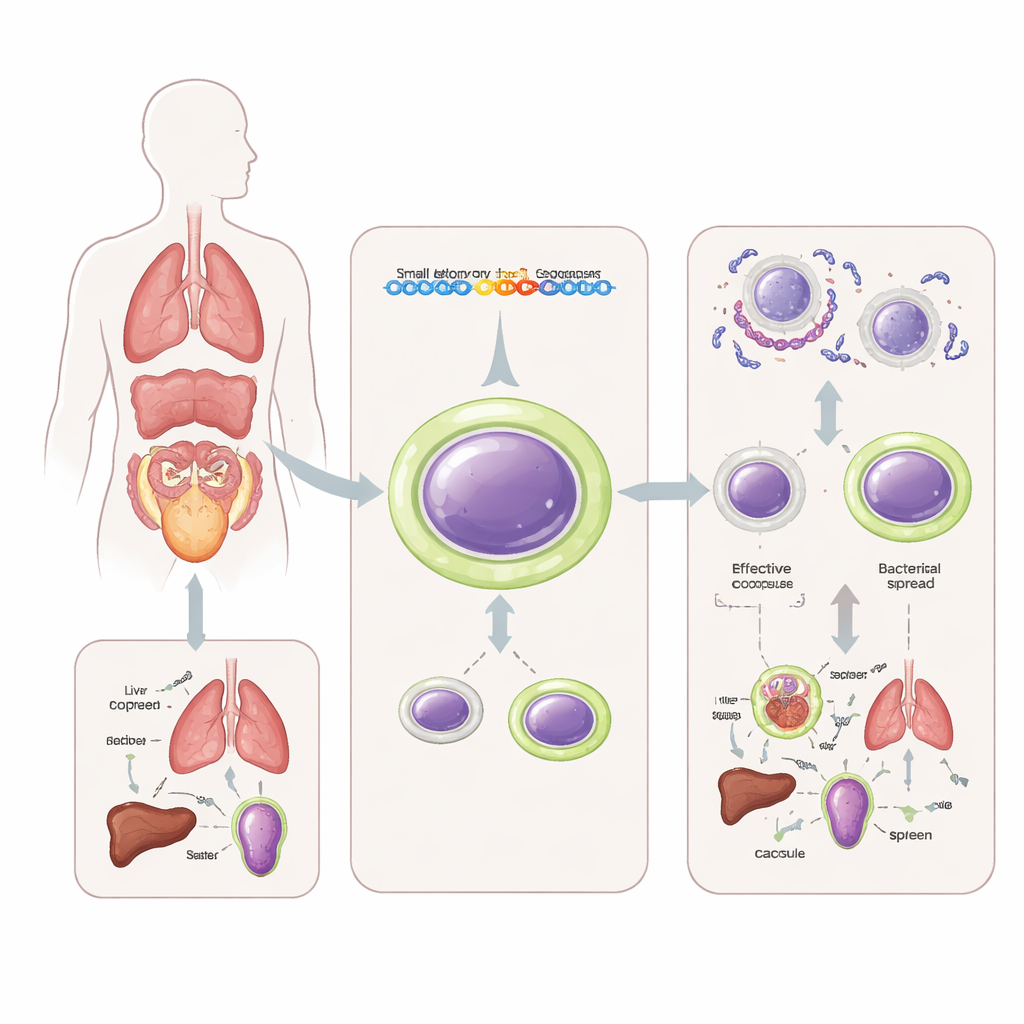
Un manteau sucré qui façonne la maladie
Les pneumocoques existent en plus d’une centaine de « sérotypes », chacun caractérisé par une chimie de capsule légèrement différente. Certains ont tendance à rester dans le nez, tandis que d’autres envahissent plus souvent le sang et les organes. Traditionnellement, les scientifiques ont attribué ces différences principalement à la composition chimique de la capsule. La capsule aide la bactérie à se cacher des cellules immunitaires qui l’auraient autrement ingérée et détruite. Les vaccins fonctionnent en entraînant le système immunitaire à reconnaître des types de capsule spécifiques, mais cela pousse aussi les bactéries à évoluer pour éviter cette reconnaissance.
L’interrupteur de contrôle caché dans l’ADN bactérien
Plutôt que de se concentrer sur la chimie de la capsule, ce travail met au point de mire un petit segment d’ADN régulateur situé juste en amont des gènes de la capsule, appelé 37-CE. Ce court tronçon fonctionne comme un variateur pour la production de capsule. Deux protéines de régulation bactériennes, SpxR et CpsR, se lient à cet ADN et règlent la quantité de capsule produite. Les chercheurs ont examiné des versions naturelles de cet élément d’ADN présentes chez différents sérotypes. Dans des expériences in vitro, ils ont montré que SpxR et CpsR se lient à ces variantes avec des affinités très différentes, ce qui suggère que même de faibles changements de séquence peuvent réorienter le contrôle de la capsule.
Échanger l’interrupteur modifie l’épaisseur et l’évasion immunitaire
Pour comprendre les conséquences in vivo, l’équipe a conçu des souches dans lesquelles les gènes principaux de la capsule restaient inchangés, mais le segment régulateur 37-CE était remplacé par des versions provenant d’autres sérotypes. En culture, ces échanges modifiaient l’épaisseur de la capsule, et les effets dépendaient des conditions de croissance mimant les voies respiratoires ou le sang. Les capsules plus fines étaient plus facilement englouties par les cellules immunitaires de souris, confirmant que cet élément d’ADN influe directement sur la résistance à la phagocytose. Chez la souris, des souches portant différentes versions de 37-CE montraient des différences marquées dans leur persistance au niveau du foie et de la rate lors d’une infection sanguine, même lorsque leur composition chimique de capsule était identique.
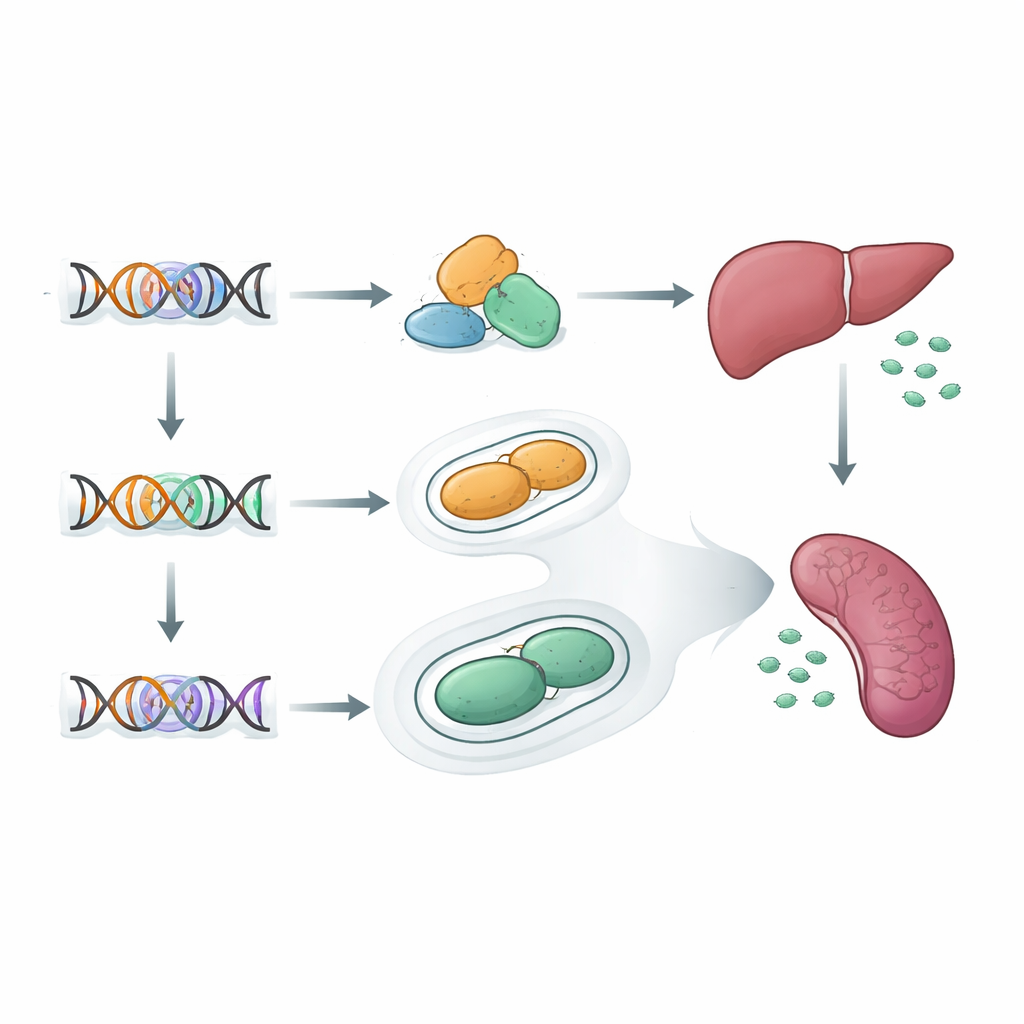
Affiner l’infection selon les organes
Les auteurs sont allés plus loin en suivant l’activité des gènes de la capsule pendant l’infection grâce à un marqueur bioluminescent intégré. Ils ont constaté que certaines variantes de 37-CE coupaient spécifiquement la production de capsule dans le foie, où un élimination précoce est cruciale, mais permettaient une expression robuste de la capsule dans la rate et les poumons. Cet ajustement organe par organe signifie qu’une variante peut rendre les bactéries plus faciles à éliminer dans le foie tout en leur permettant de survivre et de se multiplier dans la rate, qui peut ensuite réensemencer la circulation sanguine. L’équipe a aussi construit des souches portant un type de capsule peu virulent mais combinant différents segments régulateurs. Ils ont montré que la structure chimique de la capsule et son « câblage » régulateur déterminent ensemble si une souche se comporte de manière bénigne ou sévère lors d’une septicémie.
Conséquences pour l’évasion vaccinale et les menaces futures
Les vaccins actuels poussent principalement les pneumocoques à changer le type de capsule qu’ils affichent — un saut génétique plus important qui peut être coûteux sur le plan métabolique et n’est pas toujours possible selon le fond génétique. Cette étude révèle un raccourci évolutif plus simple : de petites mutations dans un court élément d’ADN régulateur peuvent augmenter ou diminuer l’épaisseur de la capsule dans des tissus spécifiques sans modifier le type de capsule. Cela signifie qu’une souche déjà couverte par les vaccins pourrait, en théorie, devenir plus difficile à éliminer simplement en ajustant cet interrupteur de contrôle, lui permettant d’échapper aux défenses immunitaires tout en conservant sa capsule d’origine. Ces travaux suggèrent que, pour garder une longueur d’avance sur ce pathogène adaptable, les stratégies futures devront prendre en compte non seulement la composition de la capsule, mais aussi la façon dont sa production est contrôlée au niveau de l’ADN.
Citation: Marra, M., Gazioglu, O., Glanville, D.G. et al. Transcriptional regulation of the pneumococcal capsule can dictate serotype-specific infection. Nat Commun 17, 3671 (2026). https://doi.org/10.1038/s41467-026-69722-4
Mots-clés: Streptococcus pneumoniae, capsule bactérienne, évasion vaccinale, régulation génétique, septicémie