Clear Sky Science · fr
Les macrophages CD19+ associés aux tumeurs induisent un microenvironnement immunosuppresseur dans le carcinome hépatocellulaire
Pourquoi les défenseurs de l’organisme aident parfois le cancer du foie
Le cancer du foie est l’un des cancers les plus mortels au monde, en partie parce que les tumeurs peuvent détourner le propre système immunitaire de l’organisme contre lui-même. Cette étude met au jour une sous-population surprenante de cellules immunitaires à l’intérieur des tumeurs hépatiques qui, au lieu de combattre le cancer, l’aident activement à se cacher et à se développer. Comprendre qui sont ces cellules « traîtresses » et comment elles fonctionnent ouvre de nouvelles pistes pour rendre l’immunothérapie plus efficace chez les patients atteints de carcinome hépatocellulaire, la forme la plus courante de cancer du foie.
Un groupe particulier de cellules immunitaires au sein des tumeurs
Les auteurs se sont concentrés sur les macrophages associés aux tumeurs, des cellules immunitaires qui engloutissent normalement microbes et débris mais se trouvent souvent corrompues dans les cancers. En analysant des échantillons de tumeurs hépatiques provenant de nombreux patients, ils ont découvert un sous-groupe distinct de macrophages portant une molécule de surface appelée CD19, habituellement présente sur les cellules B plutôt que sur les macrophages. Ces macrophages CD19-positifs étaient beaucoup plus abondants dans les tumeurs hépatiques que dans le foie sain voisin ou le sang, et étaient également enrichis dans plusieurs autres cancers solides. Des analyses en cellules uniques ont confirmé que ces cellules sont de véritables macrophages avec un profil génique et protéique unique, et non des cellules B mal identifiées.
Comment ces cellules façonnent un voisinage favorable à la tumeur
Les patients dont les tumeurs contenaient de nombreux macrophages CD19-positifs avaient tendance à présenter des cancers plus volumineux, plus agressifs et des survies plus courtes. Les échantillons tumoraux riches en ces cellules présentaient moins de cellules CD8 tueuses de cancer et davantage de cellules T régulatrices, un schéma typique d’un environnement fortement immunosuppresseur. Chez la souris, l’ajout de macrophages CD19-positifs à des cellules de cancer du foie accélérait la croissance tumorale et réduisait la présence de cellules T utiles, tout en augmentant d’autres cellules myéloïdes suppressives. Fait important, lorsque les chercheurs ont utilisé des lymphocytes T génétiquement modifiés reconnaissant CD19 pour éliminer sélectivement ces macrophages, les tumeurs hépatiques ont régressé même chez des souris dépourvues de cellules B normales, identifiant ainsi les macrophages eux-mêmes comme cibles thérapeutiques.
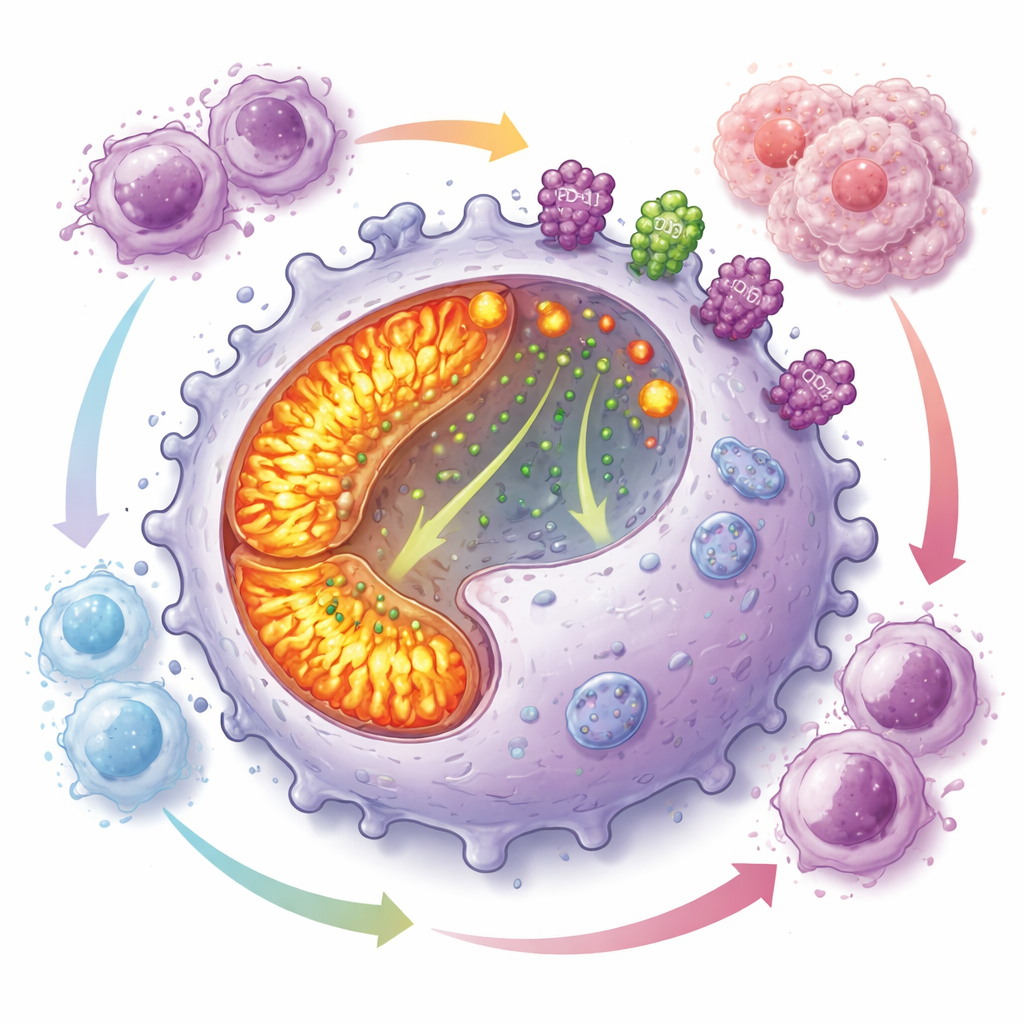
Un programme énergivore qui atténue l’attaque immunitaire
En creusant plus loin, l’équipe a observé que les macrophages CD19-positifs activent fortement leurs « centrales » internes. Leurs mitochondries, les organites produisant de l’énergie, étaient plus nombreuses et plus actives que chez les autres macrophages, avec une phosphorylation oxydative accrue et davantage d’espèces réactives de l’oxygène. Malgré cet état énergétique, ces cellules présentaient une capacité d’engloutissement réduite mais se divisaient rapidement, ce qui favorise leur accumulation dans les tumeurs. Parallèlement, elles exprimaient à haute dose PD-L1 et CD73 à leur surface — deux molécules connues pour éteindre les réponses des lymphocytes T et pour générer de l’adénosine, un petit métabolite qui supprime puissamment l’immunité. Des expériences en co-culture ont montré que ces macrophages inhibaient fortement la prolifération de plusieurs types de lymphocytes T.
L’interrupteur maître derrière les macrophages traîtres
Les chercheurs ont identifié un facteur de transcription appelé PAX5 comme le moteur central de ce programme macrophagique délétère. PAX5 est surtout connu pour guider le développement des cellules B, et pourtant ici il est fortement actif dans les macrophages CD19-positifs. Contraindre des cellules de type macrophage à exprimer PAX5 a stimulé la biogenèse mitochondriale, augmenté la production d’énergie et élevé les niveaux protéiques — mais pas les niveaux d’ARNm — de PD-L1, CD73 et CD19. Des expériences mécanistiques ont montré que PAX5 favorise l’entrée du calcium dans les mitochondries, abaissant le calcium dans le cytosol et empêchant un régulateur clé, TFEB, d’entrer dans le noyau. Avec TFEB retenu, la production et la fonction des lysosomes diminuent, de sorte que des protéines comme PD-L1 et CD73 ne sont plus efficacement dégradées et s’accumulent à la surface cellulaire, intensifiant ainsi l’immunosuppression.
Transformer la découverte en meilleures options thérapeutiques
Parce que ces macrophages dépendent fortement de l’activité de CD73 et du métabolisme mitochondrial, les auteurs ont testé si bloquer ces voies pouvait améliorer l’efficacité de l’immunothérapie. Dans le cancer hépatique murin, combiner un blocage de PD-L1 avec des anticorps contre CD73 ou un inhibiteur de CD73 a réduit la taille des tumeurs, augmenté l’infiltration de lymphocytes T et diminué la prolifération des cellules cancéreuses. De même, associer des anticorps anti–PD-L1 à un inhibiteur de la phosphorylation oxydative mitochondriale a amélioré le contrôle tumoral et favorisé l’entrée de cellules immunitaires dans les tumeurs. Fait marquant, ces bénéfices ont disparu chez des souris dont les macrophages étaient dépourvus de PAX5, confirmant que les effets des traitements étaient liés à l’inactivation du programme macrophagique CD19-positif piloté par PAX5. Globalement, le travail suggère que cibler sélectivement ce sous-ensemble de macrophages — par des thérapies cellulaires dirigées contre CD19, l’inhibition de CD73 ou des médicaments métaboliques — pourrait aider à convertir une tumeur hépatique immunologiquement « froide » en une tumeur beaucoup plus réceptive aux inhibiteurs de points de contrôle existants.
Citation: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Mots-clés: carcinome hépatocellulaire, macrophages associés aux tumeurs, immunothérapie, PD-L1 et CD73, métabolisme mitochondrial