Clear Sky Science · fr
L’expression tumorale spécifique de HORMAD1 perturbe l’arrêt mitotique et accroît la sensibilité aux inhibiteurs des kinases mitotiques
Pourquoi c’est important pour le traitement du cancer
Lorsque nos cellules se divisent, elles s’appuient sur des contrôles de sécurité complexes pour transmettre le bon jeu de chromosomes. Le cancer détourne ou affaiblit souvent ces garde-fous, entraînant des génomes chaotiques qui favorisent la maladie et conditionnent la réponse des tumeurs aux médicaments. Cette étude révèle comment une protéine inhabituelle nommée HORMAD1, normalement active uniquement dans les cellules reproductrices, est réactivée dans de nombreux cancers du sein agressifs et dans d’autres tumeurs. En sabotant subtilement un point de contrôle clé de la division cellulaire, HORMAD1 rend les cellules cancéreuses plus instables — mais aussi particulièrement vulnérables à une nouvelle classe de médicaments expérimentaux.
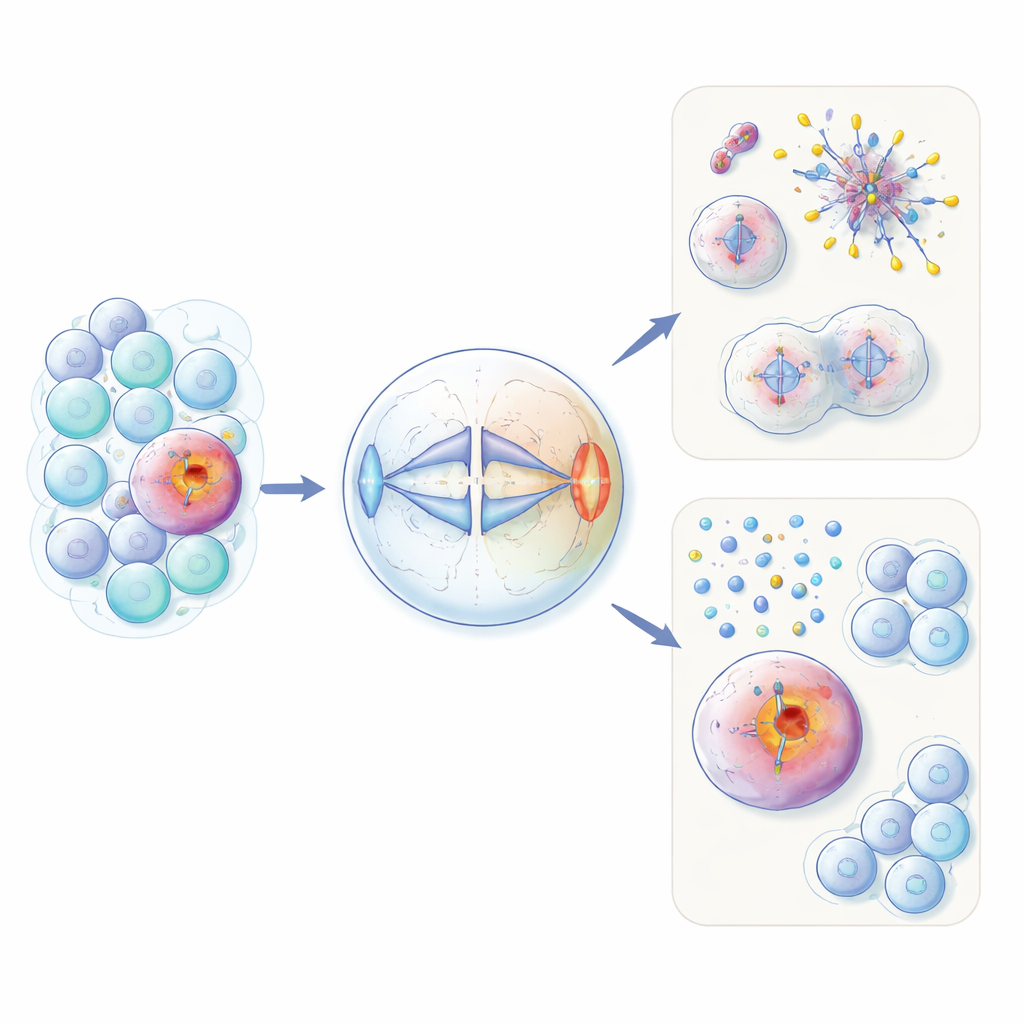
Une protéine de la fertilité mal placée dans les cellules cancéreuses
HORMAD1 apparaît normalement uniquement dans les cellules germinales, où se forment les ovules et les spermatozoïdes. Là, elle participe à la restructuration de l’ADN et au contrôle de qualité pendant la méiose, ce type spécial de division cellulaire. Les auteurs montrent que dans environ 60 % des cancers du sein triple négatif — et dans des sous-ensembles de plusieurs autres types de tumeurs — cette protéine est inappropriément réactivée. En utilisant à la fois des cellules non cancéreuses modifiées et des lignées cellulaires cancéreuses, ils ont constaté qu’un excès de HORMAD1 perturbe la séparation équitable des chromosomes lors de la division cellulaire ordinaire. Les cellules exprimant HORMAD1 présentaient davantage de chromosomes traînards, des chromosomes en trop ou en moins (aneuploïdie) et de petites « micronoyaux » contenant de l’ADN, autant de signes d’un chaos génomique observé dans les cancers agressifs.
Comment fonctionnent normalement les contrôles de la division cellulaire
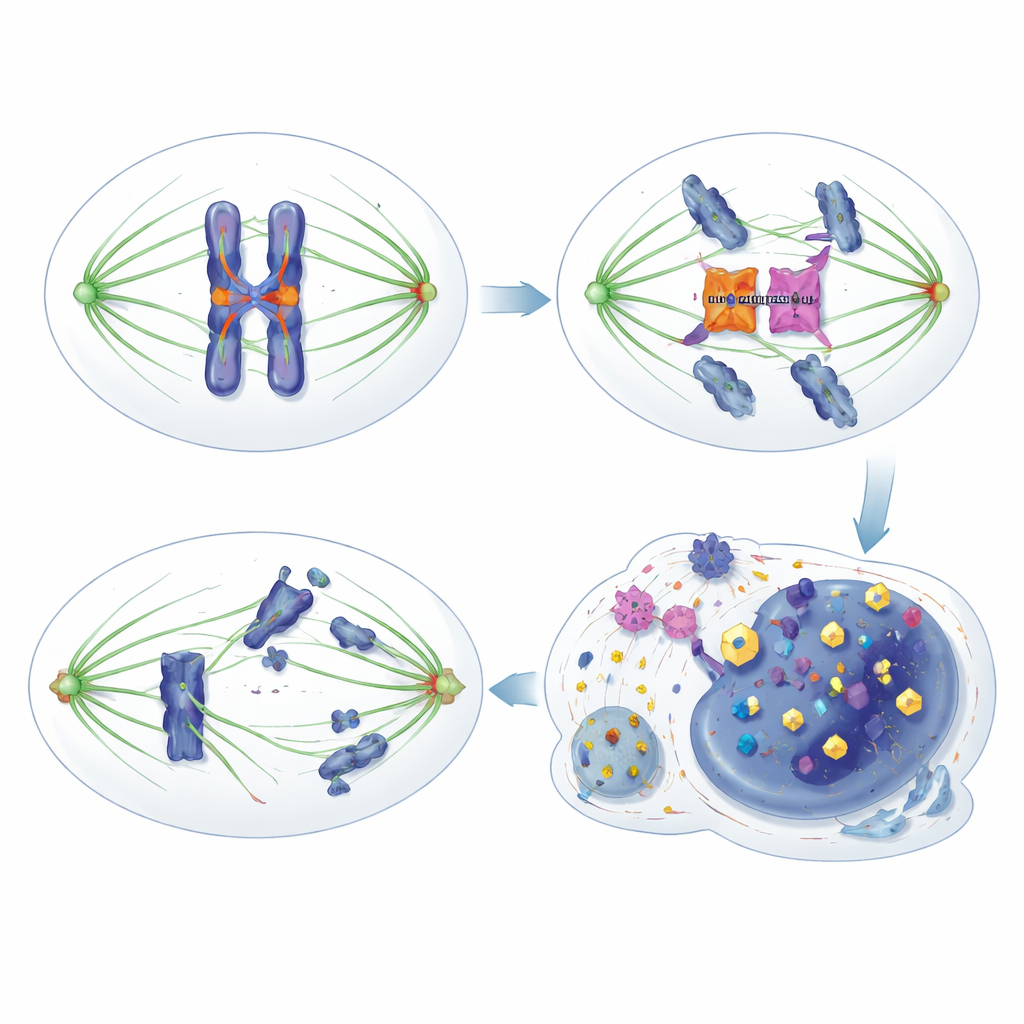
Pour se diviser correctement, une cellule assemble un fuseau de fibres de microtubules qui s’attachent à chaque chromosome. Un système de surveillance connu sous le nom de point de contrôle de l’assemblage du fuseau agit comme un frein sensible à la tension : si un chromosome n’est pas correctement attaché, le frein bloque la progression, empêchant la séparation tant que les erreurs ne sont pas corrigées. Plusieurs enzymes appelées kinases mitotiques, notamment MPS1, Aurora B et BUB1, aident à détecter les mauvaises attaches et favorisent la « correction des erreurs » afin que chaque cellule fille reçoive le bon jeu de chromosomes. La perturbation de ce système peut à la fois alimenter le développement du cancer et créer des faiblesses spécifiques que certains médicaments peuvent exploiter.
HORMAD1 affaiblit discrètement le frein
Les chercheurs ont découvert que HORMAD1 sape ce frein de sécurité d’une manière subtile mais importante. Plutôt que d’interférer avec des composants classiques du point de contrôle comme la protéine HORMA MAD2L1, HORMAD1 se lie directement à la kinase Aurora B. Aurora B s’associe normalement à une autre protéine, INCENP, pour être pleinement active et modifier des protéines aux centromères et aux kinétochores — des sites critiques sur les chromosomes où s’attachent les fibres du fuseau. Lorsque HORMAD1 est présent dans des cellules tumorales en division, il entre en compétition avec INCENP pour l’accès à Aurora B, réduisant leur association et atténuant l’activité d’Aurora B. En conséquence, les signaux habituels de phosphorylation par Aurora B sur plusieurs cibles sont affaiblis, la correction des erreurs est moins efficace et le point de contrôle devient « poreux » : les cellules sortent de la mitose trop tôt, même lorsque les attaches sont défectueuses, ce qui conduit à des méségrégations chromosomiques et à l’instabilité génomique.
De la faiblesse à une opportunité thérapeutique
Parce que HORMAD1 n’inactive qu’en partie Aurora B et les garde-fous associés, les cellules cancéreuses restent juste assez viables pour croître, mais dépendent fortement de la fonction résiduelle des kinases mitotiques pour survivre à des divisions défectueuses répétées. L’équipe a testé cela en exposant des cellules positives et négatives pour HORMAD1 à des inhibiteurs expérimentaux de MPS1, Aurora B et BUB1. Dans plusieurs modèles, l’expression de HORMAD1 rendait les cellules beaucoup plus sensibles à ces médicaments, réduisant drastiquement leur capacité à proliférer ou à former des colonies. L’épuisement génétique de BUB1 était particulièrement létal uniquement en présence de HORMAD1, révélant une dépendance forte et sélective. Dans des modèles murins utilisant des tumeurs triples négatives dérivées de patients, celles présentant des niveaux élevés de HORMAD1 ont régressé ou grossi plus lentement lorsqu’on les traitait avec une formulation nanoparticulaire d’un inhibiteur d’Aurora B, tandis que les tumeurs négatives pour HORMAD1 résistaient en grande partie au même traitement.
Ce que cela signifie pour les patients
Pour un observateur non spécialiste, HORMAD1 agit comme une épée à double tranchant dans le cancer : elle pousse les cellules tumorales vers un désordre chromosomique accru, ce qui peut favoriser la maladie, mais ce faisant elle les rend aussi dangereusement dépendantes de quelques garde-fous restants de la division cellulaire. L’étude montre que cette protéine de la fertilité mal placée affaiblit un point de contrôle clé en détournant Aurora B, rendant les tumeurs positives pour HORMAD1 particulièrement vulnérables aux médicaments ciblant Aurora B, MPS1 ou BUB1. Étant donné que HORMAD1 est largement absente des tissus normaux tout en étant présente dans un sous-ensemble clair de cancers, elle pourrait servir de biomarqueur pour identifier les patients les plus susceptibles de bénéficier de ces inhibiteurs de kinases mitotiques émergents, ouvrant potentiellement de nouvelles voies de traitement ciblé pour des cancers difficiles à traiter comme le cancer du sein triple négatif.
Citation: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Mots-clés: HORMAD1, cancer du sein triple négatif, instabilité chromosomique, kinase Aurora B, inhibiteurs du point de contrôle mitotique