Clear Sky Science · fr
Bifidobacterium longum et interventions prébiotiques restaurent les altérations du comportement alimentaire induites par un régime riche en graisses et sucres en début de vie chez la souris adulte
Pourquoi les premières habitudes de grignotage peuvent résonner à l’âge adulte
Ce que nous mangeons dès nos premiers jours peut discrètement configurer notre cerveau et notre intestin pour les années à venir. Cette étude chez la souris pose une question aux évidentes résonances humaines : si les nouveau‑nés sont exposés à des aliments riches en graisses et en sucres, cela modifie‑t‑il leur comportement alimentaire à l’âge adulte — et des bactéries intestinales amies et des fibres alimentaires spéciales peuvent‑elles renverser ces effets ? En suivant des souris depuis la naissance jusqu’à l’âge adulte, les chercheurs retracent comment un régime « type malbouffe » en début de vie remodelle les microbes intestinaux, les cellules cérébrales qui contrôlent l’appétit et les préférences alimentaires à long terme, avec des différences selon le sexe.
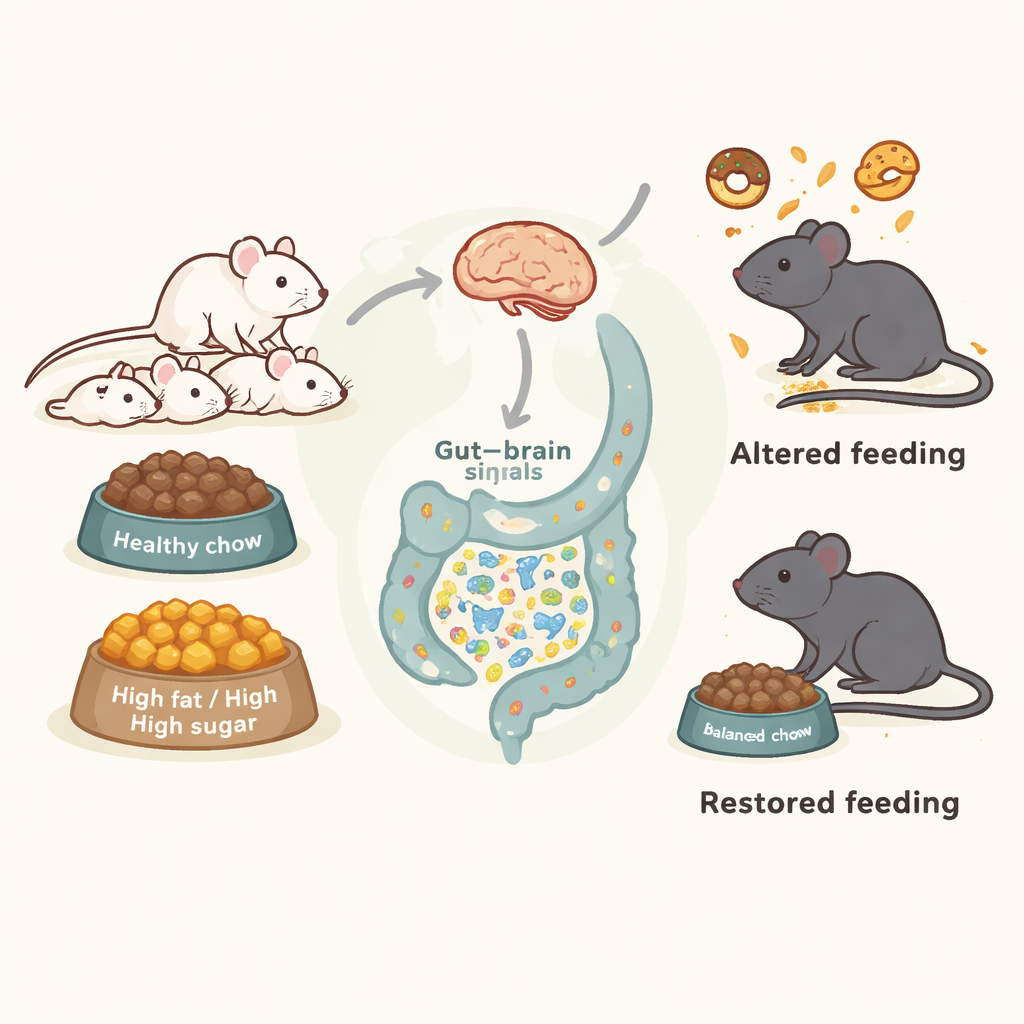
La malbouffe précoce laisse une empreinte cachée
Les souriceaux nouveau‑nés et leurs mères ont reçu soit une alimentation standard saine, soit un régime riche en graisses et en sucres (HFHS) reproduisant un schéma occidental de restauration rapide. Le régime riche n’a été administré que pendant la période précoce — de la naissance jusqu’au sevrage et une courte période après — puis tous les animaux ont été replacés sur une alimentation normale. Malgré cette « correction » tardive et des poids adultes finalement similaires, l’exposition précoce au HFHS a laissé des marques durables. À l’âge adulte, les souris précédemment exposées des deux sexes ont montré une préférence plus marquée pour l’aliment savoureux HFHS lorsqu’on leur proposait un choix, et elles ont adopté davantage le « meurtrissage » de la nourriture — un comportement de manipulation consistant à retirer et broyer la nourriture sans la manger complètement. Ces changements suggèrent qu’un régime précoce peut préparer à la fois l’attrait des aliments riches et la manière dont les animaux interagissent avec eux.
Les microbes intestinaux, intermédiaires entre le régime et le cerveau
L’équipe a suivi de près le microbiote intestinal — les milliards de microbes qui vivent dans l’intestin — et a constaté que le régime HFHS précoce réduisait les bactéries du groupe Bifidobacterium, normalement abondantes en début de vie et liées à la santé métabolique. Les modifications du microbiome ont été accompagnées d’altérations de nombreux composés sanguins, notamment des acides aminés, des molécules liées aux sels biliaires et des dérivés du tryptophane pouvant influencer la fonction cérébrale et l’humeur. De manière cruciale, ces effets n’étaient pas identiques chez les femelles et les mâles. Les femelles présentaient davantage de perturbations dans les voies liées au métabolisme de l’arginine et du tryptophane, tandis que les mâles montraient des changements des molécules liées aux sels biliaires et aux stéroïdes et dans la détection de composants de parois bactériennes. Ces schémas spécifiques au sexe impliquent que le régime précoce pourrait augmenter le risque de maladie par des voies biochimiques différentes chez les femmes et les hommes.
Les circuits cérébraux de l’appétit sont reprogrammés
Parce que l’appétit est coordonné dans l’hypothalamus, une région cérébrale profonde qui intègre les signaux corporels, les chercheurs ont examiné cette structure en détail. Ils ont observé des changements étendus et durables de l’activité génique, particulièrement chez les femelles, chez lesquelles des milliers de gènes étaient davantage modifiés que chez les mâles. Dans un noyau clé de l’hypothalamus appelé noyau arqué, ils ont constaté moins de cellules produisant la POMC, une molécule qui contribue normalement à freiner la prise alimentaire, et moins de cellules portant des récepteurs pour les hormones leptine et ghréline, qui signalent la satiété et la faim. Un autre groupe de neurones inhibiteurs marqué par la molécule PNOC, ainsi que des cellules exprimant le récepteur détecteur de bactéries NOD2, étaient aussi réduits. Ensemble, ces altérations suggèrent que le régime HFHS précoce atténue la capacité du cerveau à lire les signaux relatifs à l’équilibre énergétique et aux microbes intestinaux, prédisposant les animaux à la surconsommation ou à des troubles alimentaires même après normalisation du poids.
Fibres amies et bactéries offrent une remise à zéro partielle
Les auteurs ont ensuite testé deux « rescues » ciblant le microbiote administrés dans l’eau de boisson dès la naissance : un mélange de fibres prébiotiques (fructo‑ et galacto‑oligosaccharides, FOS+GOS) destiné à nourrir les microbes bénéfiques, et une souche spécifique de Bifidobacterium longum (APC1472). Les deux stratégies ont augmenté soit la population globale de Bifidobacterium (FOS+GOS), soit cette souche particulière (APC1472), et ont atténué de nombreux changements comportementaux induits par le régime HFHS précoce. Le meurtrissage de la nourriture et la consommation excessive d’aliments appétents ont été réduits, et chez les mâles, une préférence accrue pour un édulcorant sans calorie a été normalisée. Au niveau cérébral, les deux interventions ont restauré le nombre de neurones POMC et PNOC ainsi que de nombreuses cellules NOD2‑positives dans le noyau arqué, avec une récupération particulièrement marquée chez les femelles. Pourtant, leurs mécanismes différaient : les FOS+GOS ont produit des changements larges de la composition du microbiome et des voies liées à l’axe intestin‑cerveau, tandis que B. longum APC1472 a induit des modifications métaboliques et cérébrales plus ciblées avec une reconfiguration relativement modeste de la communauté microbienne globale.
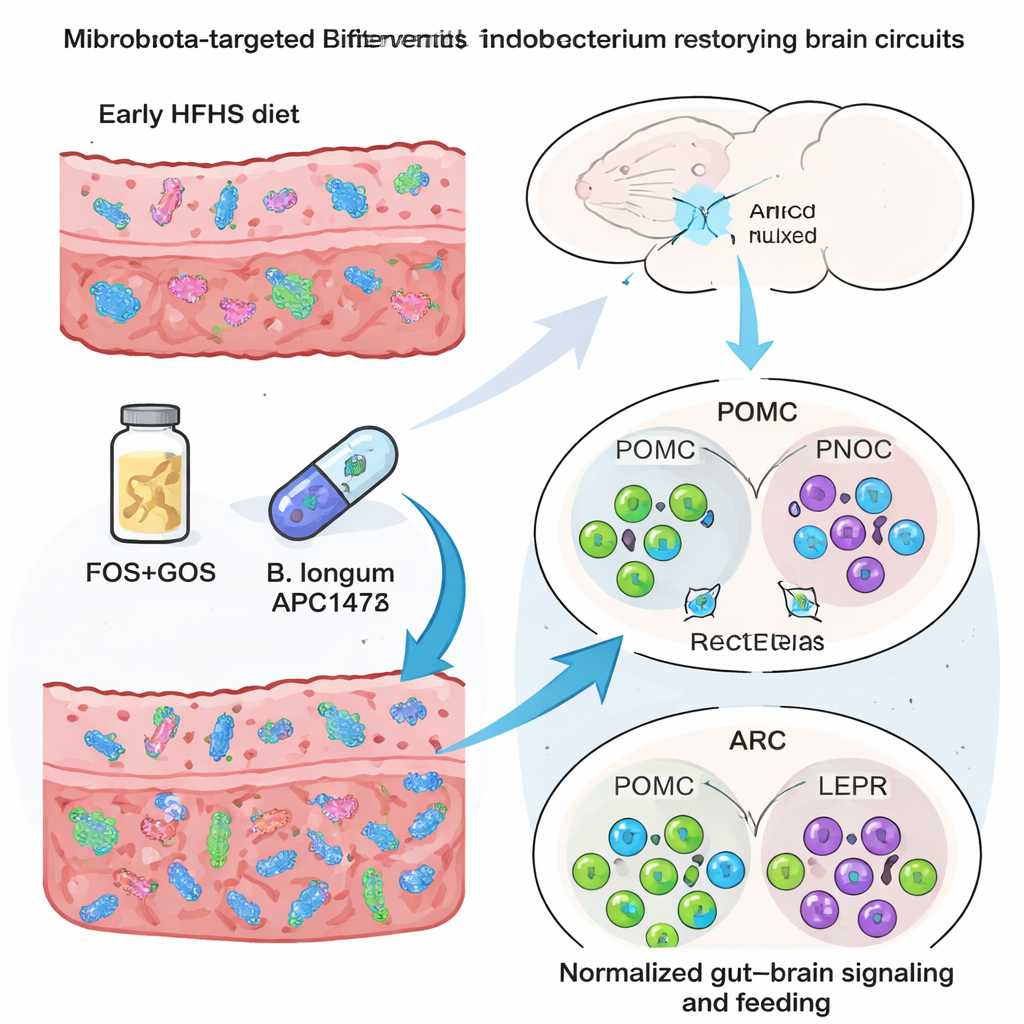
Ce que cela signifie pour les futurs régimes et thérapies
Pour le grand public, le message est à la fois alarmant et porteur d’espoir. Un régime malsain, riche en graisses et en sucres, en début de vie peut laisser des marques profondes de « programmation » sur les bactéries intestinales, la chimie sanguine et les circuits cérébraux qui orientent l’appétit, et ces marques persistent même lorsque des signes extérieurs comme le poids corporel sont revenus à la normale. Les femelles semblent plus vulnérables au niveau des réseaux géniques cérébraux, tandis que les mâles présentent des changements distincts dans la détection des produits bactériens et des hormones. Dans le même temps, des fibres prébiotiques et des souches probiotiques soigneusement choisies peuvent réparer de manière substantielle ces altérations cachées chez la souris, calmer les troubles du comportement alimentaire et rééquilibrer la communication intestin‑cerveau. Bien que des travaux supplémentaires soient nécessaires avant de traduire ces résultats chez l’humain, l’étude renforce l’idée que soutenir un microbiome sain pendant la grossesse et la petite enfance — par l’alimentation et éventuellement des compléments ciblés — pourrait aider à protéger les comportements alimentaires tout au long de la vie et à réduire le risque d’obésité et de troubles associés.
Citation: Cuesta-Marti, C., Ponce-España, E., Uhlig, F. et al. Bifidobacterium longum and prebiotic interventions restore early-life high-fat/high-sugar diet-induced alterations in feeding behavior in adult mice. Nat Commun 17, 1653 (2026). https://doi.org/10.1038/s41467-026-68968-2
Mots-clés: microbiote intestinal, nutrition en début de vie, probiotiques, comportement alimentaire, risque d’obésité