Clear Sky Science · fr
Polymères protéomimétiques hétérobifonctionnels pour la dégradation ciblée de MYC et KRAS
Nouveaux outils pour abattre les protéines les plus résistantes du cancer
Beaucoup des protéines les plus dangereuses qui conduisent le cancer, comme MYC et KRAS, ont longtemps été qualifiées d’« indrogables » parce que les médicaments peinent à s’y accrocher. Cette étude dévoile un nouveau type de matériau synthétique souple — appelés polymères HYDRAC — capables d’attraper ces protéines glissantes et de les envoyer vers le système d’élimination de la cellule. Pour le lecteur, ce travail offre un aperçu de la façon dont la chimie et la nanotechnologie pourraient ouvrir des options thérapeutiques pour des cancers qui résistent aux médicaments traditionnels.
Une ossature flexible plutôt qu’une pilule unique
La plupart des médicaments anticancéreux ciblés sont de petites molécules qui s’emboîtent dans des poches à la surface d’une protéine, comme une clé dans une serrure. Mais des protéines telles que MYC sont souples et dépourvues de poches favorables, tandis que KRAS mute souvent de manière à contourner les médicaments classiques. Les auteurs ont conçu à la place de longues chaînes polymériques constituées d’unités répétées. Le long de ces chaînes, ils ont fixé deux types de composants : de courts segments liant la protéine qui reconnaissent une cible telle que MYC ou RAS, et des segments « dégron » qui recrutent la machinerie d’élimination de la cellule. Parce que de nombreuses copies de chaque composant ornent la même chaîne, une seule molécule HYDRAC peut atteindre plusieurs protéines et enzymes à la fois, ce qui est difficile à réaliser avec une molécule thérapeutique unique et rigide.
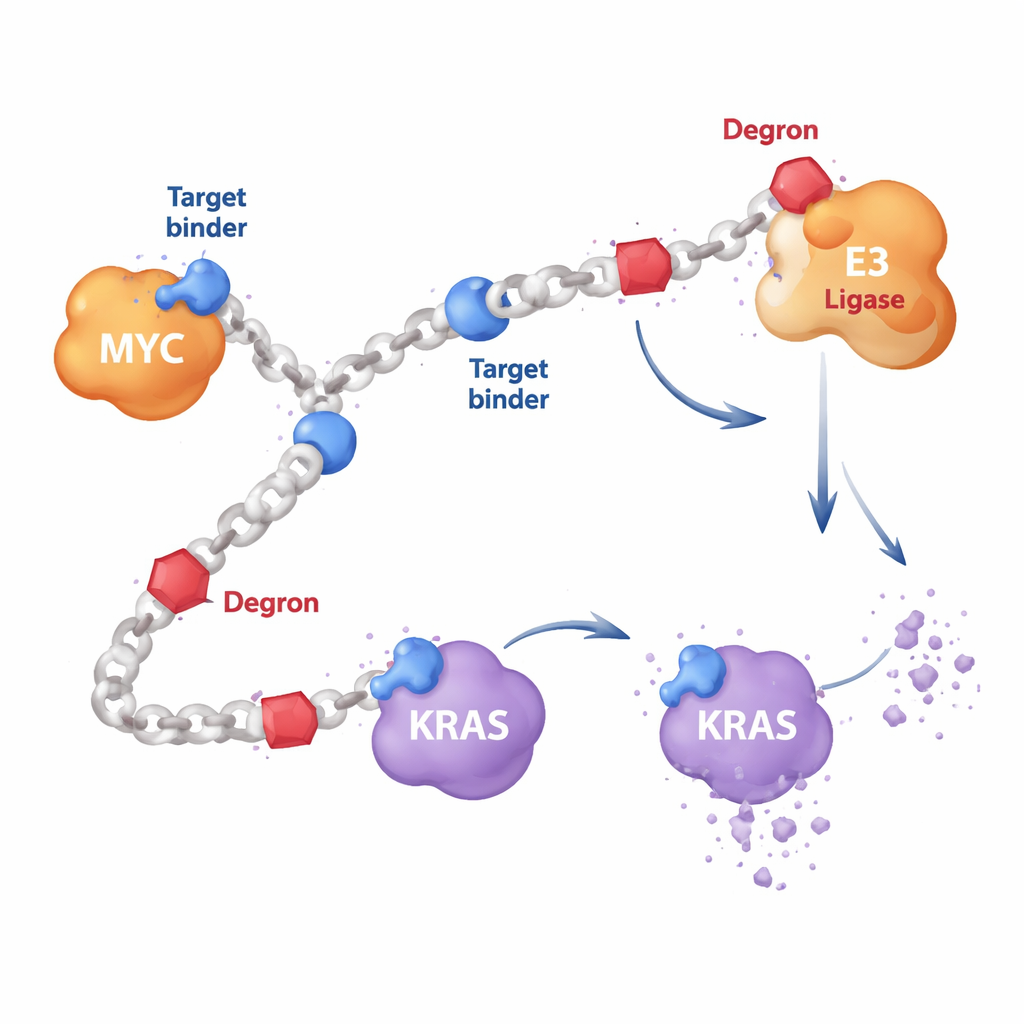
Apprendre aux cellules à dégrader MYC
Pour un premier test, les chercheurs se sont concentrés sur MYC, un commutateur maître qui stimule la croissance dans de nombreux cancers mais résiste depuis des décennies aux attaques directes. Ils ont fabriqué des polymères HYDRAC affichant un peptide connu pour lier MYC, associé à un motif dégron simple qui marque les protéines pour destruction par le protéasome de la cellule, son principal broyeur de protéines. Dans des expériences en éprouvette, ces polymères se sont repliés en formes compactes, proches de protéines, et se sont liés fortement à MYC mais pas à des protéines non liées. Dans des cellules cancéreuses, les HYDRAC ont pénétré facilement, perturbé les programmes géniques contrôlés par MYC et déclenché la mort cellulaire — des effets qui dépendaient de la présence conjointe sur la même chaîne polymérique des composants ciblant et du dégron.
De la culture cellulaire à la réduction des tumeurs
Dans les cellules, le traitement par HYDRAC a provoqué une chute nette des niveaux de protéine MYC sans réduire l’ARN de MYC, indiquant une destruction réelle plutôt qu’une simple extinction de l’expression. Le blocage du protéasome ou d’enzymes clés activant certaines voies de dégradation a permis de restaurer les niveaux de MYC, montrant que les polymères agissent en redirigeant les systèmes d’élimination de la cellule. Des analyses à l’échelle du protéome ont révélé que très peu d’autres protéines étaient affectées, suggérant une sélectivité remarquable. Dans des modèles murins de tumeurs pilotées par MYC, des HYDRAC marqués par fluorescence se sont accumulés préférentiellement dans les tumeurs après injection et y sont restés pendant plusieurs jours. Des doses répétées ont ralenti la croissance tumorale sans perte de poids majeure ni dommages tissulaires évidents, et des échantillons de tumeur montraient moins de cellules en division et davantage de signes d’apoptose.
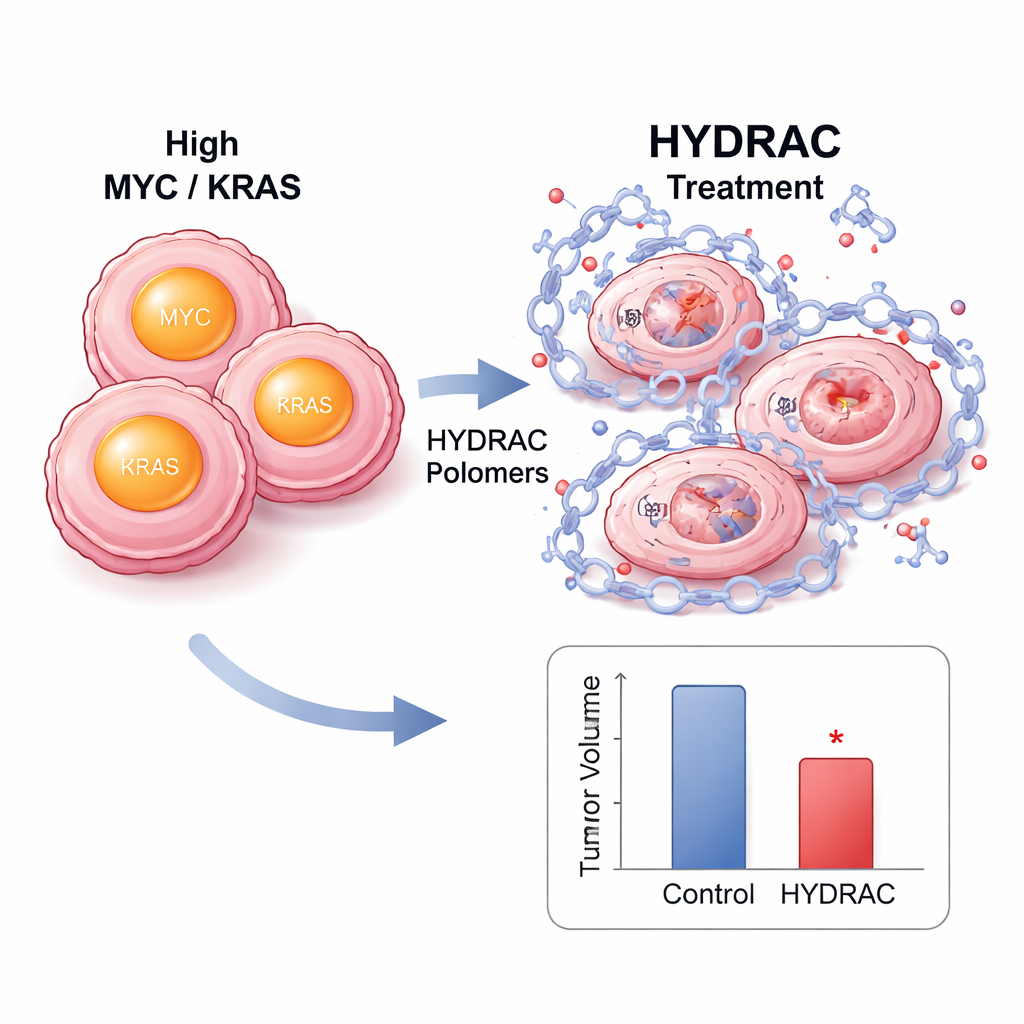
Une plateforme modulable pour de nombreuses cibles pathologiques
Un des points forts de l’approche HYDRAC est que ses groupes latéraux peuvent être échangés comme des pièces interchangeables. L’équipe a remplacé le dégron d’origine par d’autres éléments recruteurs qui mobilisent différentes enzymes cellulaires, y compris celles reconnaissant le médicament thalidomide. Chaque version a dégradé MYC seulement lorsque l’enzyme visée était présente et fonctionnelle, confirmant que les polymères peuvent être réglés pour utiliser des voies cellulaires distinctes. Pour tester la généralité, les chercheurs ont ensuite construit des HYDRAC ciblant RAS en utilisant un peptide qui reconnaît les protéines RAS. Ces constructions ont dégradé avec succès le KRAS mutant dans deux lignées cellulaires cancéreuses différentes, laissant entrevoir un potentiel « pan-KRAS » qui ne dépend pas d’une mutation spécifique — une étape importante pour les cancers où coexistent de nombreuses variantes de KRAS.
Pourquoi cela compte pour les soins futurs contre le cancer
Ce travail présente les HYDRAC comme une nouvelle classe de matériaux programmables qui ne se contentent pas de bloquer les protéines problématiques — ils aident les cellules à les effacer. En combinant de nombreux éléments de ciblage et de dégradation sur un polymère flexible, les HYDRAC contournent les limites de conception des médicaments traditionnels de faible masse et des PROTACs, qui ne portent généralement qu’un seul exemplaire de chaque fonction. Bien qu’il reste beaucoup à faire avant que ces matériaux n’atteignent la clinique, les résultats dans des modèles pilotés par MYC et KRAS suggèrent que des protéines cancéreuses longtemps considérées comme « indrogables » peuvent, en fait, être vulnérables lorsque la médecine ressemble davantage à une brosse moléculaire sur mesure qu’à une petite pilule unique.
Citation: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Mots-clés: dégradation ciblée des protéines, MYC, KRAS, thérapeutiques à base de polymères, nanomédecine contre le cancer