Clear Sky Science · fr
Paysage épigénomique intégratif des cerveaux atteints de la maladie d’Alzheimer révélant des perturbations moléculaires des oligodendrocytes associées au tau
Pourquoi cette recherche cérébrale est importante
La maladie d’Alzheimer est surtout connue pour la perte de mémoire et l’accumulation de deux protéines problématiques dans le cerveau : l’amyloïde et le tau. Pour autant, les personnes atteintes peuvent présenter des schémas de lésions très différents, même avec le même diagnostic. Cette étude pose une question essentielle : quels commutateurs au sein des cellules cérébrales contribuent à déterminer l’ampleur de l’accumulation de ces protéines nocives et leur impact sur différents types cellulaires ? En examinant des marques chimiques sur l’ADN de centaines de cerveaux, les chercheurs révèlent un lien surprenant entre le tau et les cellules qui assurent le câblage du cerveau.
Des marques chimiques sur l’ADN comme commutateurs cachés
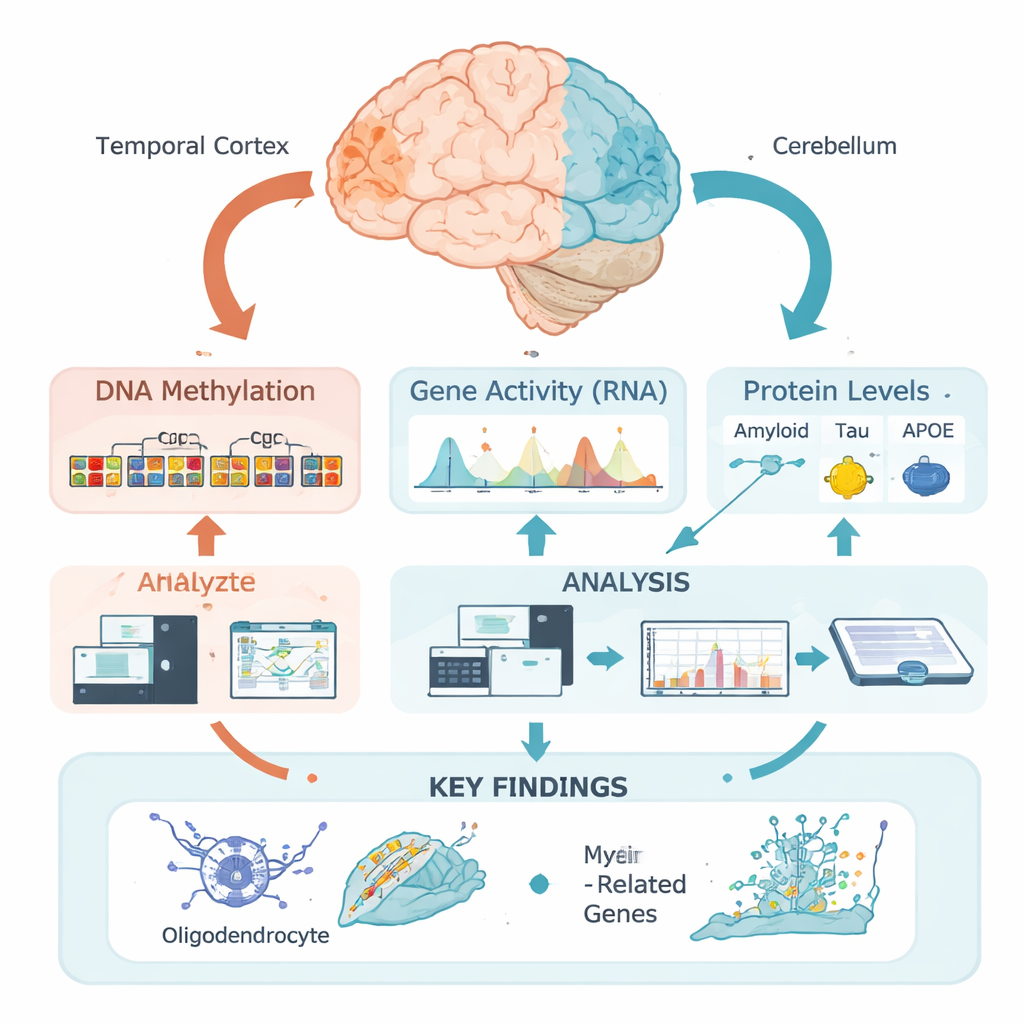
Notre ADN porte les instructions de base pour construire et faire fonctionner les cellules cérébrales, mais ces instructions sont régulées par des marques épigénétiques — des étiquettes chimiques qui peuvent augmenter ou diminuer l’activité des gènes voisins sans modifier le code génétique. L’une des marques les plus importantes est la méthylation de l’ADN, où de petits groupes chimiques se fixent à des sites précis de l’ADN. Plutôt que d’examiner des sites isolés, l’équipe a utilisé une nouvelle approche « régionale » : elle a regroupé de nombreux sites proches en zones fonctionnelles selon la façon dont l’ADN est emballé dans le cortex temporal, une région fortement affectée dans la maladie d’Alzheimer, et dans le cervelet, relativement épargné. Cela leur a permis de demander où, au sens biologique, les schémas de méthylation changent en relation avec les caractéristiques de la maladie.
Relier les marques de l’ADN aux protéines de l’Alzheimer
Les chercheurs ont analysé des tissus cérébraux de 472 personnes chez qui la maladie d’Alzheimer avait été confirmée post mortem. Pour chaque échantillon de cortex temporal, ils ont mesuré en détail les niveaux d’amyloïde, de tau et de protéines APOE sous différentes formes biochimiques, ainsi que les scores microscopiques classiques des plaques amyloïdes et des enchevêtrements de tau. Ils ont ensuite réalisé des études d’association épigénomique à l’échelle du génome, testant si les niveaux régionaux de méthylation de l’ADN suivaient ces mesures. De manière frappante, presque toutes les associations fortes identifiées étaient liées non pas à l’amyloïde, mais au tau — en particulier au tau total soluble et à une forme membranaire phosphorylée (chimiquement modifiée) considérée comme particulièrement toxique.
Un signal fort dans les cellules du câblage cérébral
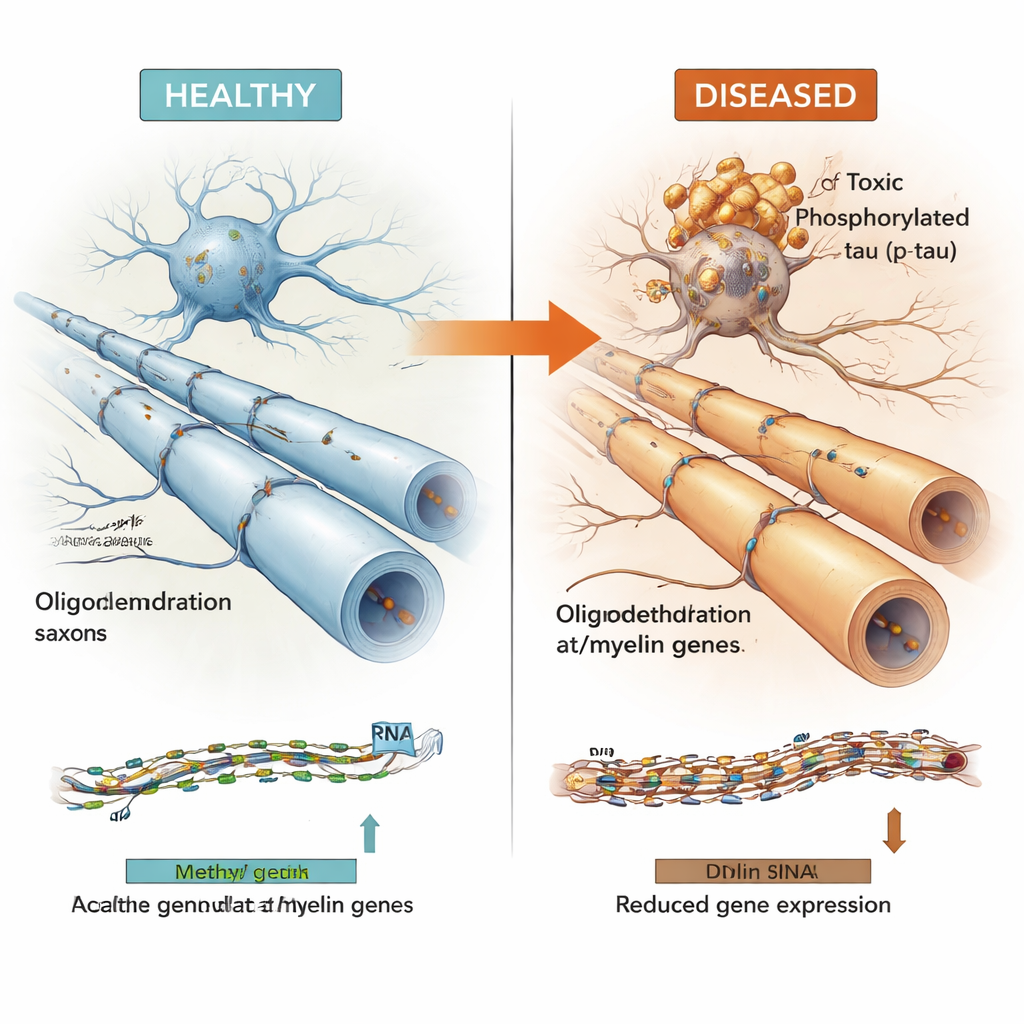
Beaucoup des régions d’ADN associées au tau se trouvaient dans des parties « actives » du génome qui influencent les gènes voisins. En combinant les données de méthylation avec des mesures d’activité génique provenant des mêmes cerveaux, l’équipe a montré que ces régions contrôlaient souvent des gènes utilisés par les oligodendrocytes — les cellules qui entourent les fibres nerveuses d’une gaine isolante de myéline, permettant aux signaux électriques de voyager rapidement et de façon fiable. Des gènes clés liés à la myéline tels que MBP, MAG et MYRF, ainsi que le gène de risque de l’Alzheimer BIN1 et un gène candidat plus récent appelé LDB3, apparaissent dans cet ensemble. Des niveaux plus élevés de tau phosphorylé toxique coïncidaient généralement avec une augmentation de la méthylation à ces régions et une expression réduite des gènes associés aux oligodendrocytes et à la myéline, tandis que le pool plus bénin de tau total soluble montrait le schéma inverse.
Un motif observé dans plusieurs maladies cérébrales
Pour vérifier si ces résultats étaient robustes et généraux, les auteurs ont examiné de grands ensembles de données indépendants provenant d’autres collections de cerveaux Alzheimer, ainsi que de cerveaux affectés par des « tauopathies » primaires telles que la paralysie supranucléaire progressive et la maladie de Pick. Bien que ces cohortes aient été mesurées avec des technologies différentes et souvent dans des régions cérébrales distinctes, de nombreuses mêmes régions d’ADN et gènes d’oligodendrocytes ont montré un comportement cohérent : leurs niveaux de méthylation étaient liés à la charge en enchevêtrements de tau, et leur expression était réduite dans les cerveaux malades et dans des études en cellules uniques portant spécifiquement sur les oligodendrocytes. Il est important de noter que ces schémas ne semblaient pas s’expliquer simplement par la génétique ou par la perte globale de cellules, ce qui suggère un véritable basculement épigénétique dans le fonctionnement des oligodendrocytes.
Ce que cela signifie pour la compréhension de l’Alzheimer
Pris ensemble, les résultats étayent un modèle dans lequel l’augmentation des niveaux de tau nocif est étroitement liée à des changements épigénétiques dans les oligodendrocytes qui affaiblissent l’expression des gènes liés à la myéline, pouvant fragiliser le câblage du cerveau et contribuer au déclin cognitif. On ignore encore ce qui survient en premier — l’accumulation de tau ou la perturbation de ces gènes de la myéline — mais les associations fortes et répétées observées sur des milliers d’échantillons et plusieurs maladies pointent vers un mécanisme partagé. En cartographiant ces commutateurs de l’ADN et en les intégrant dans une « Atlas Multiomique » public, ce travail met en lumière les oligodendrocytes et leur régulation épigénétique comme des cibles prometteuses pour des thérapies futures visant à stabiliser les circuits cérébraux, plutôt que de se concentrer uniquement sur les neurones ou les plaques amyloïdes.
Citation: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Mots-clés: Maladie d’Alzheimer, protéine tau, méthylation de l’ADN, oligodendrocytes, myéline