Clear Sky Science · fr
Base structurale du signalement et de la modulation du canal humain activé par le zinc (ZAC)
Comment un oligo‑élément aide les cellules nerveuses à communiquer
Le zinc est surtout connu comme nutriment dans les comprimés multivitaminés, mais dans l’organisme ce métal joue aussi le rôle d’un messager chimique rapide dans le cerveau. L’étude décrite ici révèle, à résolution atomique, comment une protéine peu connue appelée canal activé par le zinc (ZAC) détecte le zinc à l’extérieur des cellules et convertit ce signal en une réponse électrique. Comprendre cette porte particulière de la membrane cellulaire pourrait éclairer la manière dont le zinc module l’activité cérébrale et suggérer de nouvelles voies pour ajuster les signaux nerveux en santé et en maladie.
Une porte spéciale pour les signaux au zinc
Beaucoup des messages rapides entre cellules nerveuses sont véhiculés par des molécules familières comme la sérotonine ou l’acétylcholine, qui ouvrent des canaux en forme d’anneau dans la membrane. ZAC est un parent lointain de ces récepteurs, mais au lieu de répondre à une molécule organique, il est activé par des ions métalliques comme le zinc, le cuivre et les protons. ZAC est présent dans de nombreux tissus humains, y compris le cerveau, mais il est absent chez des animaux de laboratoire classiques comme les souris et les rats, ce qui a ralenti les avancées. Ce travail utilise la cryo‑microscopie électronique à haute résolution pour capturer plusieurs clichés tridimensionnels du ZAC humain : dans son état de repos, lié au zinc, et lié à deux médicaments différents qui ferment le canal. Ensemble, ces structures révèlent comment le zinc se place au sommet du canal, comment les ions le traversent et comment des bloqueurs maintiennent la porte fermée ou la coincent ouverte dans un état non conductant.
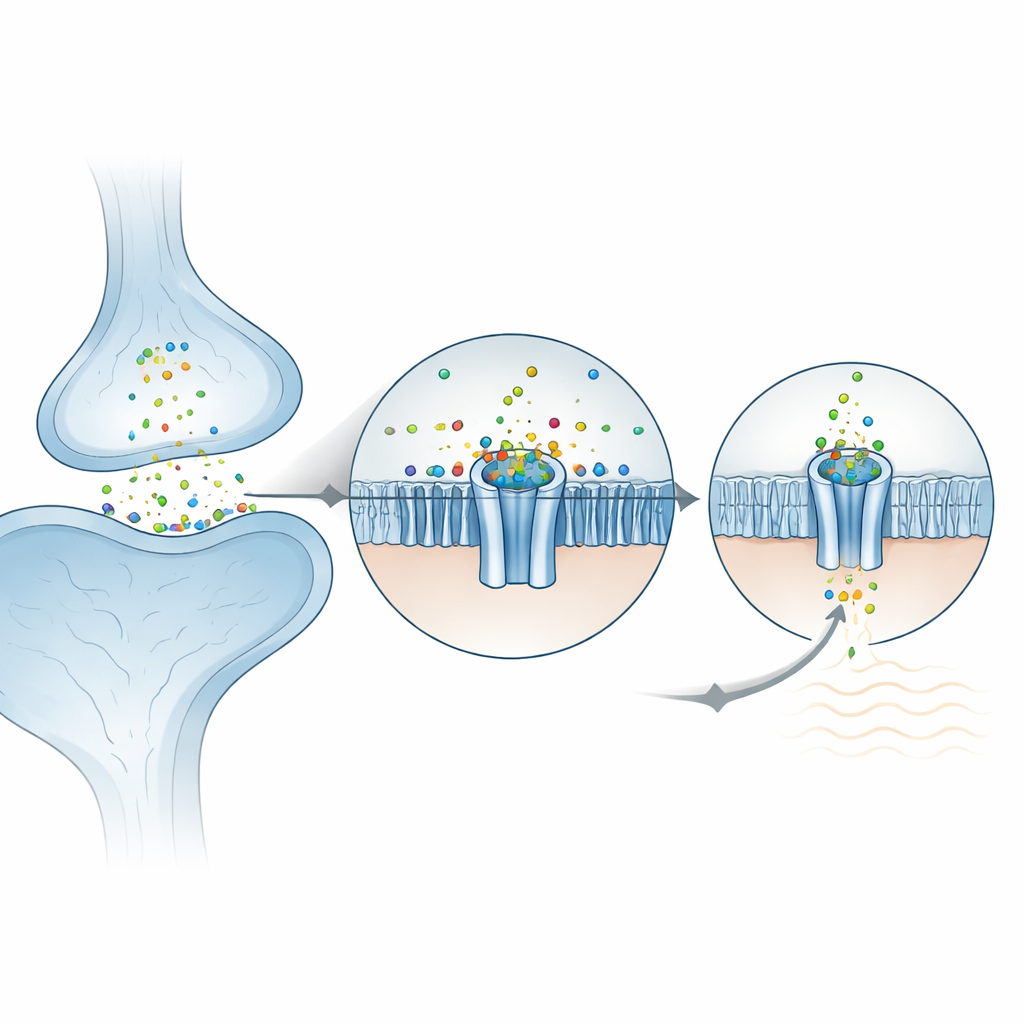
Comment le zinc se verrouille dans le canal
À la surface externe de la cellule, ZAC est composé de cinq sous‑unités identiques formant une rosette. Les chercheurs ont trouvé que des ions zinc se logent dans cinq poches équivalentes, chacune située entre deux sous‑unités voisines dans le domaine externe. De manière surprenante, le zinc n’est pas retenu par les acides aminés « classiques » qui lient habituellement les métaux (comme l’histidine ou la cystéine). Il est plutôt soutenu principalement par deux chaînes latérales aromatiques en anneau qui stabilisent l’ion chargé positivement via de dites interactions cation–π. Lorsque ces résidus clés ont été mutés dans des ovocytes de grenouille utilisés pour des enregistrements électriques, le canal a perdu sa réponse au zinc, confirmant leur rôle central. L’environnement entourant est déjà pré‑organisé, ce qui aide à expliquer pourquoi ZAC présente une activité spontanée notable même sans zinc : la protéine se trouve proche d’un point de basculement entre fermé et ouvert, et le zinc ne fait que pousser l’équilibre.
Le passage des ions et une variante génétique courante
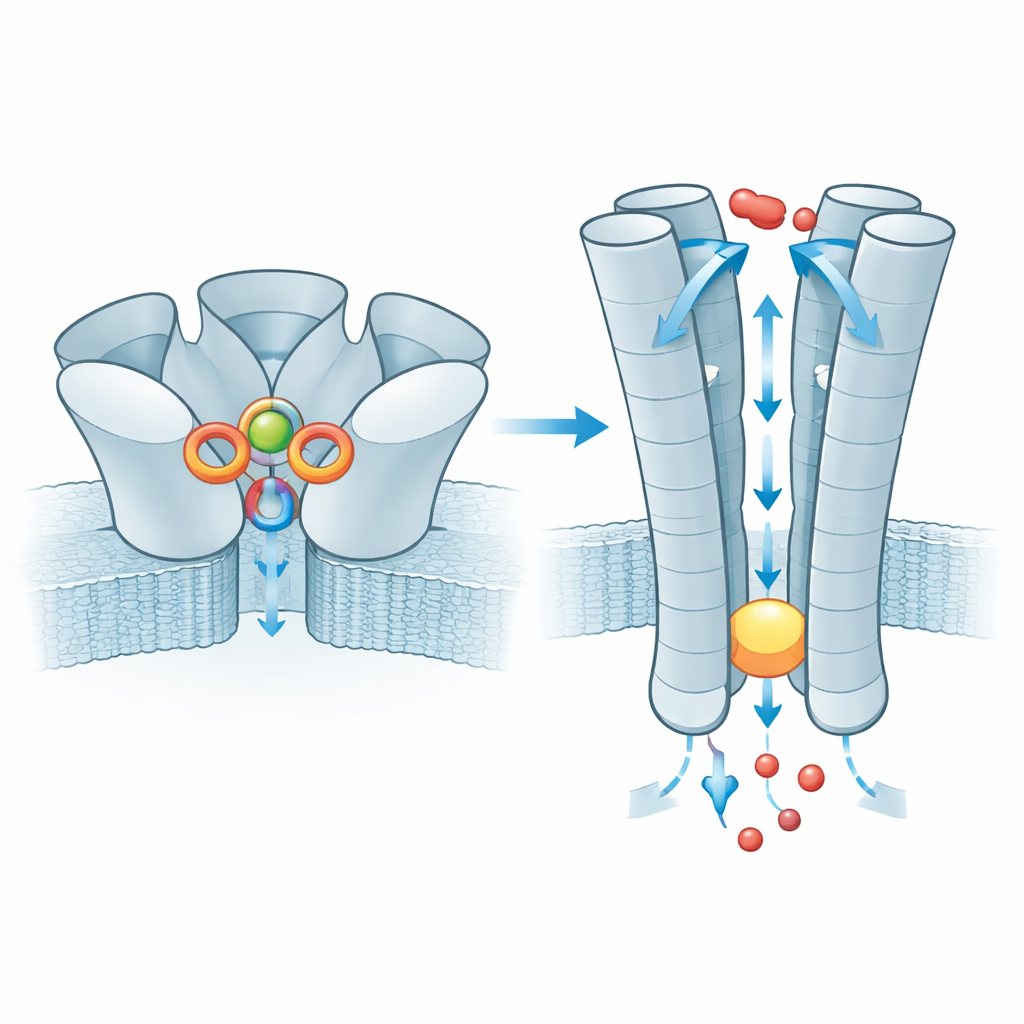
Une fois le zinc lié, l’effet est transmis à la partie traversant la membrane de ZAC, où cinq hélices internes forment le pore. À l’état repos, ce tube se rétrécit au niveau d’un anneau de résidus de leucine, créant un bouchon hydrophobe qui bloque le passage des ions. Avec le zinc lié, le bouchon s’élargit juste assez pour laisser passer de petits ions positifs tels que le sodium et le potassium, tandis que le revêtement chargé du pore aide à sélectionner ces ions. L’équipe a également examiné une variante humaine très courante de ZAC dans laquelle un seul acide aminé (thréonine) est remplacé par une alanine dans un court brin situé au‑dessus du bouchon. Ce petit changement affaiblit un réseau d’interactions entre sous‑unités voisines qui transmet normalement la liaison du zinc à la porte, et des mesures électriques montrent que les canaux construits à partir de cette variante conduisent des courants bien plus faibles. La variante agit donc comme un convertisseur de signal moins efficace, bien que son impact sur la physiologie humaine reste inconnu.
Comment deux médicaments rendent le canal silencieux
Outre le zinc, l’étude explore aussi comment deux antagonistes, le TTFB et la d‑tubocurarine (d‑TC), ferment ZAC. Le TTFB est une petite molécule créée sur mesure qui s’insère profondément dans la région membranaire, se glissant entre deux des hélices formant le pore juste au‑dessus de la porte. Là, elle interagit avec une poche hydrophobe ajustée et des résidus polaires à proximité, calant efficacement les hélices pour qu’elles ne puissent pas se déplacer vers un état pleinement ouvert et conducteur. La d‑TC, un médicament plus ancien autrefois utilisé comme relaxant musculaire, agit de manière plus diffuse. Une molécule de d‑TC se lie dans la même poche externe qui accueille normalement le zinc, imitant la charge positive du zinc mais empêchant le zinc réel de se lier correctement. Une seconde molécule de d‑TC se place à l’entrée du pore lui‑même, bouchant physiquement le tunnel. Ensemble, ces liaisons piègent ZAC dans une conformation désensibilisée et non conductrice alors que la forme de la protéine reste relativement ouverte.
Ce que ces découvertes signifient pour le zinc et la santé
Ce travail structural montre en détails moléculaires clairs que ZAC est un véritable détecteur du zinc, utilisant un berceau aromatique inhabituel pour percevoir le métal au même type de site où d’autres membres de la famille lient des neurotransmetteurs. Il identifie aussi des réseaux d’interactions spécifiques qui ajustent la facilité d’ouverture et de fermeture du canal, et cartographie deux sites distincts de liaison aux médicaments qui peuvent soit caler la porte fermée soit boucher le pore. Pour un public non spécialiste, le message principal est que le zinc n’est pas seulement un nutriment statique mais un signal actif, et que ZAC en est l’un des détecteurs dédiés. À mesure que les scientifiques recherchent les rôles de ZAC dans l’organisme humain et dans les troubles neurologiques liés au déséquilibre en zinc, ces plans à l’échelle atomique fournissent une feuille de route pour concevoir des molécules plus précises afin de moduler ce canal et, potentiellement, de corriger une signalisation au zinc perturbée.
Citation: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Mots-clés: signalisation au zinc, canaux ioniques activés par ligand, neurosciences, structure cryo‑EM, modulation des canaux