Clear Sky Science · fr
La palmitoylation d'ASCT2 régulée par l’axe JNK1–ZDHHC14 orchestre le métabolisme du glutamine et la progression du NSCLC
Alimenter l’incendie du cancer du poumon
De nombreux cancers pulmonaires à croissance rapide sont dépendants du glutamine, un acide aminé courant qui sert à la fois de carburant et de matériau de construction. Cette étude révèle comment les cellules tumorales ajustent finement une « porte » majeure d’entrée du glutamine à leur surface et comment perturber ce système de contrôle pourrait ralentir la croissance tumorale. Comprendre cette vanne d’alimentation cachée aide à expliquer pourquoi certains tumeurs sont si difficiles à affamer et pointe vers de nouvelles combinaisons médicamenteuses susceptibles de couper leur approvisionnement en énergie plus efficacement.
Une porte cellulaire pour le glutamine
Le glutamine pénètre dans les cellules principalement via une protéine de transport appelée ASCT2, située dans la membrane externe et qui fait entrer le glutamine. Le cancer du poumon non à petites cellules (NSCLC), la forme la plus fréquente de cancer du poumon, dépend souvent fortement du glutamine pour soutenir sa division rapide et sa survie. Des niveaux élevés d’ASCT2 dans les tumeurs sont associés à une maladie agressive et à un mauvais pronostic pour les patients. Pourtant ASCT2 lui‑même est constamment synthétisé, modifié et dégradé, ce qui pose la question : qu’est‑ce qui détermine la quantité de ce gardien qui reste à la surface cellulaire à un moment donné ?
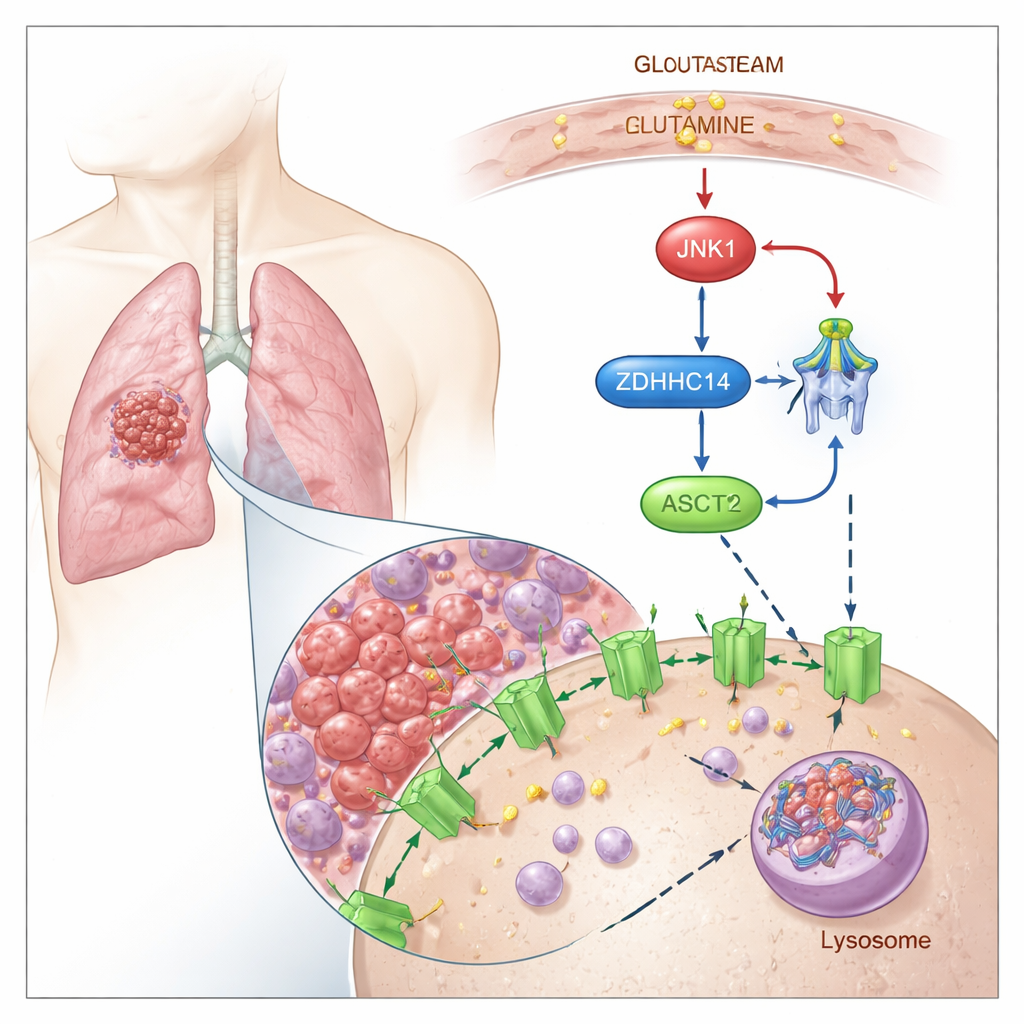
Marquer ASCT2 pour la dégradation
Les chercheurs montrent qu’ASCT2 est contrôlé par une « étiquette » chimique appelée palmitoylation, dans laquelle un acide gras est fixé sur des cystéines spécifiques de la protéine. Ils ont découvert qu’une enzyme nommée ZDHHC14 ajoute cette étiquette lipidique sur deux sites conservés d’ASCT2 (Cys39 et Cys48). Une fois marqué, ASCT2 est réorienté depuis la surface cellulaire vers des centres de recyclage cellulaires appelés lysosomes, où il est dégradé. Bloquer la palmitoylation empêche ASCT2 d’être marqué et dégradé, entraînant une augmentation des niveaux de la protéine ASCT2 et une hausse de l’entrée du glutamine, sans modifier l’activité génique sous‑jacente.
Une contre‑enzyme qui protège la porte
En opposition à ZDHHC14 se trouve une autre enzyme, ABHD17B, qui enlève l’étiquette lipidique d’ASCT2. Lorsque ABHD17B est active, ASCT2 est moins palmitoylée, plus stable et plus susceptible d’être recyclée vers la surface cellulaire plutôt que dirigée vers le lysosome. Cet aller‑retour d’étiquetage et de désétiquetage agit comme un bouton finement réglé du flux de glutamine : ZDHHC14 pousse ASCT2 vers la destruction, tandis qu’ABHD17B le sauve et maintient le transport du glutamine. Dans les cellules de cancer du poumon, déplacer cet équilibre vers moins de palmitoylation augmente l’absorption du glutamine et favorise la croissance tumorale in vitro et chez la souris.
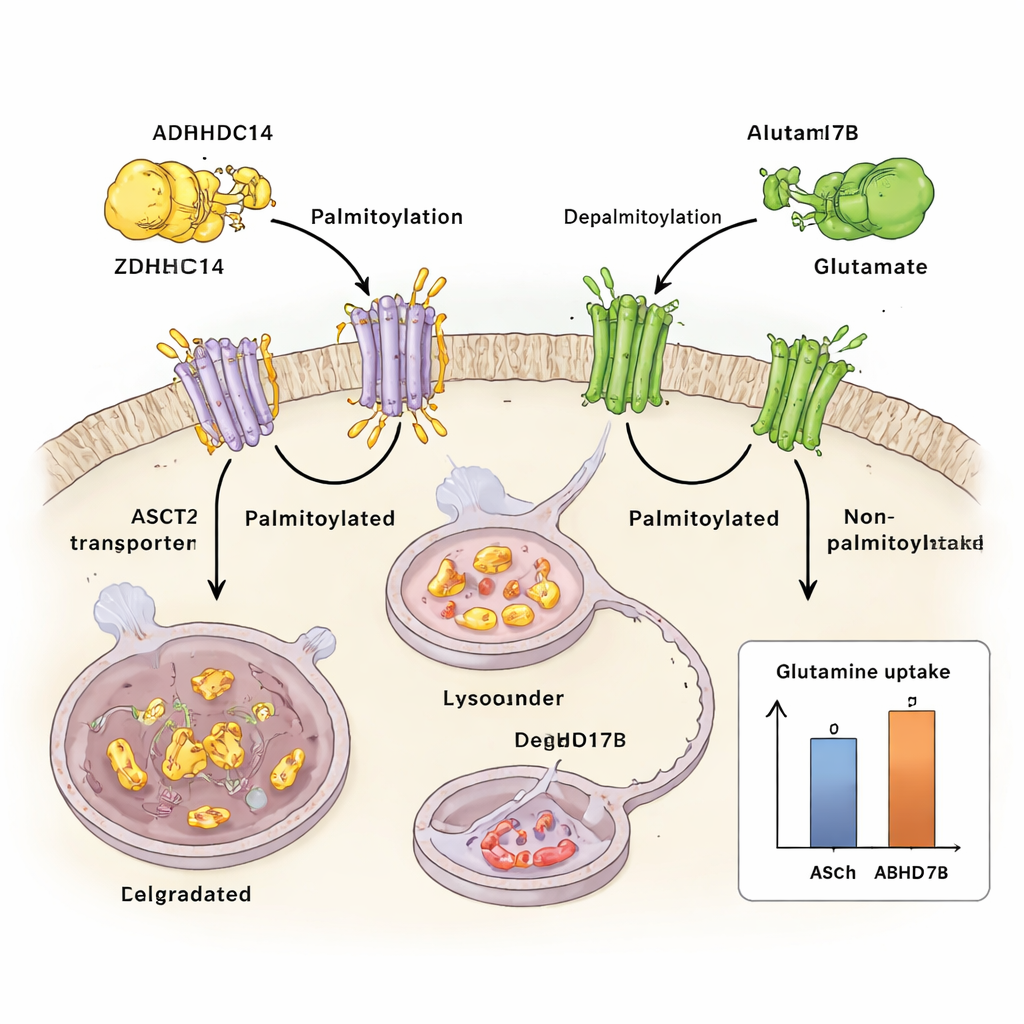
Comment le stress nutritif reprogramme le système
L’équipe a ensuite examiné ce qui se passe lorsque les cellules tumorales manquent de glutamine. En cas de privation de glutamine, une protéine de signalisation sensible au stress appelée JNK1 s’active. JNK1 se lie physiquement à ZDHHC14 et ajoute un groupe phosphate à un site spécifique (Thr440), marquant ZDHHC14 pour sa propre dégradation lysosomale. À mesure que les niveaux de ZDHHC14 diminuent, ASCT2 reçoit moins de marques de palmitoylation, échappe à la dégradation et s’accumule à la surface cellulaire — précisément quand la cellule a le plus besoin de récupérer le glutamine rare. La mutation de ce seul site sensible à JNK1 stabilise ZDHHC14, restaure l’étiquetage d’ASCT2 et réduit l’absorption du glutamine, ce qui souligne à quel point le stress nutritif est intégralement connecté à cette boucle de contrôle.
Transposer le mécanisme en thérapie
Étant donné l’importance d’ASCT2 pour le métabolisme tumoral, des médicaments qui le bloquent, comme le composé expérimental V9302, sont étudiés comme traitements anticancéreux. Cette étude révèle que la signalisation JNK1 peut contrebalancer la destruction d’ASCT2, protégeant de fait la porte au glutamine. Dans des modèles cellulaires et murins de NSCLC, la combinaison d’un inhibiteur de JNK avec V9302 réduit plus fortement l’absorption du glutamine, la croissance des cellules tumorales et la taille des tumeurs que chaque médicament pris isolément. Des échantillons de patients et des bases de données publiques montrent en outre que de faibles niveaux de ZDHHC14 et des niveaux élevés d’ASCT2 sont fréquents dans le NSCLC et associés à une survie réduite, suggérant que ce profil moléculaire pourrait aider à identifier les patients les plus susceptibles de bénéficier du ciblage de cette voie.
Ce que cela signifie pour les patients
Concrètement, ce travail montre que certains cancers du poumon contrôlent leur carburant préféré en ajustant une vanne moléculaire à leur surface. Un trio d’acteurs — JNK1, ZDHHC14 et ABHD17B — décide si la porte au glutamine ASCT2 est marquée pour destruction ou maintenue ouverte. Lorsque le glutamine se fait rare, le système bascule pour préserver ASCT2 et maintenir le flux d’énergie, aidant les tumeurs à survivre dans des conditions difficiles. En bloquant simultanément ASCT2 et la voie JNK qui le protège, les chercheurs ont pu affamer plus efficacement les cellules cancéreuses dans des modèles de laboratoire et chez l’animal. Bien que des tests supplémentaires soient nécessaires, cet axe phosphorylation–palmitoylation offre un nouvel angle prometteur pour des thérapies visant à couper les lignes de vie nutritives des tumeurs pulmonaires affamées de glutamine.
Citation: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Mots-clés: métabolisme du glutamine, cancer du poumon non à petites cellules, transporteur ASCT2, palmitoylation des protéines, signalisation JNK