Clear Sky Science · fr
L'axe AdipoR1–AMPK supprime le cancer du sein à travers les sous‑types moléculaires via des voies de mort cellulaire multimodales, y compris la ferroptose et l'apoptose
Pourquoi les cellules graisseuses comptent pour le cancer du sein
La plupart d'entre nous considèrent la graisse corporelle comme une réserve d'énergie passive, mais les adipocytes sont des véritables usines actives qui libèrent hormones et molécules de signalisation dans la circulation sanguine. Cette étude examine comment l'un de ces signaux d'origine adipeuse, agissant via une molécule appelée AdipoR1 sur les cellules du cancer du sein, peut ralentir la croissance tumorale. Le travail est important car il suggère une nouvelle façon de traiter de nombreuses formes de cancer du sein en exploitant la communication entre le tissu adipeux et les tumeurs, potentiellement en renforçant l'effet des médicaments existants.
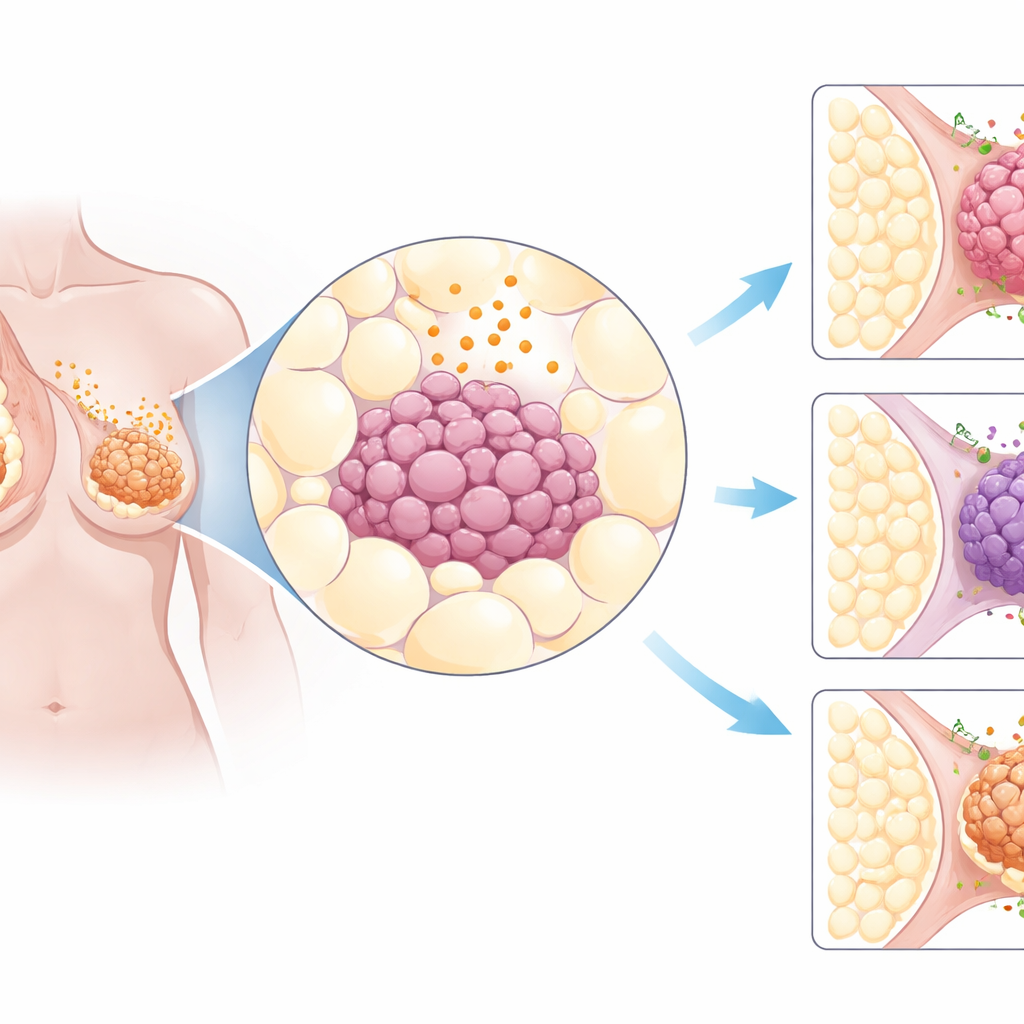
Un regard à travers de nombreux cancers
Les chercheurs ont commencé par exploiter de larges bases de données publiques sur le cancer contenant des informations génétiques de milliers de tumeurs de patients. Ils se sont concentrés sur une trentaine de gènes impliqués dans les signaux provenant du tissu adipeux et les structures cellulaires qui reçoivent ces signaux. En comparant des tumeurs provenant de 31 organes différents avec des tissus sains, un schéma est ressorti : les cancers du sein présentaient des altérations particulièrement marquées de ces signaux liés à la graisse. En particulier, le récepteur AdipoR1 était fréquemment exprimé à des niveaux supérieurs à la normale dans les tumeurs mammaires, que celles‑ci soient dépendantes des hormones, HER2‑positives ou du type plus agressif triple négatif. Des prélèvements tissulaires de plus de 600 cancers du sein ont confirmé que la protéine AdipoR1 était largement présente dans les cellules tumorales.
Tester un médicament activant le signal adipeux sur des cellules cancéreuses
Pour savoir ce que fait réellement AdipoR1 au sein des tumeurs, l'équipe a utilisé des lignées cellulaires de cancer du sein cultivées en laboratoire, représentant plusieurs sous‑types courants. Ils ont traité ces cellules avec l'AdipoRon, une petite molécule qui active AdipoR1. AdipoRon a rapidement déclenché un commutateur de détection énergétique connu dans les cellules, appelé AMPK, montrant que le signal passait bien. À mesure que la dose d'AdipoRon augmentait, les cellules cancéreuses se divisaient plus lentement, se déplaçaient moins dans des tests de cicatrisation et nombre d'entre elles ont subi l'autodestruction programmée. Lorsque les chercheurs ont délibérément réduit les niveaux d'AdipoR1 dans les cellules, l'effet d'AdipoRon a fortement diminué, alors qu'augmenter AdipoR1 rendait le médicament plus efficace, reliant ainsi directement l'effet à ce récepteur.
Plusieurs façons de pousser les cellules cancéreuses vers la mort
En analysant l'activité génique après traitement, les scientifiques ont constaté qu'AdipoRon déclenchait des réponses au stress à l'intérieur des cellules de cancer du sein. Il a activé des gènes liés à l'apoptose classique ainsi que ceux impliqués dans une forme plus récemment reconnue de destruction cellulaire dépendante du fer, appelée ferroptose. Des marqueurs clés de ce processus ont augmenté au niveau de l'ARN et de la protéine, en particulier dans les cellules de cancer du sein sensibles aux hormones, et des mesures chimiques ont confirmé l'oxydation des lipides cellulaires, soutenant cette observation. Parallèlement, AdipoRon a réduit les niveaux de protéines qui aident normalement les cellules cancéreuses à survivre, y compris des acteurs de la réparation de l'ADN (BRCA1 et BRCA2), le récepteur d'œstrogènes qui stimule la croissance dans de nombreuses tumeurs, et TROP2, une molécule de surface associée à un comportement agressif.
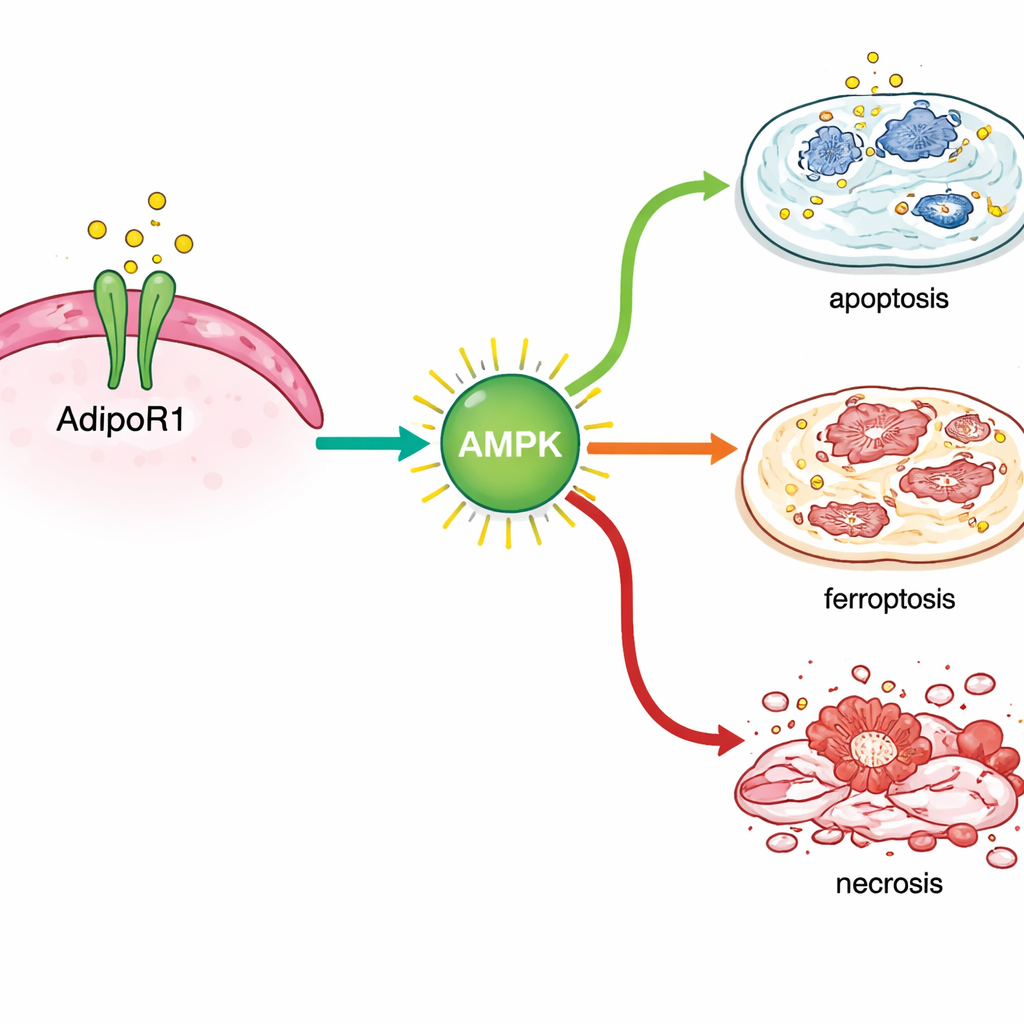
Travailler avec, et non contre, les traitements actuels
L'équipe s'est ensuite demandé si l'activation d'AdipoR1 pouvait compléter les médicaments standards. Dans les cellules de cancer du sein sensibles aux hormones, la combinaison d'AdipoRon et du tamoxifène a produit une inhibition de la croissance plus importante que chaque médicament seul. Dans les lignées triple négatif, AdipoRon a renforcé l'effet d'agents chimiothérapeutiques courants tels que le paclitaxel et la doxorubicine. Chez des souris porteuses de tumeurs mammaires sensibles aux hormones, les chercheurs ont administré AdipoRon par voie orale. Les tumeurs des animaux traités ont croisé plus lentement et contenaient des zones nécrosées plus étendues à l'examen histologique. Fait important, les souris n'ont pas montré d'effets secondaires évidents sur le comportement, le poids ou la santé hépatique durant la période de traitement.
Ce que cela pourrait signifier pour les patients
Dans l'ensemble, les résultats suggèrent que l'activation d'AdipoR1 dans les cellules du cancer du sein mobilise plusieurs voies chevauchantes de mort cellulaire tout en affaiblissant des systèmes de survie clés, et que cette approche fonctionne à travers différentes formes génétiques de la maladie. Plutôt que de remplacer les thérapies actuelles, des médicaments ciblant AdipoR1 comme l'AdipoRon pourraient servir d'adjuvants rendant les tumeurs plus vulnérables à l'hormonothérapie, à la chimiothérapie ou aux futurs agents ciblés. Avant que cette stratégie n'atteigne la clinique, il faudra développer des activateurs d'AdipoR1 plus puissants et sélectifs, clarifier quels patients ont des tumeurs exprimant le récepteur de manière marquée, et évaluer soigneusement la sécurité. Néanmoins, ce travail pointe une idée intrigante : les signaux émanant de notre tissu adipeux pourraient être redirigés pour aider à combattre le cancer du sein plutôt que de le nourrir.
Citation: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Mots-clés: cancer du sein, adipokines, AdipoR1, voies de mort cellulaire, métabolisme du cancer