Clear Sky Science · fr
Rôle des radeaux lipidiques dans le signal oncogénique médié par FGFR2c via l’implication du canal TRPA1 dans les cellules d’adénocarcinome canalaire pancréatique
Pourquoi de petites îles dans la membrane cellulaire comptent
Le cancer du pancréas fait partie des cancers les plus meurtriers, en partie parce que ses cellules sont particulièrement efficaces pour se détacher de la tumeur initiale et envahir les tissus voisins. Cette étude examine de minuscules « îles » à la surface des cellules cancéreuses, composées de cholestérol et de lipides, et pose une question simple aux implications importantes : ces îles aident-elles à activer un signal de croissance qui rend le cancer du pancréas plus agressif, et leur perturbation peut-elle ralentir ce processus ?
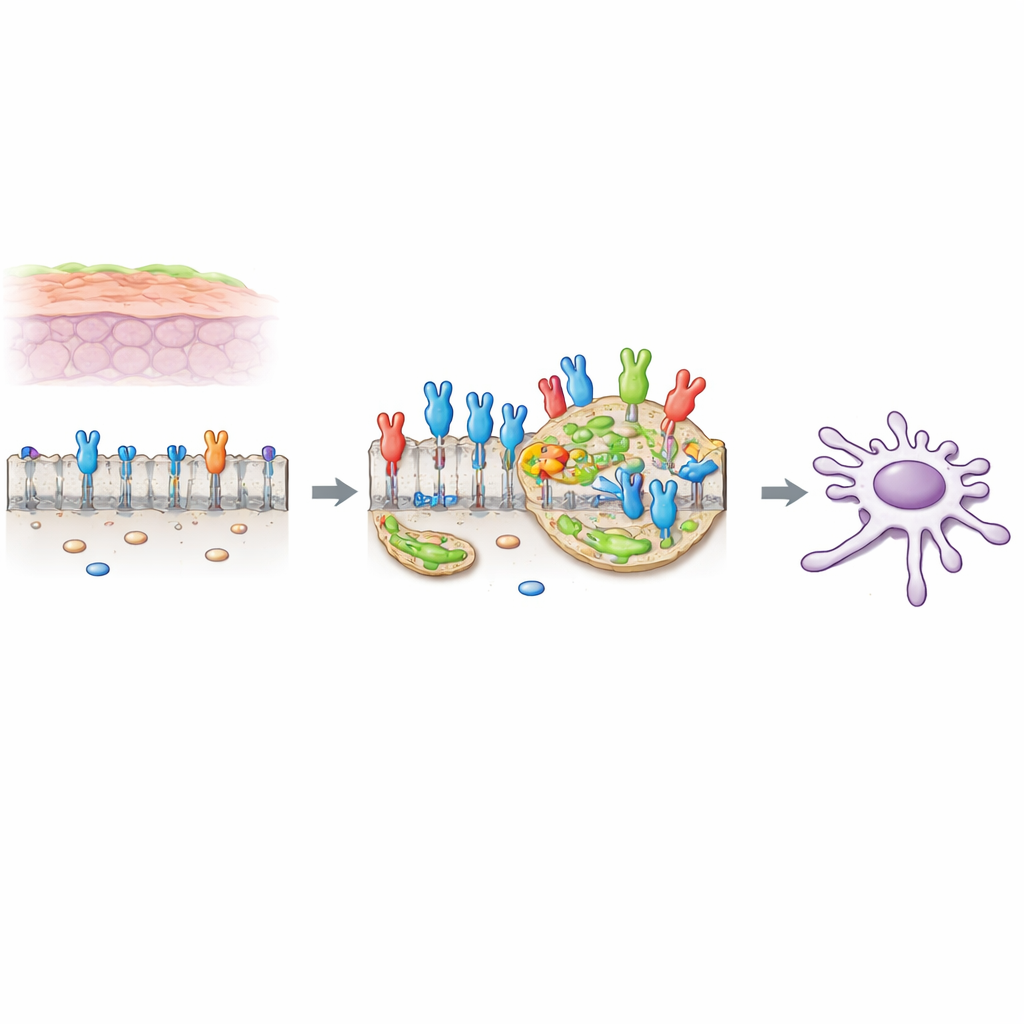
Un interrupteur pro‑cancer à la surface cellulaire
De nombreuses cellules portent à leur surface des interrupteurs qui répondent à des signaux de croissance. L’un de ces interrupteurs, appelé FGFR2c, est une variante que l’on trouve normalement dans des cellules plus flexibles et mobiles, mais qui devient anormalement abondante dans les cellules d’adénocarcinome canalaire pancréatique (PDAC). Lorsqu’il est activé par sa molécule partenaire dans l’environnement, il déclenche des changements connus sous le nom de transition épithélio‑mésenchymateuse (EMT), qui rendent les cellules moins attachées et plus aptes à se déplacer et à envahir. Des travaux antérieurs des auteurs ont montré que, dans les cellules PDAC, FGFR2c active une cascade de messagers internes impliquant une protéine appelée PKCε et plusieurs voies de croissance classiques, renforçant la survie, la mobilité et l’invasion cellulaires.
Des îles riches en cholestérol comme amplificateurs de signal
La membrane externe d’une cellule n’est pas uniforme. Elle contient de petites zones riches en cholestérol appelées radeaux lipidiques, qui servent de plates‑formes miniatures où les molécules de signalisation peuvent se regrouper et communiquer plus efficacement. Les chercheurs ont constaté que lorsque FGFR2c est activé par son signal externe, davantage de récepteurs se déplacent vers ces radeaux lipidiques. À l’aide de marqueurs fluorescents et de fractionnements biochimiques, ils ont montré que FGFR2c activé se concentre dans ces zones, tandis que sa distribution en dehors des radeaux passe d’un motif uniforme à un motif ponctué, cohérent avec un regroupement du récepteur sur ces îles.
Déstabiliser les îles affaiblit les traits cancéreux
Pour tester si ces îles lipidiques sont essentielles aux effets pro‑cancer de FGFR2c, l’équipe a utilisé un composé (méthyl‑β‑cyclodextrine) qui élimine sélectivement le cholestérol de la membrane et déstabilise les radeaux lipidiques sans tuer les cellules. Dans les cellules PDAC riches en FGFR2c, la perturbation des radeaux a fortement réduit l’activation des molécules de signalisation clés en aval du récepteur et atténué le programme EMT : les gènes et protéines associés à un état mobile et invasif ont diminué, tandis que des caractéristiques épithéliales ont été partiellement restaurées. Le même traitement a également abaissé les niveaux de protéines liées à l’invasion comme MCL‑1, SRC et des enzymes dégradant la matrice, et a réduit la capacité des cellules cancéreuses à se déplacer et à pénétrer un gel imitant les tissus environnants. Les cellules contenant très peu de FGFR2c ont montré presque aucune réponse, soulignant à quel point ce partenariat récepteur–radeau est central dans ces tumeurs.
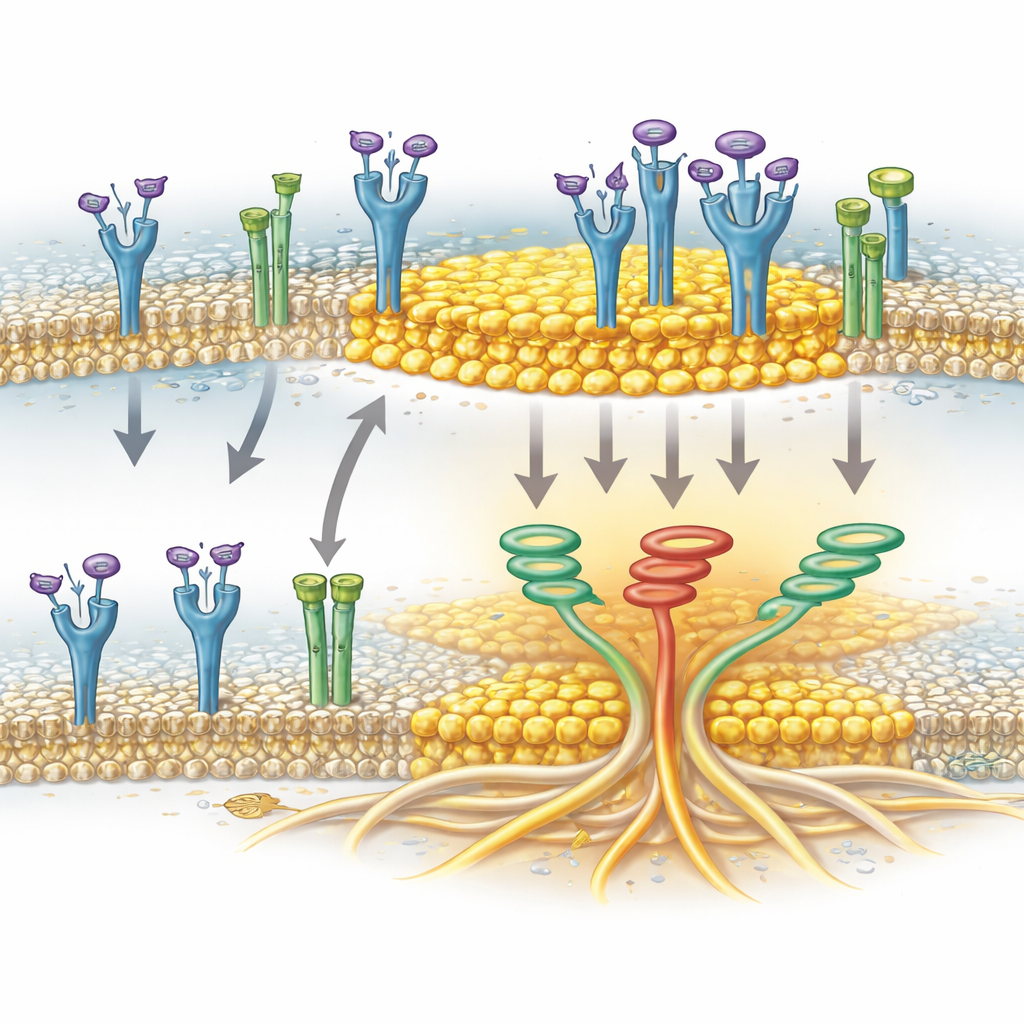
Un canal ionique comme facilitateur du regroupement
L’étude identifie aussi un aide‑surprise : TRPA1, une protéine de canal surtout connue pour la détection d’irritants et du stress oxydatif dans les neurones. Dans les cellules du cancer pancréatique, TRPA1 est présente à la membrane et peut résider dans les radeaux lipidiques. Les auteurs ont montré que TRPA1 s’associe physiquement à FGFR2c lorsque le récepteur est activé et que cette association coïncide avec l’enrichissement de FGFR2c dans les fractions de radeaux. Lorsque les niveaux de TRPA1 ont été réduits, FGFR2c activé ne s’accumulait plus efficacement dans les régions de radeaux, même si les radeaux eux‑mêmes restaient intacts. Cela indique que TRPA1 n’est pas un simple passager mais aide activement à escorter ou stabiliser FGFR2c au sein de ces plates‑formes riches en cholestérol, où le récepteur peut déclencher plus efficacement le réseau de signalisation invasif.
Ce que cela signifie pour les traitements futurs
Dans l’ensemble, ce travail dessine un tableau dans lequel FGFR2c, TRPA1 et les radeaux lipidiques forment une unité coopérative qui renforce le comportement invasif des cellules du cancer pancréatique. FGFR2c fournit le signal de croissance, les radeaux lipidiques offrent la scène physique où s’assemblent les complexes de signalisation, et TRPA1 aide à amener le récepteur sur cette scène. Pour un lecteur non spécialiste, l’idée principale est que non seulement les molécules à l’origine du cancer, mais aussi les micro‑paysages membranaires qu’elles occupent, peuvent déterminer la dangerosité d’une tumeur. En ciblant FGFR2c, TRPA1 ou la stabilité de ces îles riches en cholestérol — seuls ou en combinaison — de futurs traitements pourraient affaiblir la machinerie invasive des cellules du cancer pancréatique de manière plus précise et spécifique à la tumeur.
Citation: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Mots-clés: cancer du pancréas, radeaux lipidiques, FGFR2c, canal TRPA1, invasion cellulaire