Clear Sky Science · fr
Cibler les mutants p53 du cancer Y220C, Y220N et Y220S avec le stabilisateur de petite molécule rezatapopt
Pourquoi cela compte pour les traitements futurs du cancer
Le cancer neutralise souvent p53, une protéine parfois qualifiée de « gardien » de la cellule, en la mutant de manière à ce qu’elle ne puisse plus contrôler les cellules dangereuses. Une modification particulière de p53, connue sous le nom de Y220C, est fréquente dans les tumeurs solides et est devenue un cas d’étude pour des médicaments visant à réparer p53 défaillant plutôt qu’à tuer les cellules directement. Cette étude pose une question pratique et axée sur les patients : un médicament expérimental prometteur, rezatapopt, déjà en essais cliniques pour Y220C, pourrait-il aussi aider des personnes dont les tumeurs portent des mutations voisines mais plus rares en position 220 de p53 ?
Un médicament conçu pour boucher une fissure de p53
Beaucoup de mutations de p53 font que la protéine s’ouvre et perd sa conformation précise. Dans la mutation Y220C, la substitution crée une petite cavité à la surface de la protéine : un défaut que des chimistes ont compris pouvoir « boucher » avec des petites molécules sur mesure pour stabiliser p53. Rezatapopt est l’une de ces molécules, conçue en s’appuyant sur des séries chimiques antérieures qui se lient dans cette cavité et agissent comme une bride moléculaire. Les auteurs se concentrent sur deux autres mutations au même résidu aminé, Y220S et Y220N, qui creusent un creux similaire mais déstabilisent p53 encore davantage que Y220C. Si rezatapopt pouvait également combler ces variantes, cela étendrait potentiellement cette approche de médecine de précision à des milliers de patients supplémentaires chaque année. 
Mesurer dans quelle mesure rezatapopt saisit et stabilise le p53 mutant
Pour tester cela, l’équipe a purifié le domaine central de liaison à l’ADN de p53 portant les substitutions Y220C, Y220S ou Y220N et les a exposés à rezatapopt (et à des analogues chimiques proches). À l’aide d’essais basés sur la chaleur, ils ont montré que les trois protéines mutantes devenaient plus stables lorsque le médicament se liait, Y220C et Y220S retrouvant une robustesse comparable à celle du type sauvage. En revanche, Y220N n’a récupéré qu’une partie de sa stabilité perdue. Une seconde technique mesurant la chaleur libérée lors de la liaison a expliqué pourquoi : rezatapopt se fixe très fortement à Y220C (de l’ordre de quelques dizaines de nanomolaires), un peu moins fortement à Y220S, et encore plus faiblement à Y220N, bien que toutes ces affinités restent dans des plages jugées prometteuses par les chimistes médicinaux.
Voir la pièce de réparation moléculaire en détail atomique
Des structures cristallographiques à haute résolution ont fourni une explication visuelle. Dans les trois mutants, rezatapopt s’insère dans la cavité créée par la mutation selon une pose conservée : son échafaudage central remplit l’intervalle, une extrémité s’enfonce profondément dans la poche avec un groupe d’atomes de fluor, et l’autre extrémité interagit avec une boucle protéique voisine. Le médicament établit un réseau de contacts, incluant un atome de fluor judicieusement placé qui engage le squelette protéique. Pour Y220S, ces interactions sont conservées avec seulement des décalages mineurs, permettant une forte stabilisation. Pour Y220N, en revanche, la liaison du médicament contraint la chaîne latérale de l’asparagine à se tourner vers le cœur non polaire de la protéine d’une manière énergétiquement défavorable, et certains contacts avec « l’ancre » fluorée du médicament sont perdus. Cet ajustement forcé explique à la fois l’affinité plus faible et le sauvetage incomplet de la stabilité. 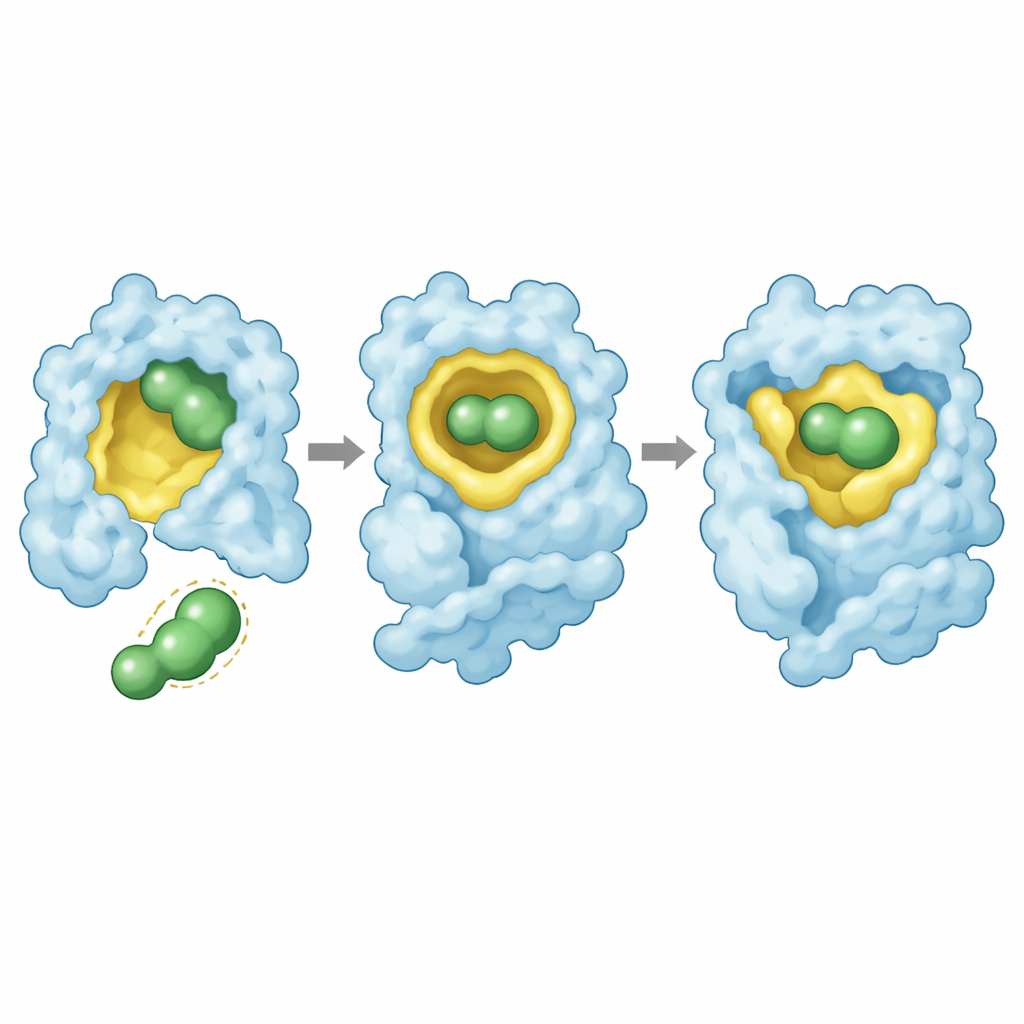
De la réparation de la protéine au comportement cellulaire
Le test crucial est de savoir si cette stabilisation redonne à p53 son rôle protecteur à l’intérieur de cellules vivantes. Les chercheurs ont modifié des cellules de cancer du poumon dépourvues de p53 naturel pour exprimer les variantes Y220C, Y220S, Y220N ou Y220H. Traitées par rezatapopt, les cellules portant Y220C ont montré une puissante activation des gènes cibles classiques de p53 impliqués dans l’arrêt du cycle cellulaire et l’induction de la mort cellulaire. Les cellules Y220S ont affiché un profil très similaire : récupération de la forme repliée et active de p53, forte activation génique, ralentissement de la prolifération et augmentation de la mort cellulaire, mais seulement à des concentrations du médicament plus de dix fois supérieures à celles nécessaires pour Y220C. Les cellules Y220N, en comparaison, n’ont montré aucune activation claire des gènes cibles à des doses tolérées et sont restées majoritairement dans un état mal replié, bien que de légers effets tardifs sur la croissance suggèrent un sauvetage fonctionnel partiel.
Ce que cela signifie pour les patients et la conception future de médicaments
Pour les personnes dont les tumeurs portent la mutation Y220S, ces résultats sont prudemment encourageants : rezatapopt peut, en principe, restaurer les fonctions protectrices de p53, mais seulement à des doses nettement plus élevées, difficiles à atteindre de manière sûre chez les patients. Pour Y220N, le médicament actuel semble insuffisant pour réparer pleinement p53 dans des conditions réalistes. Néanmoins, les plans structuraux fournis par ce travail expliquent pourquoi la conception actuelle est sous-optimale et comment de futures molécules pourraient être ajustées pour engager les trois chaînes latérales mutantes sans les contraindre dans des positions défavorables. Autrement dit, créer un véritable médicament de réparation « pan-Y220 » semble complexe mais réalisable, et augmenterait modestement le nombre de patients susceptibles de bénéficier de cette stratégie émergente consistant à réparer, plutôt qu’à remplacer, le suppresseur de tumeur endogène.
Citation: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Mots-clés: réactivation de p53, rezatapopt, mutation Y220C, médecine de précision contre le cancer, stabilisation des protéines