Clear Sky Science · fr
La déubiquitination par OTUD4 stabilise l’EGFR et active la voie PI3K/AKT pour favoriser l’invasivité du cancer du sein triple négatif
Pourquoi cette recherche est importante pour le cancer du sein
Le cancer du sein triple négatif est l’une des formes les plus difficiles à traiter car il ne présente pas les marqueurs hormonaux et de croissance que ciblent de nombreux médicaments. Cette étude met au jour une molécule « protectrice » jusque-là cachée qui aide les cellules cancéreuses à maintenir activé un puissant interrupteur de croissance. En comprenant ce système de soutien invisible, les chercheurs pourraient trouver de nouvelles façons d’interrompre les signaux qui alimentent la croissance et la dissémination tumorales.
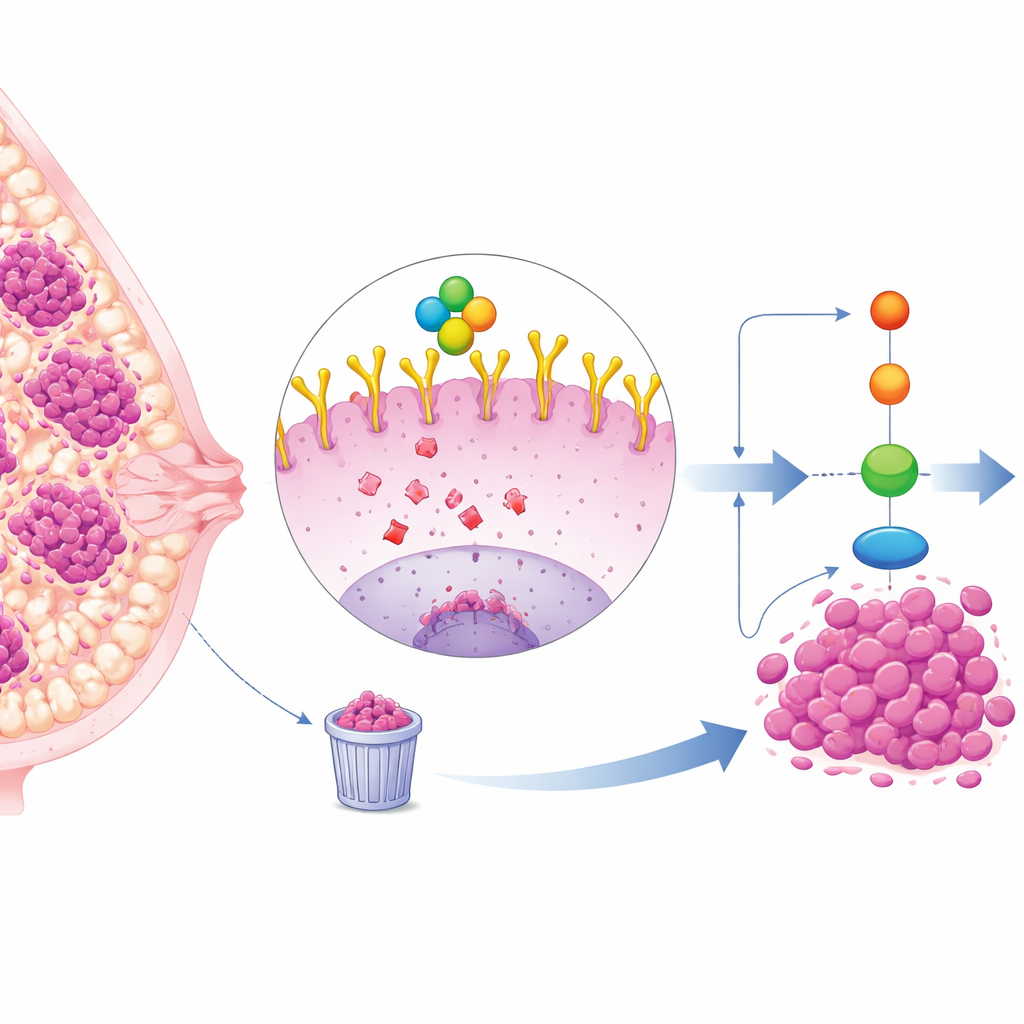
Un sous-type de cancer du sein difficile à traiter
Le cancer du sein triple négatif (TNBC) représente environ un quart des cas de cancer du sein et a tendance à croître et se propager plus rapidement que d’autres sous-types. Parce que les cellules TNBC ne portent pas de récepteurs d’œstrogène, de progestérone ou HER2, les thérapies ciblées classiques sont moins efficaces, laissant la chimiothérapie et la chirurgie comme principales options. De nombreux tumeurs TNBC affichent cependant des niveaux élevés d’une protéine de surface cellulaire appelée EGFR, qui agit comme une antenne pour capter les signaux de croissance et de survie. Des niveaux élevés d’EGFR sont associés à un mauvais pronostic, mais les médicaments bloquant directement l’EGFR ont donné des résultats décevants en clinique, ce qui suggère l’existence de couches de régulation plus profondes.
Trouver un assistant caché de la croissance tumorale
Les chercheurs se sont concentrés sur OTUD4, une enzyme qui enlève de petites étiquettes protéiques appelées ubiquitines d’autres protéines. Ces étiquettes agissent souvent comme des signaux d’élimination, marquant les protéines pour qu’elles soient détruites ; les retirer peut donc stabiliser et protéger la protéine marquée. À partir de larges bases de données sur le cancer et d’échantillons de tissus de patients, l’équipe a montré que OTUD4 est présent à des niveaux plus élevés dans les tumeurs et lignées cellulaires TNBC que dans le tissu mammaire normal. Les patients dont les tumeurs exprimaient davantage OTUD4 semblaient avoir une survie plus mauvaise, ce qui suggère que OTUD4 se comporte comme un oncogène, un gène favorisant la progression tumorale.
Comment OTUD4 rend les cellules cancéreuses plus agressives
Pour tester le rôle réel d’OTUD4 dans les cellules TNBC, les scientifiques ont réduit son expression dans deux lignées cellulaires TNBC largement étudiées. Lorsque OTUD4 était diminué, les cellules cancéreuses proliféraient plus lentement, formaient moins de colonies et étaient moins capables de migrer dans des essais de cicatrisation et de Transwell, autant de signes d’une agressivité réduite. À l’inverse, la surexpression d’OTUD4 entraînait une prolifération plus rapide et une mobilité accrue, renforçant l’idée qu’OTUD4 est un moteur du comportement malin. Chez la souris, les tumeurs issues de cellules dépourvues d’OTUD4 croissaient plus lentement et montraient une baisse des marqueurs de division cellulaire et des signaux de croissance, confirmant ces effets in vivo.
Un bouclier moléculaire qui protège l’EGFR
En creusant le mécanisme, l’équipe a utilisé des cribles d’interaction protéique et des essais biochimiques pour identifier l’EGFR comme partenaire d’interaction direct d’OTUD4. Ils ont constaté qu’OTUD4 se lie à une région spécifique de l’EGFR et enlève des chaînes d’ubiquitine liées en K48, le type d’étiquette qui marque habituellement les protéines pour la destruction par le système de recyclage cellulaire. Quand OTUD4 était réduit, l’EGFR se dégradait plus rapidement, alors que l’activité de son gène restait inchangée, montrant qu’OTUD4 agit après la synthèse de l’EGFR, et non au niveau de l’ADN ou de l’ARN. Le blocage du système d’élimination des protéines restaurait les niveaux d’EGFR, soulignant que l’étape clé est la protection contre la dégradation. Avec davantage d’EGFR stable à la surface cellulaire, une voie de signalisation intracellulaire majeure, la voie PI3K/AKT/mTOR, reste activée, stimulant la croissance et la survie cellulaires.
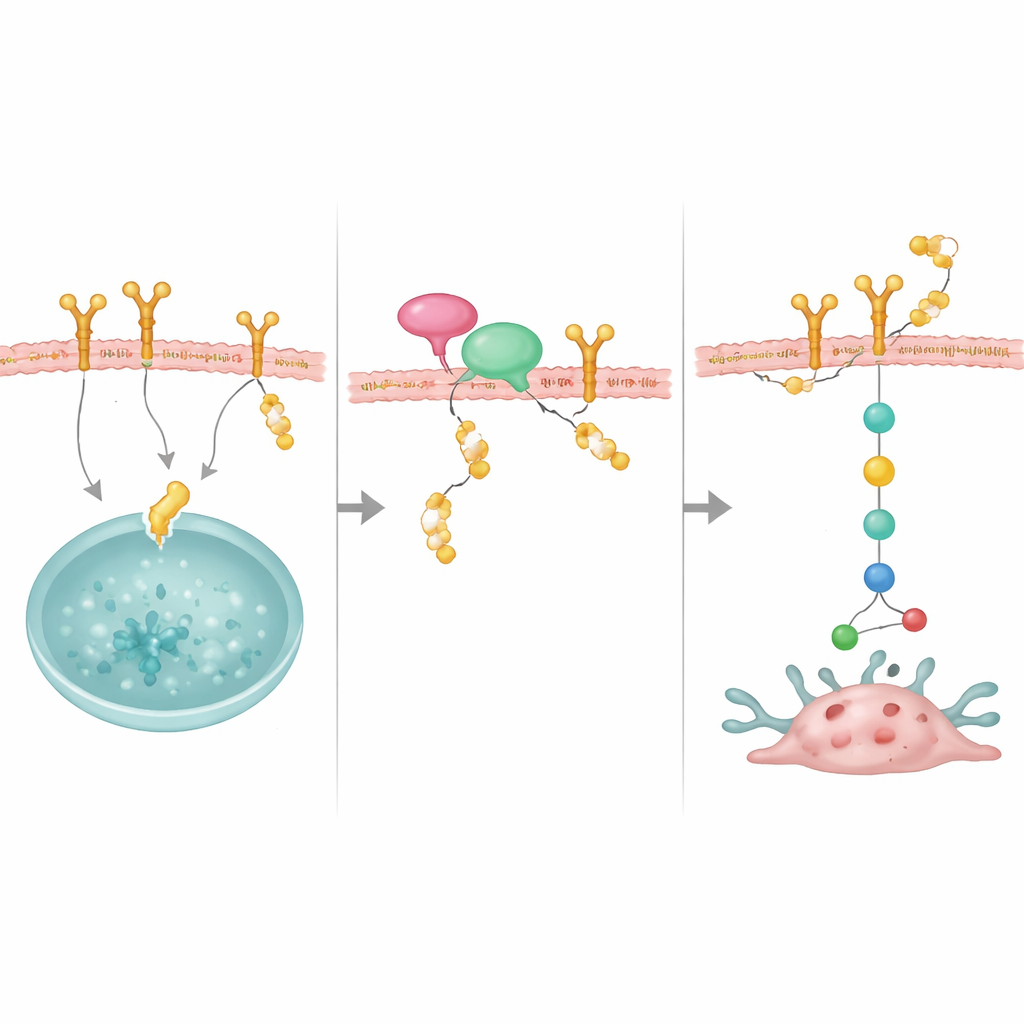
Un adaptateur qui amène le protecteur vers sa cible
L’étude a également mis en évidence un partenaire important, NRP1, une protéine membranaire auparavant liée aux cancers du sein agressifs. NRP1 se lie à la fois à OTUD4 et à l’EGFR et aide à positionner OTUD4 pour sauver l’EGFR de la destruction. Lorsque NRP1 était réduit, l’EGFR devenait moins stable et ses signaux de croissance faiblissaient, bien que les niveaux d’OTUD4 ne changent pas. La surexpression d’OTUD4 pouvait partiellement compenser la perte de NRP1, ce qui suggère que NRP1 agit comme une plateforme d’ancrage recrutant OTUD4 vers l’EGFR. Ensemble, ces molécules forment un complexe stabilisateur qui maintient des niveaux élevés d’EGFR à la surface cellulaire.
Quelles implications pour les traitements futurs
En révélant comment OTUD4 et NRP1 coopèrent pour protéger l’EGFR de la dégradation, cette étude identifie un nouveau point de contrôle d’un signal de croissance clé dans le cancer du sein triple négatif. Plutôt que d’essayer de bloquer l’activité d’EGFR au niveau de son site actif, les thérapies futures pourraient viser à perturber les actions protectrices d’OTUD4 ou son recrutement par NRP1, réduisant les niveaux d’EGFR et atténuant la voie PI3K/AKT qui alimente la croissance tumorale. Bien que des travaux supplémentaires soient nécessaires pour trouver des inhibiteurs d’OTUD4 sûrs et efficaces et pour comprendre les voies d’échappement possibles utilisées par les cellules cancéreuses, ces découvertes ouvrent des pistes prometteuses pour des traitements plus ciblés contre ce sous-type de cancer du sein difficile à traiter.
Citation: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Mots-clés: cancer du sein triple négatif, signalisation EGFR, OTUD4, voie PI3K AKT, dégradation des protéines