Clear Sky Science · fr
La déshydrogénase acyl-CoA à chaîne courte initie la déméthylation et la fuite de l’ADNmt pour stimuler l’immunité antitumorale dans le cancer colorectal
Pourquoi nos propres cellules cachent parfois le cancer au système immunitaire
Le cancer colorectal est l’un des tumeurs les plus meurtrières au monde, en partie parce que les défenses immunitaires de l’organisme échouent souvent à le reconnaître et à l’attaquer. Cette étude révèle un lien inattendu entre la façon dont les cellules cancéreuses brûlent les graisses, la gestion de l’ADN par leurs petites centrales énergétiques (les mitochondries) et le déclenchement ou non d’une alerte du système immunitaire. En reconstituant cette chaîne d’événements, les chercheurs mettent aussi en lumière un composé naturel ancien, l’hypéricine, comme piste pour réveiller l’attaque immunitaire dans le cancer colorectal.
Un « gardien » mitochondrial absent dans les tumeurs du côlon
L’équipe a commencé par analyser de larges jeux de données humains et murins pour identifier des gènes métaboliques constamment modifiés dans le cancer colorectal. Une enzyme s’est distinguée : la déshydrogénase acyl-CoA à chaîne courte, ou ACADS, qui aide normalement les mitochondries à dégrader les acides gras courts. Dans des échantillons de patients et dans plusieurs modèles murins, les niveaux d’ACADS étaient nettement plus faibles dans les tissus tumoraux que dans le côlon voisin sain. Lorsque les scientifiques ont réduit ACADS dans des cellules de cancer du côlon de souris, les tumeurs ont grandi plus rapidement et de façon plus agressive ; augmenter ACADS a ralenti la croissance tumorale. Des souris génétiquement modifiées pour manquer spécifiquement d’ACADS dans l’épithélium intestinal ont développé davantage et de plus grosses tumeurs dans un modèle chimique de cancer associé à la colite, appuyant l’idée qu’ACADS agit comme un suppresseur de tumeur dans l’intestin.
Comment les tumeurs étouffent les signaux d’alarme immunitaire
Ces effets sur la croissance ne pouvaient pas s’expliquer uniquement par la vitesse de multiplication des cellules cancéreuses en culture, qui variait peu. Au contraire, la perte d’ACADS n’a favorisé la croissance tumorale que chez des animaux dotés d’un système immunitaire intact, ce qui indique des modifications du microenvironnement tumoral. Des analyses unicellulaires de cancers colorectaux humains ont montré que les tumeurs à faible ACADS étaient entourées de davantage de cellules tumorales et de cellules immunitaires suppressives — comme des cellules suppressives dérivées du myéloïde, certains macrophages et des lymphocytes T régulateurs — et contenaient moins de lymphocytes T effecteurs et de cellules NK. Ce profil dessine un « quartier immunosuppresseur » qui abrite la tumeur et la protège des attaques. 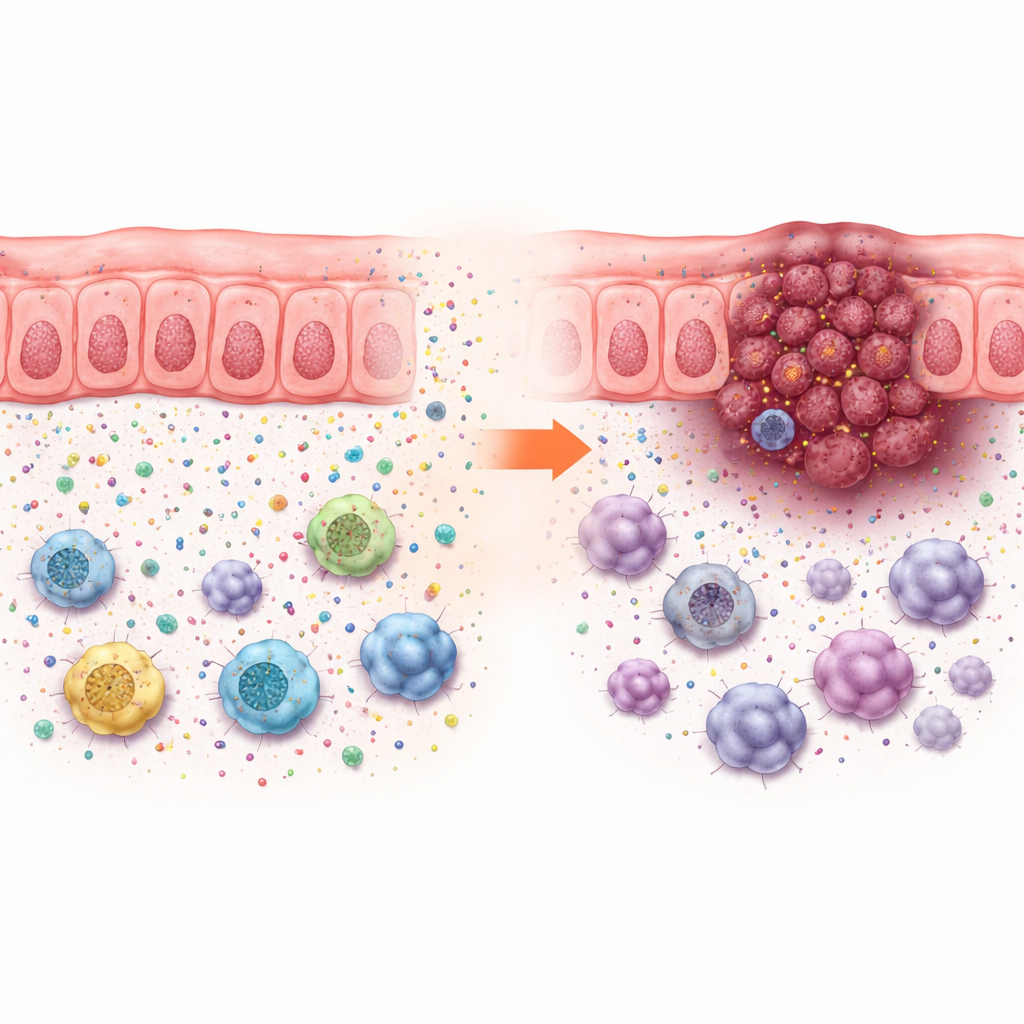
Fuite d’ADN mitochondrial comme déclencheur caché
Qu’est-ce qui relie une enzyme de dégradation des lipides à un capteur immunitaire de l’ADN ? La réponse se trouve dans l’ADN mitochondrial (ADNmt). En cas de stress, des fragments d’ADNmt peuvent fuir les mitochondries vers le compartiment cytosolique, où cGAS les détecte comme un signal de danger. Les chercheurs ont montré que les cellules cancéreuses déficientes en ACADS présentaient moins d’ADNmt dans ce compartiment cytosolique, bien que la quantité totale d’ADNmt restât inchangée. Bloquer la fuite d’ADNmt dans des cellules riches en ACADS coupait la voie cGAS–STING, confirmant que ces fragments d’ADN échappés constituent l’alarme critique. Fait surprenant, des facteurs classiques de stress mitochondrial tels que les espèces réactives de l’oxygène, les pics calciques ou des changements majeurs de la morphologie mitochondriale n’expliquaient pas complètement la différence. L’étude met plutôt en cause les « portes » de la membrane mitochondriale et, surtout, les marques chimiques portées par l’ADNmt lui‑même. 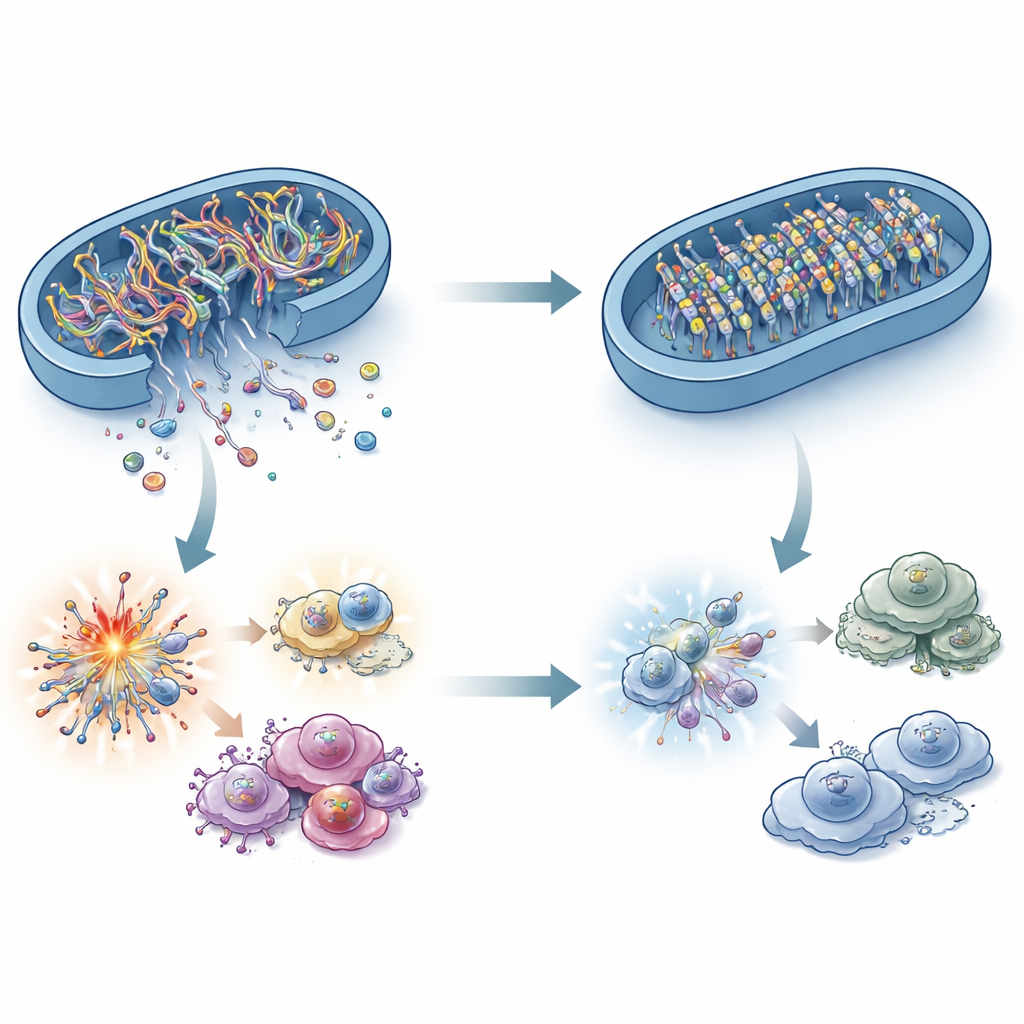
Un partenaire méthylant l’ADN qui verrouille l’alarme
Par des cribles d’interaction protéique, ACADS a été trouvé associé à une forme de l’enzyme de méthylation de l’ADN DNMT1 qui se localise aux mitochondries. Lorsque ACADS disparaissait, ce DNMT1 mitochondrial s’accumulait, ajoutant des groupes méthyle supplémentaires sur l’ADNmt. Ces marques rendent l’ADNmt plus stable et moins susceptible de se fragmenter et de fuir. Surcharger les cellules en DNMT1 mitochondrial a réduit la fuite d’ADNmt, atténué la signalisation cGAS–STING et accéléré la croissance tumorale, tandis que bloquer DNMT1 avec la décitabine a restauré la fuite d’ADNmt et ralenti les tumeurs déficientes en ACADS. Les échantillons de patients reflétaient ces observations : un faible ACADS coïncidait avec un DNMT1 mitochondrial élevé, une signalisation STING affaiblie, moins de lymphocytes T effecteurs, davantage de cellules immunosuppressives et une moindre probabilité de réponse aux immunothérapies ciblant les points de contrôle.
Réanimer les défenses immunitaires avec un vieux composé
Pour vérifier si cette voie pouvait être exploitée thérapeutiquement, les chercheurs ont utilisé un criblage informatisé pour chercher des molécules se liant à ACADS. Ils ont identifié l’hypéricine, un pigment naturel déjà testé comme traitement photo‑activé pour certains lymphomes cutanés. Dans des cellules de cancer colorectal, l’hypéricine a augmenté les niveaux d’ACADS, réduit le DNMT1 mitochondrial, favorisé la fuite d’ADNmt et réactivé la voie cGAS–STING — changements dépendants de la présence d’ACADS. Dans des modèles tumoraux murins et dans des cultures à court terme de tumeurs colorectales humaines, le traitement par l’hypéricine a réduit la taille des tumeurs ou a fait basculer les cellules immunitaires vers un état plus actif, riche en lymphocytes T. Bien que des travaux supplémentaires soient nécessaires avant toute utilisation clinique, ces résultats suggèrent que réactiver pharmacologiquement ACADS pourrait aider à convertir une tumeur « froide » et immunosuppressive en une tumeur plus réceptive à l’immunothérapie.
Ce que cela signifie pour les patients et les traitements futurs
Concrètement, ce travail montre que certains cancers colorectaux prolifèrent en partie parce qu’ils éteignent une enzyme mitochondriale qui favorise normalement la fuite de petits fragments d’ADN dans le cytosol, où ils servent de signaux d’alerte pour mobiliser le système immunitaire. En laissant un partenaire méthylant verrouiller cet ADN mitochondrial, les tumeurs déficientes en ACADS gardent ces signaux cachés et échappent à la détection immunitaire. Restaurer l’activité d’ACADS, par exemple avec des composés de type hypéricine, pourrait rouvrir ce système d’alarme mitochondrial, renforcer l’immunité antitumorale et améliorer les réponses aux immunothérapies existantes. ACADS, le DNMT1 mitochondrial et l’activité de la voie STING pourraient donc servir de biomarqueurs et de cibles utiles dans la recherche de traitements plus efficaces contre le cancer colorectal.
Citation: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Mots-clés: cancer colorectal, immunité antitumorale, ADN mitochondrial, métabolisme des lipides, voie cGAS-STING