Clear Sky Science · fr
Cibler fused in sarcoma (FUS) : une nouvelle stratégie antisens pour traiter la fibrose pulmonaire idiopathique
Pourquoi la cicatrisation des poumons importe
La fibrose pulmonaire idiopathique (FPI) est une maladie pulmonaire implacable dans laquelle les délicates alvéoles se transforment lentement en tissu cicatriciel rigide, rendant chaque respiration plus difficile. Les traitements actuels peuvent ralentir cette fibrose mais ne peuvent ni l’arrêter ni l’inverser. Cette étude explore une nouvelle cible appelée FUS, une protéine qui aide les cellules à gérer leurs messages génétiques, et teste si l’éteindre avec un brin conçu de matière semblable à l’ADN pourrait calmer le processus de cicatrisation et aider les poumons endommagés à se réparer.
Un contrôleur du trafic cellulaire déréglé
FUS est une protéine qui réside normalement dans le noyau cellulaire, où elle participe à la gestion du traitement et de l’utilisation des ARN — les copies opérationnelles de nos gènes. Dans des maladies cérébrales comme la SLA, FUS peut mal fonctionner, quitter le noyau, s’agréger dans le cytoplasme et perturber le fonctionnement normal de la cellule. Les auteurs se sont demandé si un dysfonctionnement similaire pouvait entraîner la fibrose dans la FPI. Ils ont étudié des fibroblastes pulmonaires — les cellules du tissu conjonctif qui déposent le matériau cicatriciel — provenant de patients atteints de FPI et de donneurs sains. Dans les cellules FPI, les niveaux de FUS étaient globalement plus élevés et, de façon cruciale, une bien plus grande quantité de FUS se trouvait dans le cytoplasme que dans les cellules saines. Grâce à la microscopie électronique à haute résolution, ils ont confirmé que cette protéine était anormalement abondante hors du noyau, suggérant que son contrôle habituel des ARN pouvait être perturbé dans les poumons fibreux. 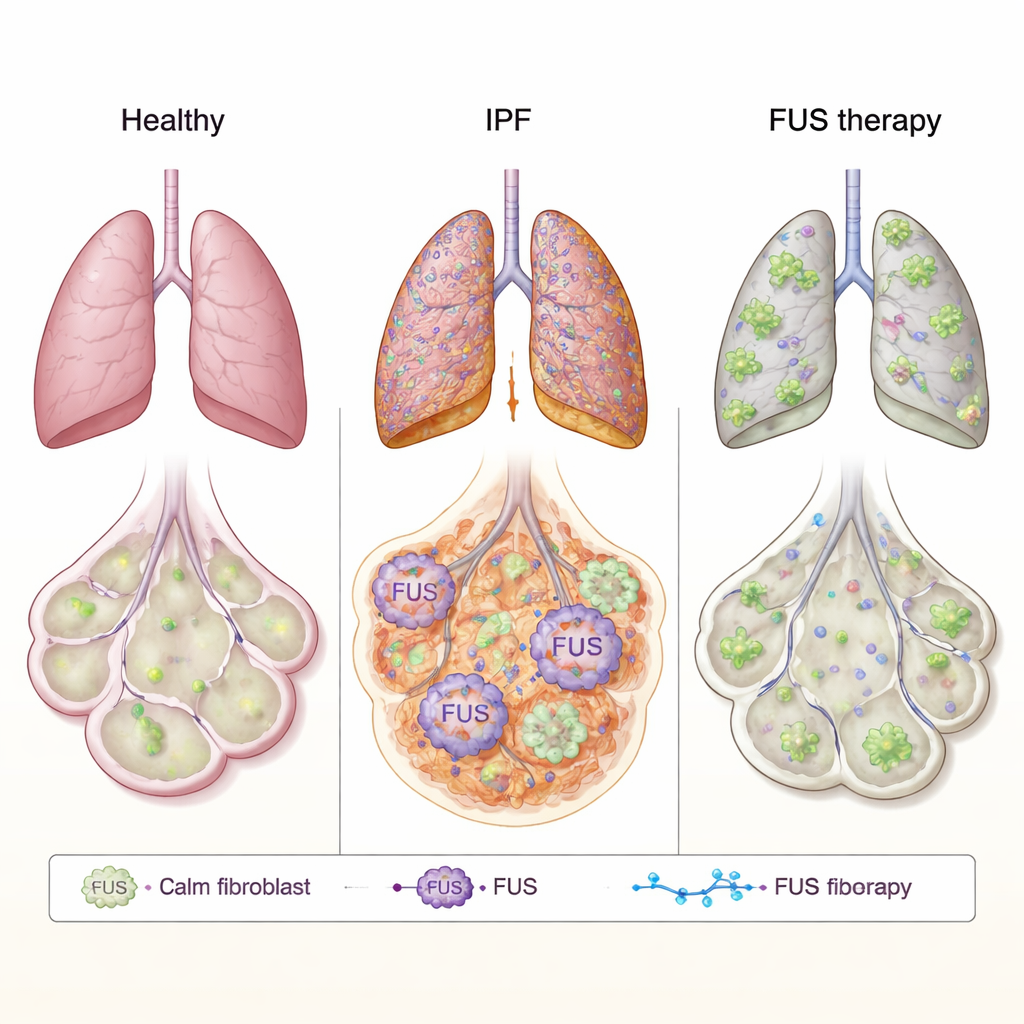
Comment FUS alimente les cellules cicatrisantes
Pour comprendre l’action réelle de cette protéine mal comportée, les chercheurs ont augmenté l’expression de FUS dans des fibroblastes sains et l’ont réduite dans des fibroblastes FPI. Un excès de FUS a poussé les cellules saines à se diviser plus rapidement, tandis que la diminution de FUS dans les cellules FPI a ralenti leur prolifération et leur migration — deux comportements centraux dans la formation de cicatrices. L’équipe a ensuite utilisé une technique qui « fige » les interactions protéine–ARN et identifie les ARN liés à FUS. Dans les fibroblastes FPI, FUS était retrouvé associé à de nombreux messages génétiques qui favorisent la fibrose, y compris ceux codant pour le collagène, des facteurs de croissance comme le TGF‑β et des signaux inflammatoires. En d’autres termes, FUS agissait comme un point de convergence reliant tout un réseau de messages pro‑cicatrisation.
Éteindre le signal avec un médicament de précision
L’étude a testé un oligonucléotide antisens appelé ION363 — un court brin chimiquement modifié conçu pour se lier à l’ARN de FUS et déclencher sa destruction. Lorsque les fibroblastes FPI ont été traités par ION363, les niveaux de FUS ont chuté, les cellules ont ralenti leur prolifération et leur migration, et les gènes clés impliqués dans la construction de la cicatrice se sont tus. Fait important, cet effet ne reposait pas sur la mort cellulaire ni sur l’induction d’un état sénescent : il semblait plutôt réinitialiser leur comportement. Appliqué à des tranches fines de tissu pulmonaire FPI maintenues vivantes en laboratoire, le traitement a atténué de larges groupes de gènes liés à la matrice extracellulaire, à l’inflammation et à l’épithélium anormal, tandis que des gènes associés à la production de surfactant et à la fonction alvéolaire saine ont été renforcés. Le traitement a également réduit la coloration du collagène et augmenté les marqueurs des cellules de surface pulmonaire fonctionnelles, suggérant une bascule de la cicatrisation vers la réparation.
Aider les alvéoles endommagées à se régénérer
Étant donné que les cellules qui tapissent les alvéoles — les cellules alvéolaires de type II — sont cruciales pour la réparation pulmonaire, les chercheurs ont construit des « alvéolosphères » tridimensionnelles à partir de cellules de patients pour imiter de mini‑unités pulmonaires. Dans les cultures issues de patients FPI, ces structures survivent normalement mal. Avec le traitement par ION363, davantage d’alvéolosphères se sont formées, ont grandi davantage et ont montré une activité lysosomale accrue — un signe caractéristique du renouvellement actif. Des colorations détaillées ont révélé plus de cellules portant des marqueurs de cellules matures échangeant des gaz, indiquant que le silence de FUS a non seulement calmé les fibroblastes, mais a aussi encouragé l’épithélium blessé à reconstruire une surface plus saine. 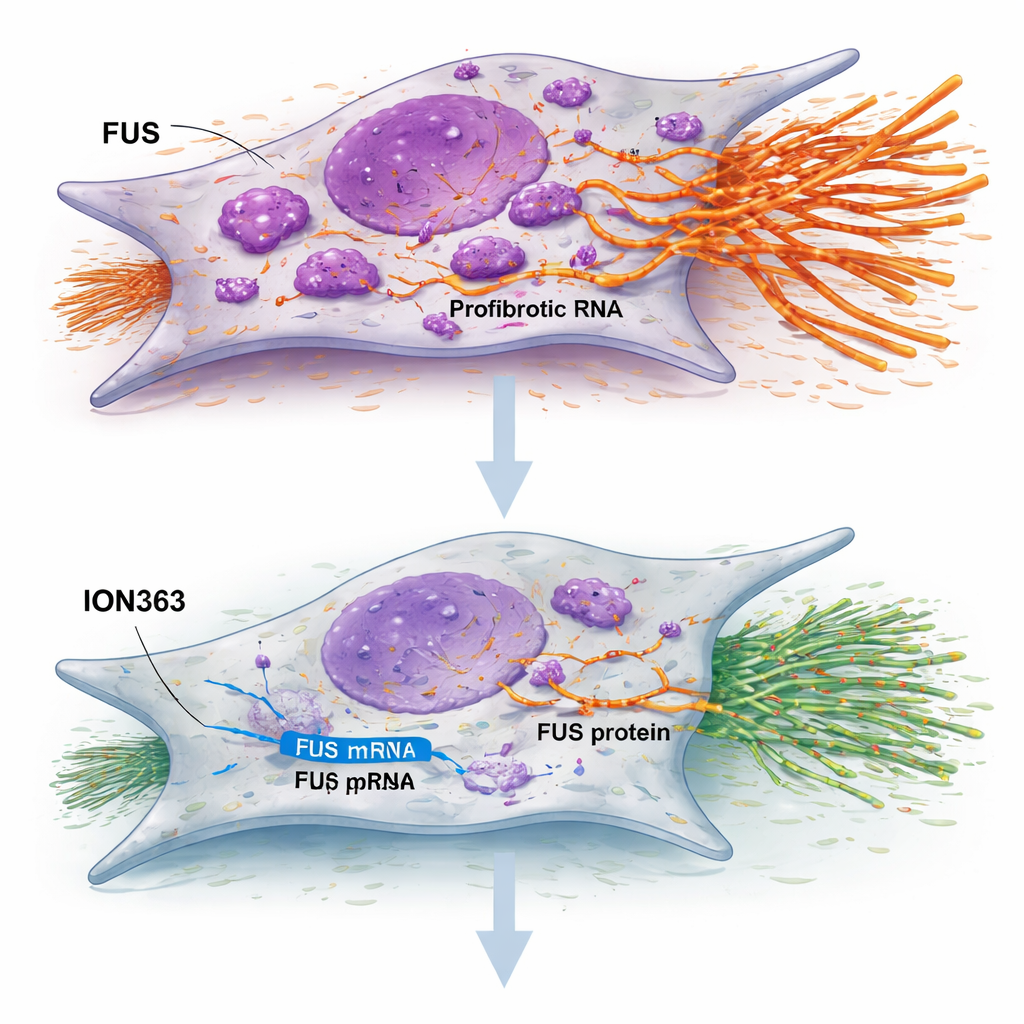
Ce que cela pourrait signifier pour les patients
En somme, le travail décrit FUS comme un interrupteur maître dans la FPI, reliant des fibroblastes hyperactifs formant des cicatrices à un échec de la réparation des délicates alvéoles. En abaissant FUS avec un médicament antisens ciblé, les chercheurs ont pu réduire les programmes géniques profibrotiques, limiter l’accumulation de collagène et favoriser la régénération dans des modèles pulmonaires dérivés de patients. Bien que cette approche soit encore au stade de laboratoire et nécessite des tests rigoureux chez l’animal et en essais cliniques, elle suggère qu’un jour la FPI pourrait être traitée non seulement en ralentissant la fibrose, mais en rééquilibrant directement les programmes cellulaires qui contrôlent la lésion et la réparation pulmonaires.
Citation: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Mots-clés: fibrose pulmonaire idiopathique, oligonucléotide antisens, protéine FUS, fibrose pulmonaire, réparation alvéolaire