Clear Sky Science · fr
La protéine E7 du papillomavirus humain 16 renforce les caractéristiques souches des cellules en régulant l’axe APC2/SPIN4/β-caténine dans le cancer du col de l’utérus
Pourquoi cette recherche est importante
Le cancer du col de l’utérus reste une cause majeure de mortalité chez les femmes dans le monde, en particulier là où le dépistage et la vaccination sont limités. Les chercheurs savent que certains types de papillomavirus humain (HPV), en particulier le HPV16, sont des agents clés de cette maladie, mais les mécanismes par lesquels le virus maintient les tumeurs agressives et sujettes aux récidives ne sont pas encore totalement élucidés. Cette étude explore comment une protéine virale, appelée E7, contribue à maintenir une petite mais puissante population de « cellules souches cancéreuses » capables d’alimenter la croissance tumorale, la dissémination et la résistance aux traitements — ce qui fournit des pistes pour des thérapies plus ciblées.
D’un virus courant à un cancer dangereux
La plupart des infections à HPV se résolvent spontanément, mais une infection persistante par des types à haut risque peut transformer les cellules saines du col en cellules cancéreuses. La protéine virale E7 est au cœur de ce processus : elle désactive des mécanismes de contrôle qui régulent normalement la division cellulaire. Des travaux antérieurs de ce groupe ont montré que E7 du HPV16 renforce les propriétés de type souche des cellules du cancer du col, les rendant plus difficiles à éradiquer. Dans l’étude actuelle, l’équipe a cherché à cartographier les réseaux génétiques contrôlés par E7 afin de comprendre précisément comment il permet à ces cellules dangereuses de survivre et de prospérer.
Suivre l’impact de E7 à l’intérieur des cellules tumorales
Pour suivre l’influence de E7, les chercheurs ont utilisé des lignées cellulaires de cancer du col cultivées en laboratoire et réduit les niveaux de E7 au moyen de petits ARN interférents, un outil qui silencie temporairement des gènes spécifiques. Ils ont ensuite mesuré quelles activités géniques étaient modifiées à l’échelle du génome. Ils ont combiné cela avec une batterie de tests fonctionnels : vitesse de prolifération, capacité de migration et d’invasion à travers des membranes artificielles, et aptitude à former des amas sphériques en culture — un signe distinctif des cellules souches cancéreuses. Ils ont aussi examiné des tumeurs cultivées chez la souris et analysé de larges ensembles de données publiques sur le cancer pour voir comment leurs observations correspondaient aux profils de patients.
Un rôle surprenant pour une voie connue
Les expériences de cartographie génétique ont fortement mis en évidence la voie Wnt/β-caténine, un régulateur bien connu des cellules souches normales et de nombreux cancers. Lorsque E7 était silencée, les niveaux de β-caténine diminuaient, ce qui suggère que cette voie était désactivée. Parallèlement, l’équipe a observé de forts changements au niveau d’un gène appelé APC2. Dans de nombreux autres cancers, les protéines apparentées à APC agissent comme des freins sur la signalisation Wnt, contribuant à limiter la croissance cellulaire. Ici, cependant, les cellules du cancer du col semblaient utiliser APC2 d’une façon inattendue : lorsque APC2 était réduit, les cellules cancéreuses proliféraient plus lentement, étaient moins capables de migrer et d’envahir, et perdaient leurs caractéristiques de type souche. Chez la souris, des tumeurs avec un silence prolongé d’APC2 étaient beaucoup plus petites, tandis que les animaux restaient en bonne santé, suggérant une fenêtre thérapeutique potentiellement sûre.
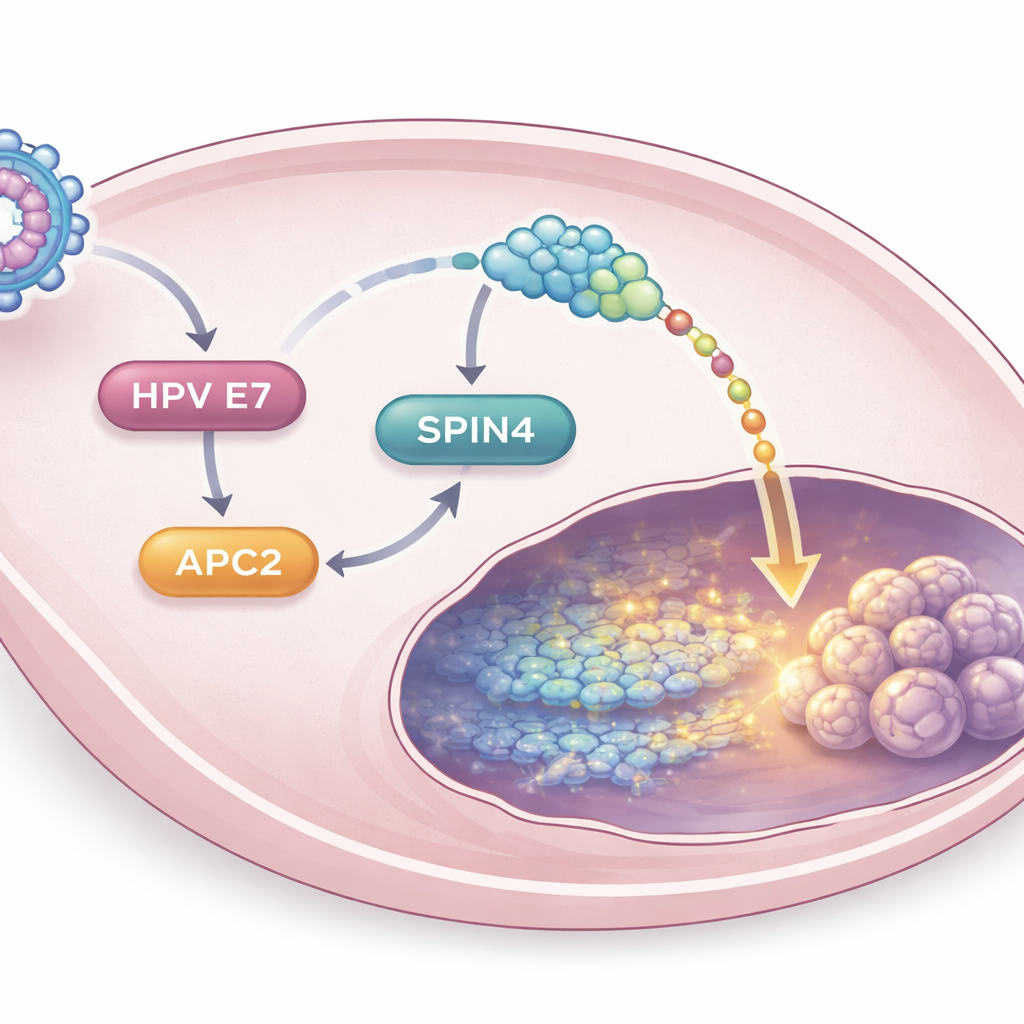
Dresser une nouvelle chaîne favorisant le cancer
En approfondissant, les scientifiques ont montré que E7 du HPV16 augmente indirectement les niveaux d’APC2 via une autre protéine appelée E2F1, qui active des ensembles de gènes liés à la croissance. Une fois élevé, APC2 stimule à son tour l’activité d’une protéine moins connue, SPIN4. L’analyse des données tumorales humaines a révélé que SPIN4 est plus abondant dans les cancers du col que dans les tissus normaux, et que des niveaux plus élevés sont associés à une survie plus mauvaise. En laboratoire, l’inhibition de SPIN4 réduisait la capacité d’APC2 à promouvoir la prolifération cellulaire, l’invasion, l’activité Wnt/β-caténine et les comportements de type cellule souche. Dans les expériences chez la souris, les tumeurs déficientes en SPIN4 étaient plus petites et présentaient une diminution des marqueurs associés à la « souche ». Ensemble, ces résultats décrivent une chaîne étape par étape — HPV16 E7 vers APC2 vers SPIN4 vers Wnt/β‑caténine — qui, de manière coordonnée, maintient les cellules du cancer du col agressives et dotées de caractéristiques souches.
Perspectives pour des traitements plus intelligents
Pour le grand public, le message principal est que cette étude identifie un circuit intracellulaire jusque-là méconnu dans les cancers du col pilotés par le HPV. Plutôt que d’agir comme un simple interrupteur marche/arrêt, la protéine virale E7 détourne une série spécifique de protéines hôtes — APC2 et SPIN4 — pour préserver une réserve dangereuse de cellules souches cancéreuses via la voie Wnt/β‑caténine. Cet axe aide non seulement à expliquer pourquoi certaines tumeurs sont si persistantes, mais met aussi en évidence plusieurs nouvelles cibles que des médicaments ou des thérapies combinées pourraient viser, notamment chez les patientes dont les cancers résistent aux traitements standards. En ciblant le circuit en forme de virus qui soutient les cellules « graines » tumorales, les thérapies futures pourraient mieux prévenir la repousse et améliorer les résultats à long terme.
Citation: Shen, T., Ma, Y., Wu, T. et al. Human papillomavirus16 E7 enhances cell stemness by regulating the APC2/SPIN4/β-catenin axis in cervical cancer. Oncogenesis 15, 10 (2026). https://doi.org/10.1038/s41389-026-00602-8
Mots-clés: cancer du col de l’utérus, papillomavirus humain, cellules souches cancéreuses, voie Wnt β-caténine, signalisation oncogénique