Clear Sky Science · fr
Troncation partielle du domaine C-terminal de PTCH1 dans le cancer favorise la tumorigénèse par activation non canonique d'une boucle GLI–PI3K
Pourquoi un petit changement protéique compte dans le cancer du côlon
Le cancer du côlon résulte généralement d'une accumulation lente d'altérations génétiques. Cette étude se penche sur une modification étonnamment minime d'une protéine de surface cellulaire appelée PTCH1 et montre comment l'élagage d'une partie de sa « queue » peut aider les cellules cancéreuses du côlon à croître plus rapidement, à se disséminer plus facilement et à résister potentiellement à certains traitements existants. Comprendre cet interrupteur de croissance caché pourrait ouvrir la voie à des traitements nouveaux et plus ciblés pour un sous‑groupe de patients.
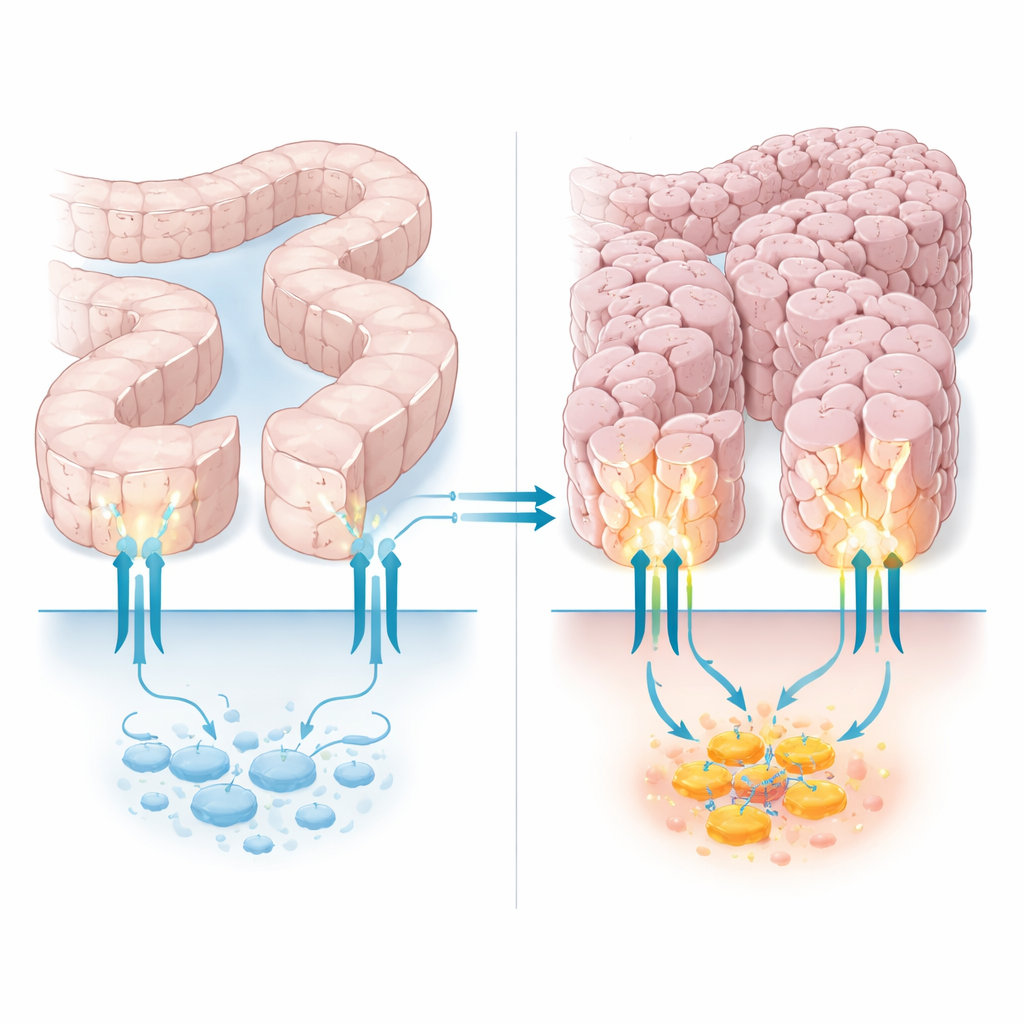
Le garde‑barrière cellulaire avec un emploi secondaire caché
PTCH1 est surtout connu comme le garde‑barrière de la voie Hedgehog, une ligne de communication utilisée par les cellules durant le développement et la réparation tissulaire. Dans son rôle classique, PTCH1 maintient sous contrôle une protéine partenaire, Smoothened, et régule ainsi une famille de contrôleurs de l'ADN appelés GLI. Mais PTCH1 possède aussi une longue queue souple qui pend à l'intérieur de la cellule, servant de piste d'amarrage pour d'autres protéines qui influencent la mort cellulaire, le recyclage des composants cellulaires et plus encore. Des travaux antérieurs ont montré que certains cancers du côlon, de l'estomac et de l'utérus présentent des mutations qui coupent une partie de cette queue interne. Ces mutations ne semblaient pas briser l'interrupteur Hedgehog classique mais rendaient les cellules cancéreuses plus aptes à survivre au stress, suggérant que ce segment de la queue contribue discrètement au rôle suppresseur de tumeur de PTCH1.
Modification génétique des cellules cancéreuses pour tester l'impact
Pour savoir ce que font réellement ces mutations raccourcissant la queue, les chercheurs ont utilisé l'édition génomique CRISPR/Cas9 pour les recréer dans une lignée cellulaire de cancer du côlon. Ils ont comparé deux clones édités, chacun portant une troncation différente de la queue de PTCH1, à des cellules par ailleurs identiques exprimant un PTCH1 normal. Les cellules mutantes se divisaient plus vite, formaient beaucoup plus de colonies et prospéraient même en croissance sans attachement — un comportement associé à la capacité de disséminer dans l'organisme. Lorsqu'elles furent implantées chez la souris, les cellules à queue tronquée ont produit des tumeurs bien plus volumineuses en quelques semaines, avec davantage de cellules en cours de division. Fait important, les cellules éditées produisaient toujours PTCH1 et gardaient sa fonction de garde‑barrière principale, montrant que l'agressivité supplémentaire provient de la perte des fonctions internes spécialisées de la queue, et non d'une simple suppression de PTCH1.
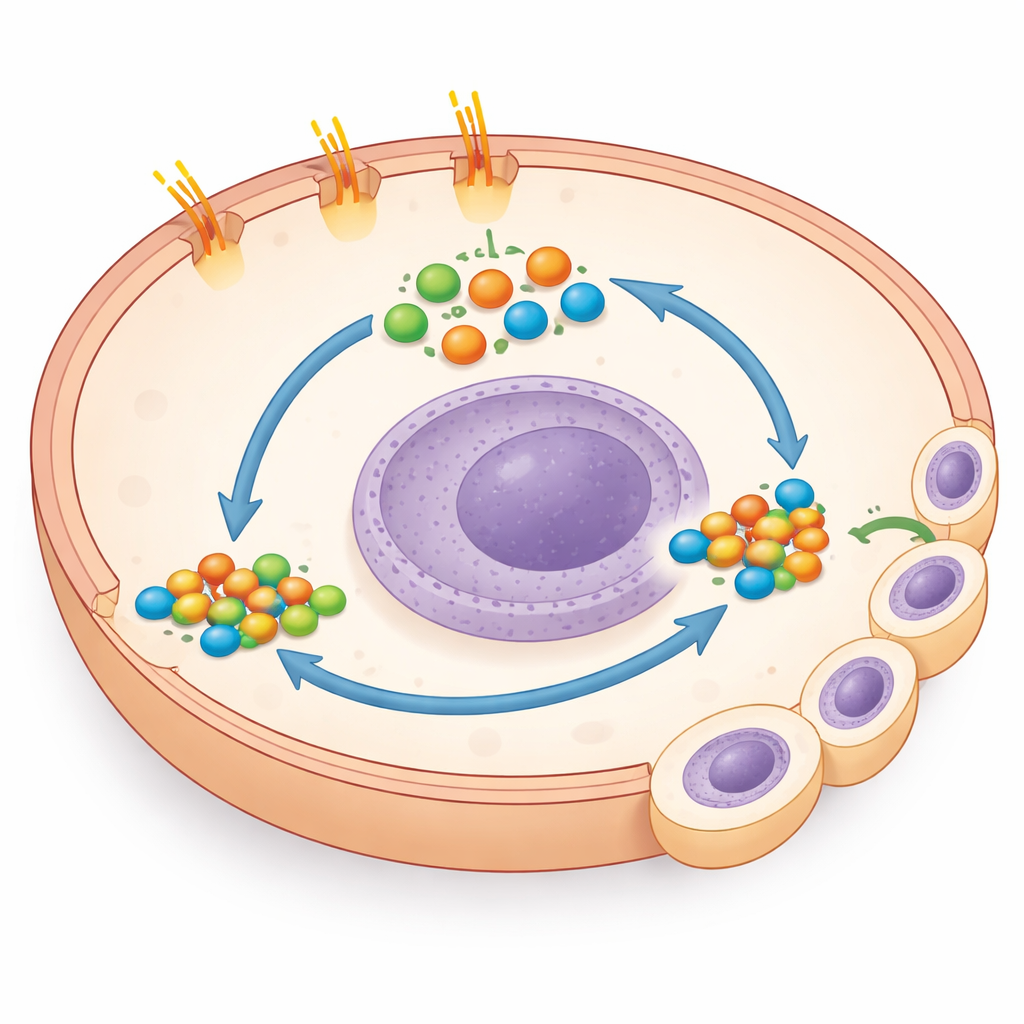
Un raccourci surprenant vers un puissant interrupteur de croissance
En creusant la biologie sous‑jacente, l'équipe a fait une découverte inattendue : les cellules à queue tronquée présentaient des niveaux fortement augmentés de GLI1 et GLI2, moteurs clés de programmes géniques favorisant la croissance et la survie. Normalement, l'activité de GLI augmente lorsque Smoothened est libéré, mais bloquer Smoothened n'avait ici aucun effet. À la place, bloquer directement GLI avec une petite molécule, ou réduire GLI1 par des outils génétiques, a nettement réduit la croissance des cellules mutantes en culture et dans d'autres lignées de cancer du côlon portant naturellement des mutations de la queue de PTCH1. Cela a montré que la perte de la queue active GLI via une voie « non canonique » contournant l'interrupteur Hedgehog habituel, et que les cellules cancéreuses deviennent fortement dépendantes de ce raccourci pour leur comportement agressif.
Plusieurs circuits de croissance s'activent, mais une boucle domine
Par séquençage de l'ARN des cellules, les chercheurs ont identifié des milliers de gènes dont l'activité changeait lorsque la queue de PTCH1 était tronquée. Beaucoup appartenaient à des circuits cancéreux bien connus, notamment ceux contrôlés par le récepteur du facteur de croissance épidermique (EGFR), Ras, et des systèmes de signalisation qui régulent le métabolisme cellulaire et des propriétés de type souche. Les cellules mutantes montraient une activité accrue de l'EGFR et de ses ligands, ainsi qu'une activité supérieure dans deux grandes voies en aval : MAPK et PI3K/Akt. Pourtant, lorsque les scientifiques bloquèrent l'EGFR ou sa branche MAPK, les cellules mutantes ralentissaient seulement partiellement. En revanche, de faibles doses d'inhibiteurs de PI3K freinaient fortement leur croissance et leur formation de colonies et réduisaient les niveaux de GLI1, soulignant PI3K/Akt comme partenaire critique de ce nouveau mécanisme d'activation de GLI.
Une boucle autorenforçante qui alimente la croissance tumorale
Des expériences complémentaires ont révélé un cycle de rétroaction : la troncation de la queue de PTCH1 augmente l'activité de GLI ; GLI, à son tour, contribue à maintenir élevée la signalisation PI3K/Akt ; et PI3K/Akt aide à stabiliser et activer GLI. Disrupter soit GLI soit PI3K rompait cette boucle et privait les cellules mutantes de leur avantage de croissance, tandis qu'une simple stimulation de PI3K/Akt ne pouvait pas contourner un blocage direct de GLI. Les cellules présentaient aussi une activité réduite de la PKA, une enzyme qui, en temps normal, marque les protéines GLI pour leur inactivation, ce qui incline probablement encore la balance en faveur des programmes pilotés par GLI.
Ce que cela peut signifier pour les traitements futurs
Pour les patients, le message clé est que certains cancers du côlon portent des mutations de la queue de PTCH1 qui câblent discrètement une boucle de rétroaction positive GLI–PI3K, aidant les tumeurs à croître et à échapper aux médicaments visant l'interrupteur Hedgehog plus familier ou la voie EGFR–MAPK. Ces tumeurs pourraient au contraire être particulièrement vulnérables à des traitements qui inhibent directement GLI ou ciblent PI3K/Akt. Le travail suggère que séquencer PTCH1 dans les tumeurs du côlon — en particulier celles du côté droit du côlon, où ces mutations sont plus fréquentes — pourrait aider à identifier les patients susceptibles de bénéficier de stratégies ciblant PI3K ou GLI, transformant ainsi une subtile élagation protéique en un indice thérapeutique utile.
Citation: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Mots-clés: cancer du côlon, signalisation Hedgehog, mutations de PTCH1, facteurs de transcription GLI, voie PI3K Akt